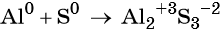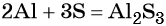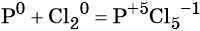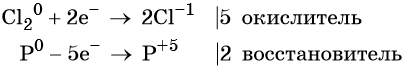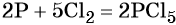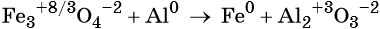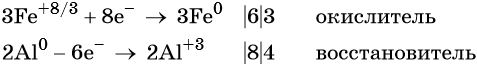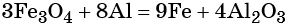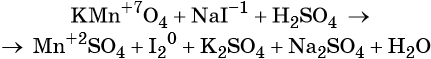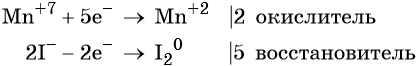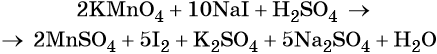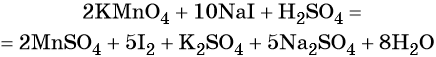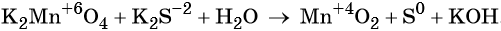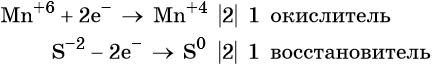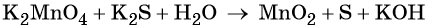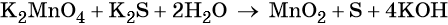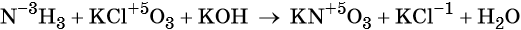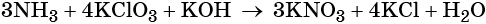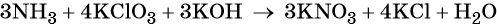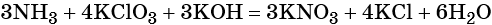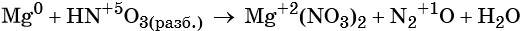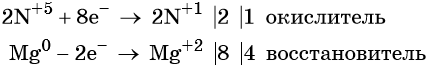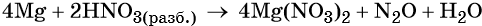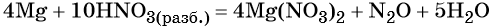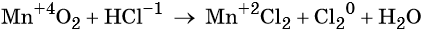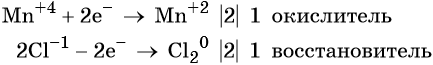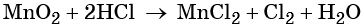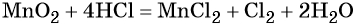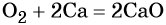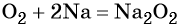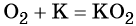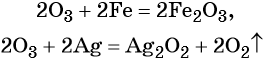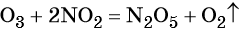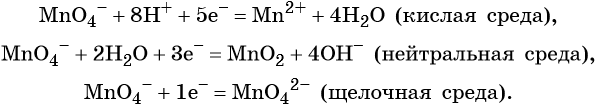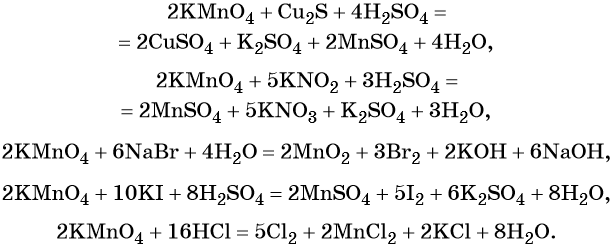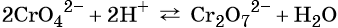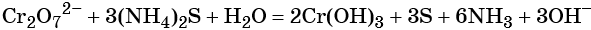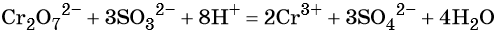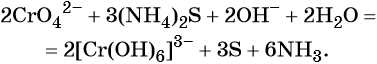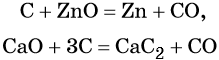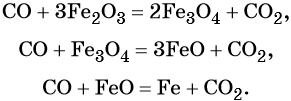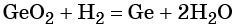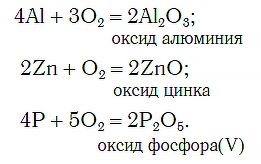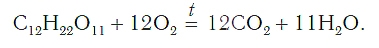Урок №67-68. Окислительно-восстановительные реакции
ОКИСЛИТЕЛЬ-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ (ОВР)
ОВР – это реакции, в ходе которых атомы изменяют свои степени окисления.
Основные положения теории ОВ реакций
1. Окислением называется процесс отдачи электронов атомом, молекулой или ионом.
При окислении степень окисления повышается.
2. Восстановлением называется процесс присоединения электронов атомом, молекулой или ионом.
При восстановлении степень окисления понижается.
F +9 ) 2 ) 7
F 0 + 1ē → F -1 в осстанавливается (окислитель)
В зял – В осстановился – Понизил СО
Na +11 ) 2 ) 8 ) 1
Na 0 – 1ē → Na +1 о кисляется (восстановитель)
О тдал – О кислился – Повысил СО
Задания для закрепления
№3. Расставьте коэффициенты в УХР методом электронного баланса, укажите процессы окисления (восстановления), окислитель (восстановитель); запишите реакции в полном и ионном виде:
А) Zn + HCl = H 2 + ZnCl 2
Б) Fe + CuSO 4 = FeSO 4 + Cu
№4. Даны схемы уравнений реакций:
СuS + HNO 3 (разб.) = Cu(NO 3 ) 2 + S + NO + H 2 O
K + H 2 O = KOH + H 2
Расставьте коэффициенты в реакциях используя метод электронного баланса.
№5. Расставьте коэффициенты в ОВР методом электронного баланса, укажите окислитель и восстановитель
MnO 2 + HCl = MnCl 2 + Cl 2 + H 2 O
H 2 S + KMnO 4 + H 2 SO 4 =S + MnSO 4 + K 2 SO 4 + H 2 O
Окислительно-восстановительные реакции. Окислитель и восстановитель
Окислительно-восстановительными называют реакции, которые сопровождаются изменением степеней окисления химических элементов, входящих в состав реагентов.
Окислением называют процесс отдачи электронов атомом, молекулой или ионом, который сопровождается повышением степени окисления.
Восстановлением называют процесс присоединения электронов атомом, молекулой или ионом, который сопровождается понижением степени окисления.
Окислителем называют реагент, который принимает электроны в ходе окислительно-восстановительной реакции. (Легко запомнить: окислитель — грабитель.)
Восстановителем называют реагент, который отдаёт электроны в ходе окислительно-восстановительной реакции.
Окислительно-восстановительные реакции делят на реакции межмолекулярного окисления-восстановления, реакции внутримолекулярного окисления-восстановления, реакции диспропорционирования и реакции конмутации.
Для составления окислительно-восстановительных реакций используют метод электронного баланса.
Составление уравнения окислительно-восстановительной реакции осуществляют в несколько стадий.
Пример 1. Реакция алюминия с серой. Записываем схему реакции и указываем изменение степеней окисления:
Атом серы присоединяет два электрона, изменяя свою степень окисления от 0 до –2. Он является окислителем. Атом алюминия отдаёт три электрона, изменяя свою степень окисления от 0 до +3. Он является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов:
Подставляем найденные коэффициенты в уравнение реакции и окончательно получаем:
Пример 2. Окисление фосфора хлором. Записываем схему реакции и указываем изменение степеней окисления:
Степень окисления хлора изменяется от 0 до –1, при этом молекула хлора присоединяет два электрона. Хлор является окислителем.
Атом фосфора отдаёт пять электронов, изменяя свою степень окисления от 0 до +5. Он является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов:
Электронное уравнение для хлора записывают именно так, поскольку окислителем является молекула хлора, состоящая из двух атомов, и каждый из этих атомов изменяет свою степень окисления от 0 до –1. Коэффициент 5 относится к молекуле хлора в левой части уравнения, а количество атомов хлора в правой части уравнения 5 × 2 = 10.
Подставляем найденные коэффициенты в уравнение реакции и окончательно получаем:
Пример 3. Восстановление оксида железа (II, III) алюминием. Записываем схему реакции и указываем изменение степеней окисления:
Степень окисления железа изменяется от +8/3 до 0, при этом три иона железа (поскольку в исходном оксиде их содержится именно три) присоединяют восемь электронов (3 × 8/3 = 8). Железо является окислителем.
Алюминий отдаёт три электрона, изменяя свою степень окисления от 0 до +3. Он является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединенных и отданных электронов:
Электронное уравнение для алюминия записывают именно так, поскольку в состав оксида алюминия входят два атома алюминия. Таким образом, в левой части уравнения основной коэффициент перед оксидом железа (II, III) будет равен 3, а перед алюминием 4 × 2 = 8.
Количество атомов железа в правой части уравнения реакции составит 3 × 3 = 9. Количество молекул оксида алюминия будет равно 8/2 = 4. Окончательно получаем:
Проверяем баланс по кислороду. В левой части уравнения 3 × 4 = 12. В правой части уравнения 4 × 3 = 12. Таким образом, число атомов каждого элемента в отдельности в левой и в правой части химического уравнения равны между собой, и реакция уравнена правильно.
Этот пример наглядно показывает, что дробная степень окисления хотя и не имеет физического смысла, но позволяет правильно уравнять окислительно-восстановительную реакцию.
Очень часто окислительно-восстановительные реакции проходят в растворах в нейтральной, кислой или щелочной среде. В этом случае химические элементы, входящие в состав вещества, образующего среду реакции, свою степень окисления не меняют.
Пример 4. Окисление йодида натрия перманганатом калия в среде серной кислоты. Записываем схему реакции, указываем степени окисления элементов, участвующих в процессах окисления и восстановления:
Атом марганца принимает пять электронов, изменяя свою степень окисления от +7 до +2. Перманганат калия является окислителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов введением множителей:
Найденные коэффициенты подставим в уравнение реакции перед соответствующими формулами веществ в левой и правой частях.
Серная кислота является средой реакции. Ни один из элементов, входящих в состав этого соединения, свою степень окисления не меняет, но сульфат-анион связывает выделяющиеся в результате реакции катионы калия, натрия и марганца. Подсчитаем число сульфат-ионов в правой части. Оно равно 2 + 1 + 5 = 8. Следовательно, перед серной кислотой следует поставить коэффициент 8. Число атомов водорода в левой части уравнения равно 8 × 2 = 16. Отсюда вычисляем коэффициент для воды: 16/2 = 8.
Таким образом, уравнение реакции будет иметь вид:
Правильность баланса проверяем по кислороду. В левой части его 2 × 4 = 8 (перманганат калия); в правой — 8 × 1 = 8 (вода). Следовательно, уравнение составлено правильно.
Пример 5. Окисление сульфида калия манганатом калия в водной среде. Записываем схему реакции, указываем степени окисления элементов, участвующих в процессах окисления и восстановления:
Ион марганца принимает два электрона, изменяя свою степень окисления от +6 до +4. Манганат калия является окислителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов введением множителей:
Основные коэффициенты в уравнении реакции равны единице:
Вода является средой реакции. Ни один из элементов, входящих в состав этого соединения, свою степень окисления не меняет.
Гидроксид-ионы связывают выделяющиеся в результате реакции катионы калия. Таких катионов четыре (2 × 2), число атомов водорода также 4 (4 × 1), поэтому перед молекулой воды ставим коэффициент два (4/2 = 2):
Пример 6. Окисление аммиака хлоратом калия в щелочной среде. Записываем схему реакции, указываем степени окисления элементов, участвующих в процессах окисления и восстановления:
Хлор принимает шесть электронов, изменяя свою степень окисления от +5 до –1. Хлорат калия является окислителем.
Азот отдаёт восемь электронов, изменяя свою степень окисления от –3 до +5. Аммиак является восстановителем.
Составляем уравнение электронного баланса, уравниваем число присоединённых и отданных электронов введением множителей, сокращаем кратные коэффициенты:
Проставляем найденные основные коэффициенты в уравнение реакции:
Гидроксид калия является средой реакции. Ни один из элементов, входящих в состав этого соединения, свою степень окисления не меняет.
Катионы калия связывают выделяющиеся в результате реакции нитрат-ионы. Таких анионов три. Следовательно, перед гидроксидом калия ставим коэффициент три:
Число атомов водорода в левой части уравнения равно девяти в аммиаке (3 × 3) = 9 и трём в гидроксиде калия (3 × 1), а их общее число 9 + 3 = 12. Следовательно, перед водой ставим коэффициент (12/2) = 6. Окончательно уравнение реакции будет иметь вид:
Убеждаемся ещё раз в правильности расстановки коэффициентов, сравнивая число атомов кислорода в левой и правой его частях. Оно равно 15.
Довольно часто одно и то же вещество одновременно является окислителем и создаёт среду реакции. Такие реакции характерны для концентрированной серной кислоты и азотной кислоты в любой концентрации. Кроме того, в подобные реакции, но в качестве восстановителя, вступают галогенводородные кислоты с сильными окислителями.
Пример 7. Окисление магния разбавленной азотной кислотой. Записываем схему реакции и указываем изменение степеней окисления:
Степень окисления азота изменяется от +5 до +1, при этом два атома азота присоединяют восемь электронов. Азотная кислота является окислителем.
Магний отдаёт два электрона, изменяя свою степень окисления от 0 до +2. Он является восстановителем.
Составляем уравнение электронного баланса и уравниваем число присоединённых и отданных электронов:
Подставляем найденные коэффициенты перед окислителем и восстановителем в левой части уравнения реакции и перед продуктами окисления и восстановления в правой части уравнения реакции:
При этом в правой части уравнения реакции имеется 4 × 2 = 8 нитрат-ионов, не изменивших свою степень окисления. Очевидно, что для этого в правую часть уравнения реакции следует добавить ещё 8 молекул HNO3. Тогда общее количество молекул азотной кислоты в правой части уравнения составит 2 + 8 = 10.
В этих молекулах содержатся 10 × 1 = 10 атомов водорода. Такое же количество атомов водорода должно быть и в правой части уравнения. Следовательно, перед молекулой воды следует подставить коэффициент 10/2 = 5, и уравнение окончательно будет иметь вид:
Окончательно проверяем правильность баланса, подсчитывая число атомов кислорода в левой и правой частях уравнения. В левой части 10 × 3 = 30. В правой части (2 × 3) × 4 = 24 в нитрате магния, 1 в оксиде азота (I) и 5 × 1 = 5 в молекуле воды. Итого 24 + 1 + 5 = 30. Таким образом, реакция полностью уравнена.
Пример 8. Взаимодействие соляной кислоты с оксидом марганца (IV). Записываем схему реакции и указываем изменение степеней окисления:
Степень окисления марганца изменяется от +4 до +2, при этом марганец присоединяет два электрона. Оксид марганца (IV) является окислителем.
Составляем электронное уравнение и уравниваем число присоединённых и отданных электронов, сокращаем кратные коэффициенты:
При этом коэффициент 1 изначально относится к двум хлорид-ионам и к одной молекуле Cl2. Подставляем найденные коэффициенты перед окислителем и восстановителем в левой части уравнения реакции и перед продуктами окисления и восстановления в правой части уравнения реакции:
При этом в правой части уравнения реакции имеется 1 × 2 = 2 хлорид-иона, не изменивших свою степень окисления. Эти хлорид-ионы в окислительно-восстановительной реакции не участвовали. Очевидно, что для этого в правую часть уравнения реакции следует добавить 2 молекулы HCl. Тогда общее количество молекул HCl в правой части уравнения составит 2 + 2 = 4. В этих молекулах будет содержаться 4 × 1 = 4 атома водорода. Такое же количество атомов водорода должно быть и в правой части уравнения. Тогда перед молекулой воды следует подставить коэффициент 4/2 = 2, и уравнение в окончательном виде будет иметь вид:
Проверяем правильность баланса, подсчитывая число атомов кислорода в левой и правой частях уравнения. В левой части оно составляет 1 × 2 = 2 в оксиде марганца (IV), а в правой части 2 × 1 = 2 в молекуле воды. Таким образом, реакция полностью уравнена.
В качестве окислителя могут выступать нейтральные атомы и молекулы, положительно заряженные ионы металлов, сложные ионы и молекулы, содержащие атомы металлов и неметаллов в состоянии положительной степени окисления и др.
Ниже приведены сведения о некоторых наиболее распространенных окислителях, имеющих важное практическое значение.
Кислород. Сильный окислитель, окислительная способность значительно возрастает при нагревании. Кислород взаимодействует непосредственно с большинством простых веществ, кроме галогенов, благородных металлов Ag, Au, Pt и благородных газов, с образованием оксидов:
Взаимодействие натрия с кислородом приводит к пероксиду натрия:
Более активные щелочные металлы (K, Rb, Cs) при взаимодействии с кислородом дают надпероксиды типа ЭО2:
В своих соединениях кислород, как правило, проявляет степень окисления –2. Применяется кислород в химической промышленности, в различных производственных процессах в металлургической промышленности, для получения высоких температур. С участием кислорода идут многочисленные чрезвычайно важные жизненные процессы: дыхание, окисление аминокислот, жиров, углеводов. Только немногие живые организмы, называемые анаэробными, могут обходиться без кислорода.
Реакции, иллюстрирующие окислительные свойства кислорода при его взаимодействии с различными неорганическими веществами, приведены в уроке 14.
Озон. Обладает ещё большей по сравнению с кислородом окислительной способностью. Озон окисляет все металлы, за исключением золота, платины и некоторых других, при этом, как правило, образуются соответствующие высшие оксиды элементов, реже — пероксиды и озониды, например:
Озон окисляет оксиды элементов с промежуточной степенью окисления в высшие оксиды.
Перманганат калия способен окислять сульфиды в сульфаты, нитриты в нитраты, бромиды и йодиды — до брома и йода, соляную кислоту до хлора и т. д.:
Хромат и бихромат калия. Эти соединения широко применяют в качестве окислителей в неорганических и органических синтезах. Взаимные переходы хромат- и бихромат-ионов очень легко протекают в растворах, что можно описать следующим уравнением обратимой реакции:
Соединения хрома (VI) — сильные окислители. В окислительно-восстановительных процессах они переходят в производные Cr (III). В нейтральной среде образуется гидроксид хрома (III), например:
В кислой среде образуются ионы Cr 3+ :
В щелочной — производные анионного комплекса [Cr(OH)6] 3– :
В качестве восстановителя могут выступать нейтральные атомы, отрицательно заряженные ионы неметаллов, положительно заряженные ионы металлов в низшей степени окисления, сложные ионы и молекулы, содержащие атомы в промежуточной степени окисления, электрический ток на катоде и др.
Ниже приведены сведения о некоторых наиболее распространённых восстановителях, имеющих важное практическое значение.
Углерод. Углерод широко применяют в качестве восстановителя в неорганических синтезах. При этом в качестве продуктов окисления может образовываться углекислый газ, или оксид углерода (II). При восстановлении оксидов металлов могут образовываться свободные металлы, реже — карбиды металлов.
Восстановительные свойства углерод проявляет также в реакции получения водяного газа:
Полученную смесь водорода и оксида углерода (II) широко применяют для синтеза органических соединений.
Оксид углерода (II). Широко применяют в металлургии при восстановлении металлов из их оксидов, например:
Водород. Широко применяют в качестве восстановителя в неорганических синтезах (водородотермия) для получения чистого вольфрама, молибдена, галлия, германия и т. д.:
Тренировочные задания
Используя метод электронного баланса, расставьте коэффициенты, определите окислитель и восстановитель в уравнении реакции, схема которой:
1. Al + H2O + KNO3 + KOH → K[Al(OH)4] + NH3↑.
Урок 20. Окислительные процессы
В уроке 20 «Окислительные процессы» из курса «Химия для чайников» узнаем о процессах с участием кислорода; дадим определения топливу и окислению, а также выясним как эти самые процессы влияют на атмосферу.
Вы хорошо знаете, что человеку и животным необходим воздух (а следовательно, и кислород) для дыхания. Какую же роль играет кислород в организме человека и животных?
Процессы с участием кислорода
В живом организме протекают процессы, в которых сложные вещества пищи — белки, жиры и углеводы — вступают в химические реакции с кислородом. При этом выделяется необходимая для жизнедеятельности энергия. Кислород, необходимый для протекания этих реакций, поступает в организм благодаря процессу дыхания.
Еще одной разновидностью взаимодействия кислорода и сложных веществ является процесс гниения. Вы, наверное, видели, как над кучами гниющей лист вы или каких-либо отходов, особенно по утрам, поднимается пар (рис. 86). Это сложные вещества вступают в реакцию с кислородом воздуха. В результате этой реакции образуется вода и выделяется теплота, благодаря которой вода превращается в пар.
Можно сказать, что гниение и дыхание — это «медленное горение». Эти процессы широко распространены в природе.
Присоединение кислорода как окислительный процесс
Общим для всех рассмотренных процессов с участием кислорода O2 является то, что продуктами реакции в них являются сложные вещества, которые образуются путем присоединения атомов кислорода к атомам других элементов. Например:
Такие реакции называют реакциями окисления.
Окисление — химическая реакция, в результате которой происходит присоединение атомов кислорода к атомам других элементов.
При сгорании сложного вещества сахарозы (это обычный сахар) C12H22O11 в кислороде также протекает окисление. В этом процессе происходит соединение атомов кислорода с атомами углерода и водорода. При этом образуются углекислый газ и вода:
Окисление может протекать с выделением большого количества теплоты и света — тогда это реакция горения, а также в виде «медленного горения» — дыхания и гниения. Во всех этих случаях происходит присоединение атомов кислорода к атомам других химических элементов, которые входили в состав сложного вещества. В результате процессов горения, гниения и дыхания образуются новые сложные вещества (обычно оксиды).
Понятие о топливе
Процессы горения издавна используются для удовлетворения нужд человека в энергии и тепле.
Топливо — это вещество, которое горит с выделением тепловой энергии.
По агрегатному состоянию топливо бывает твердое, жидкое и газообразное.
Запасы топлива могут быть восполнимыми (древесина, древесный уголь) и невосполнимыми (уголь, торф, нефть).
Каменные и бурые угли. Уголь (рис. 87) является древнейшим источником энергии, с которым знакомо человечество. Он представляет собой полезное ископаемое, которое образовалось из растительного материала на протяжении многих миллионов лет. Например, древесина без доступа воздуха превращается в каменный уголь. Основная масса угля состоит из углерода и органических соединений.
Торф. В Беларуси важное значение для бытового отопления и работы небольших предприятий имеет торф (рис. 88). Это топливо, которое образуется без доступа воздуха на низинных болотах из мха сфагнума и другой растительности. В последнее время его спрессовывают с угольной крошкой и получают торфоугольные брикеты, которые также используются как топливо.

Древесина. Как топливо древесина используется преимущественно на бытовом уровне. Основная масса ее применяется как строительный материал, а также идет на химическую переработку.
Нефть. Источник самых разнообразных жидких видов топлива на Земле — нефть (рис. 89). При ее переработке получают такие важные виды горючего, как бензин, керосин, лигроин, мазут. Эти виды топлива используются в автомобилях и тракторах, реактивных авиационных двигателях, а также на тепловых электростанциях и в системах теплообеспечения жилья и предприятий.
Природный газ. Примерно на 90 % состоит из метана CH4. Использовать его в качестве топлива стали только в XX в. Сегодня наша жизнь немыслима без газопроводов (рис. 90), доставляющих «голубое топливо» в наши квартиры, на ТЭС, ТЭЦ, промышленные предприятия.
Охрана атмосферы
В результате деятельности человека происходит загрязнение атмосферы самыми различными веществами, многие из которых ядовиты для человека, животных и растений. Изменение состава атмосферы приводит к ослаблению здоровья населения, снижению продолжительности жизни, распространению болезней. Это особенно заметно в больших городах, где атмосфера загрязняется газовыми выбросами промышленных предприятий и автомобильного транспорта.
В состав почти всех известных традиционных видов топлива входят вещества, при сгорании которых образуются не только СО2 и Н2О. При неполном сгорании топлива может образовываться весьма ядовитый угарный газ (СО). Также очень неблагоприятны для человека продукты сгорания соединений, содержащих атомы серы и азота, которыми являются оксиды серы (SO2) и азота (NO, NO2).
Для улучшения качества бензина в него добавляют соединения свинца. При сгорании такого бензина в окружающую среду выбрасывается большое количество ядовитых для человека веществ, содержащих свинец.
На сжигание различных видов топлива потребляется огромное количество кислорода. Так, в течение 1 ч. полета реактивный самолет (рис. 91) потребляет количество кислорода, вырабатываемое лесом площадью 1 га. за месяц.
Смог (рис. 92) — это туман, смешанный с пылью и сажей и содержащий продукты взаимодействия оксидов серы и азота с водой.
Кислотные дожди. Дождевая вода более кислая, чем обычная, так как в ней содержатся вещества, называемые кислотами. Они образуются при взаимодействии оксидов серы и азота с парами воды.
Парниковый эффект (рис. 93) возникает в результате повышения температуры воздуха за счет накопления в атмосфере некоторых газов, называемых парниковыми. Основным парниковым газом является углекислый газ. В результате парникового эффекта повышается температура воздуха в нижних слоях атмосферы, происходит изменение климата, возможны таяния ледников, наводнения.
Поскольку атмосфера у всех народов Земли общая, разные государства предпринимают совместные меры по ее защите от вредных выбросов. Для этого на заводах устанавливаются очистительные установки, совершенствуются системы очистки выхлопных газов автотранспорта, разрабатываются новые экологически чистые производства и виды транспорта.
Уменьшить влияние химических веществ на природу, здоровье людей возможно, только сделав самые тщательные исследования источников и состава ядовитых соединений. Химия как наука позволяет человеку найти пути решения указанных выше проблем охраны атмосферы.
Краткие выводы урока:
Надеюсь урок 20 «Окислительные процессы» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.