Склерозирующий лихен
Что такое «склерозирующий лихен» (СЛ)?
СЛ — это хроническое воспалительное заболевание кожи как правило половых органов у мужчин и женщин, причины которого еще далеко не полностью изучены и известны. Однако на сегодняшний день ясно, что если СЛ не лечить, то это заболевание приводит к рубцовым изменениям половых органов, которые могу вызвать серьезные проблемы. У мужчин может, в частности, развиться сужение крайней плоти (фимоз) и затруднения при открытии головки полового члена. В более тяжелых случаях возможно образование сужения (стриктуры) наружного отверстия уретры и ладьевидной ямки (самая ближайшая к наружному отверстию часть мочеиспускательного канала), что приводит к расстройствам мочеиспускания и нарушению оттока мочи. Подобные изменения могут стать причиной снижения качества жизни, а иногда и привести к таким осложнениям как инфекция мочевых путей (пиелонефрит, цистит), расширение полостной системы почек(гидронефроз), мочекаменная болезнь. Кроме этого, тяжелые формы СЛ считаются предрасполагающими состояниями для развития рака полового члена.
Какие синонимы заболевания может употребить Ваш врач, имея в виду СЛ?
Несколько синонимов может использоваться для описания СЛ. Как правило названия диагноза СЛ могут различаться в зависимости от специальности врача и места расположения поражения кожи. Например, гинекологи часто используют термин «крауроз вульвы», дерматологи — «склероатрофический лихен», урологи — «облитерирующий ксеротический баланит». В 1976 году Международное общество по изучению заболеваний вульвы и влагалища (ISSVD) рекомендовало при описании данного заболевания использовать термин «склеротический лихен». К данной рекомендации гинекологов в 1995 году присоединилась Американская Академия Дерматологии (AAD).
На сегодняшний день, к сожалению, ни одна из профессиональных урологических ассоциаций не пришла к единству в использовании термина «склерозирующий лихен» (лат.: lichen sclerosus). В России в большинстве учебных заведений СЛ вообще не преподается обучающимся урологам как самостоятельная форма воспаления головки и крайней плоти полового члена. В связи с этим многие урологи просто не знают ни симптомов этого заболевания, ни методов его лечения. Очень часто нам приходится сталкиваться с ситуациями, когда больных СЛ лечили антибиотиками в виде системной и местной терапии от «банального баланопостита», «грибкового баланопостита», «герпеса», «хламидиоза», «приобретенного фимоза» и т.д. Однако, поскольку антибиотики и противогрибковые препараты при СЛ зачастую не эффективны, а хирургическое устранение фимоза (циркумцизия или обрезание крайней плоти) не сопровождалась дальнейшим лечением, пациенты так и не получали адекватной помощи.
Каковы причины возникновения склерозирующиго лихена?
Как уже говорилось выше, точная причина возникновения СЛ пока не известна. Однако изучен ряд факторов, которые могут принимать участие в развитии заболевания:
Какие проявления СЛ можно наблюдать у мужчин?
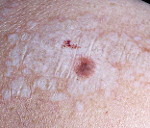
У мужчин СЛ как правило начинается с поражения кожи полового члена. Ранние проявления СЛ — появление на коже крайней плоти и головки члена белесоватых пятен и участков атрофии кожи, а также склеротических бляшек пятнистой окраски (рис. 1). Характерное проявление начальной стадии СЛ — белесоватое склеротическое кольцо.

Рис. 1. Склеротический лихен полового члена на ранней стадии I-II стадии. Поражение кожи крайней плоти в виде белесоватого кольца и головки полового члена в виде белесоватых пятен.
В дальнейшем развитие склеротической (рубцовой) ткани приводит к уплотнению кожи крайней плоти, что затрудняет открытие головки члена, способствует присоединению инфекции и развитию бактериального воспаления головки члена (баланиту). С развитием заболевания, головка полового члена перестает открываться и формируется рубцовый фимоз (рис. 2).

Рис. 2. Склеротический лихен полового члена средней степени тяжести III стадии. Рубцовый фимоз, хроническое воспаление головки и крайней плоти полового члена.
По причине снижения эластичности на наружном крае кожи крайней плоти могут появляться надрывы. На рисунке 3 показан умеренно выраженный СЛ. Однако при половом акте пациента постоянно беспокоили разрывы кожи крайней плоти, что и послужило поводом для обращения к врачу.

Рис. 3. Умеренно выраженный СЛ II-III стадии с рубцовым фимозом. Видна заживающая ранка кожи крайней плоти от разрыва, который произошел при половом акте.
У обрезанных мужчин СЛ может начинаться на половом члене в зоне кожного рубца, оставшегося после операции по обрезанию крайней плоти. Вовлечение в процесс рубцевания наружного отверстия и начальных отделов мочеиспускательного канала приводит к появлению затрудненного мочеиспускания, проявляющегося истончением струи мочи и необходимостью натуживаться, чтобы начать мочеиспускание. В нашей клинической практике мы столкнулись с пациентом 47 лет, у которого сужение крайней плоти и наружного отверстия уретры в результате СЛ полового члена привело к столь значимому нарушению оттока мочи, что у него развилась хроническая инфекция мочевых путей и коралловидный камень правой почки, потребовавший многоэтапного лечения. У этого же пациента на головке полового члена сформировалась гранулема по внешнему виду напоминавшая рак полового члена (рис. 4). К счастью этот грозный диагноз при гистологическом исследовании не подтвердился.

Рис. 4. Тяжелая степень СЛ полового члена IV стадии. Выраженное сужение наружного отверстия мочеиспускательного канала, подозрительная на рак гранулема полового члена.
Какие методы лечения Склерозирующего лихена существуют?
Объем лечения зависит от степени распространения процесса СЛ.
Важно отметить, что циркумцизия (круговое иссечение крайней плоти при СЛ имеет свои особенности. Основной задачей циркумцизии при СЛ является полное иссечение пораженных тканей. При этом не следует убирать слишком много крайней плоти, т.к. она может понадобиться в дальнейшем для выполнения пластических операций реконструкции сужений (стриктур) уретры (прежде всего ладьевидной ямки), которые могут быть вызваны СЛ. На последующих рисунках показаны этапы лечения СЛ полового члена I-II стадии (внешний вид до операции показана на рис. 3).

Рис. 5. Циркумцизия при СЛ с использованием техники двойного разреза. Разрез кожи размечен таким образом, чтобы иссечь пораженную часть крайней плоти полового члена, которая отчетливо видна.

Рис. 6. Состояние полового члена после операции. Пораженная кожа иссечена, однако ее достаточно для возможных последующих реконструктивных операций.
В чем может заключаться профилактика СЛ половых органов?
К сожалению, каких-либо эффективных профилактических мер, которые бы могли не допустить заболевание СЛ, не существует. Однако если Вы заметили у себя первые признаки СЛ, необходимо безотлагательно обратиться к врачу-урологу (мужчины) или гинекологу (женщины). Ведь как уже говорилось выше, если не лечить СЛ своевременно, могут наступить достаточно серьезные последствия. Раннее удаление пораженных тканей кожи половых органов с последующим наблюдением и, при необходимости, лечением с помощью мазей может остановить болезнь и не позволить ей вызвать столь грозные осложнения. Прежде чем обратиться к врачу, важно удостовериться (изучив его репутацию по отзывам пациентов), что он достаточно хорошо владеет диагностикой и лечением СЛ и других заболеваний половых органов. Мужчинам следует помнить, что лечение далеко зашедших форм СЛ иногда требует выполнения сложных реконструктивных операций восстановления проходимости мочеиспускательного канала. В связи с этим врач уролог, которому Вы бы доверили свое лечение, должен владеть данными операциями в совершенстве.
В клинике «Андрос» осуществляется лечение всех форм склеротического лихена половых органов. При необходимости могут быть выполнены все операции, необходимые для избавления от этого недуга, от циркумцизии до сложных реконструктивных операций на мочеиспускательном канале. При наличии поражений, подозрительных на рак полового члена, выполняется биопсия и тщательное гистологическое исследование.
При подготовке публикации использованы материалы: Lazzieri M, Barbagli G, Palmintieri E, Turini D. Lichen sclerosus of the male genitalia. Contemporary Urolology 2001; 3.
КОНТАКТЫ
197136, г. Санкт-Петербург
ул. Ленина, д. 34
Склероатрофический лишай
Склероатрофический лишай – дерматологическое заболевание неясной этиологии, при котором наблюдается атрофия различных участков кожи, в основном в области половых органов, реже других регионов тела. Симптомом этого состояния является образование светлых, почти белых бляшек и папул вокруг гениталий, изредка на шее и около подмышечных впадин, которые со временем трансформируются в атрофические очаги. Диагностика склероатрофического лишая осуществляется на основании результатов дерматологического осмотра больного, в спорных случаях может производиться биопсия кожных покровов в области поражения с последующим гистологическим исследованием. Этиотропное лечение заболевания не разработано, назначают общеукрепляющие средства, витаминотерапию и лекарства для улучшения микроциркуляции. Имеются указания на положительный эффект от использования противомалярийных средств.
Общие сведения
Склероатрофический лишай (болезнь белых пятен, каплевидная склеродермия, крауроз вульвы/полового члена) – атрофическое заболевание кожи неопределенного генеза, которое преимущественно поражает зону гениталий, но может располагаться и на иных участках кожных покровов. Это состояние было впервые описано еще в 1889 году французским дерматологом Франсуа Аллопо, принявшем заболевание за разновидность обычного плоского лишая. Лишь дальнейшие исследования позволили определить, что патология, описанная Аллопо, разделяется на два типа – первичный склероатрофический лишай и последствия красного плоского лихена (стадия атрофии). Это дерматологическая заболевание в несколько раз чаще встречается у женщин, особенно экстрагенитальные формы – последние практически никогда не наблюдаются у мужчин. Наблюдения по поводу возрастного распределения несколько разнятся – по одним данным, склероатрофический лишай в основном поражает лиц старшего возраста и крайне редко возникает у девочек в подростковый период. Согласно мнению иных исследователей, нередки случаи развития этого состояния у молодых женщин – такие различия в описании многих специалистов объясняют путаницей, при которой за болезнь белых пятен принимают застарелые формы красного плоского лишая.
Причины склероатрофического лишая
Этиология и патогенез склероатрофического лишая в данный момент изучены недостаточно, имеется лишь несколько гипотез по поводу развития этого дерматологического заболевания. Наибольшим признанием пользуется патогенетическая теория – описаны как наследственные случаи данного состояния, так и их схожее развитие у однояйцовых близнецов. Однако при этом ни дефектные гены, ни другие молекулярные механизмы возникновения склероатрофического лишая не изучены. Другая популярная теория указывает на аутоиммунные факторы развития этой патологии, поскольку ее проявления схожи с другими поражениями кожи подобного типа (склеродермией, некоторыми формами псориаза). Но и эта версия не объясняет все проявления склероатрофического лишая, кроме того, заболевание очень слабо реагирует на лечение иммуносупрессивными средствами.
Имеются указания на роль инфекционных факторов, например, боррелиоза (болезни Лайма). После перенесенной инфекции такого типа у ряда лиц возникают типичные проявления склероатрофического лишая. Не исключено влияние и других вирусных или бактериальных инфекций, также эта теория некоторыми дерматологами сочетается с аутоиммунной по причине возможной перекрестной реакции на антигены возбудителей и собственных тканей человека. Практически доказано, что предрасполагающую роль в развитии склероатрофического лишая играют гормональный дисбаланс, поражения эндокринной системы, частые психоэмоциональные стрессы. Изучение этого заболевания, попытки объяснения причин его возникновения и использования этих данных в лечении патологии продолжаются до сих пор.
Симптомы склероатрофического лишая
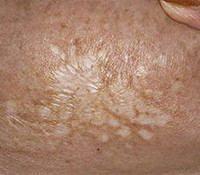
Большинство случаев склероатрофического лишая регистрируется у женщин в возрасте 35-50 лет, иногда наблюдается развитие заболевания у молодых девушек и даже подростков. Высыпания могут локализоваться на шее, груди, около подмышечных впадин, на лобке, бедрах и в области половых органов – при этом так называемые экстрагенитальные формы болезни белых пятен (наличие высыпаний на теле при отсутствии их на вульве и близлежащих участках) составляют только 20% от всех случаев. Наиболее часто склероатрофический лишай проявляется именно поражением генитальной области и собственно вульвы. Для начала заболевания характерно появление на поверхности кожных покровов папул белого цвета, которые достаточно быстро трансформируются в светлые или розовые бляшки. Поверхность бляшек несколько приподнята над здоровой кожей, шелушится, из субъективных симптомов отмечается выраженный зуд. При дальнейшем развитии склероатрофического лишая на месте бляшек образуются гипопигментированные атрофические участки кожи, поверхность которых напоминает папиросную бумагу.
Мужчины страдают от этой патологии в несколько раз реже, при этом у них практически всегда наблюдается поражение кожных покровов в области половых органов (в 90% случаев поражается крайняя плоть и поверхность головки полового члена). В остальном развитие кожных проявлений склероатрофического лишая не имеет особенностей, отмечается появление бляшек или папул с дальнейшей атрофией кожи и появлением белых пятен. Поражение крайней плоти может приводить к развитию рубцового фимоза. Как у мужчин, так и у женщин генитальные формы склероатрофического лишая могут осложняться вторичной инфекцией бактериального или вирусного генеза. Также эта форма заболевания опасна тем, что является предраковым состоянием – по статистике, примерно в 3-5% случаев болезнь белых пятен перерождается в плоскоклеточный рак кожи или половых органов.
Диагностика склероатрофического лишая
Выявление склероатрофического лишая в дерматологии не представляет особой сложности из-за выраженных проявлений заболевания – белых атрофических участков кожи, локализующихся вокруг половых органов и на вульве. При осмотре могут обнаруживаться относительно свежие очаги патологии в виде светло-розовых папул или бляшек. Однако дифференциальная диагностика склероатрофического лишая несколько затруднена, поскольку схожими проявлениями обладают склеродермия, застарелые формы красного плоского лишая, некоторые разновидности псориаза. Главной особенностью патологии является преимущественная локализация высыпаний вокруг и на половых органах, поэтому при экстрагенитальных формах наиболее часто возникают диагностические ошибки.
Патогистологические изменения при склероатрофическом лишае неодинаковы на различных стадиях процесса. На начальных этапах выявляют выраженный отек дермы, умеренную лимфогистиоцитарную инфильтрацию, расширение кровеносных сосудов. Эпидермис утолщен, наблюдается нарушение процессов ороговения, роговые массы могут забивать волосяные фолликулы, протоки потовых и сальных желез. При дальнейшем развитии склероатрофического лишая определяется атрофия эпидермиса, гомогенность коллагеновых волокон дермы. На поздних этапах в некоторых случаях могут наблюдаться признаки метаплазии клеток и начальных проявлений плоскоклеточного рака.
Лечение склероатрофического лишая
Из-за неясности причин склероатрофического лишая этиотропного лечения этого дерматологического заболевания на сегодняшний день не существует. Применяют различные симптоматические методы терапии, а также препараты, относительная эффективность которых была доказана эмпирическими клиническими наблюдениями. Из наружных средств назначают иммуносупрессивные мази (на основе кортикостероидов или такролимуса), однако они могут уменьшить выраженность симптомов лишь на стадии развития бляшек и папул. Аналогично в лечении склероатрофического лишая используют и противомалярийные средства – их не назначают при развившейся атрофии кожи. Препараты, улучшающие местное кровоснабжение и процессы микроциркуляции (например, на основе витаминов), также позволяют значительно уменьшить выраженность симптомов. Некоторые специалисты указывают на необходимость лечения основного заболевания, которое могло быть провоцирующим для склероатрофического лишая – эндокринных нарушений, сахарного диабета и пр.
Иногда в терапии болезни белых пятен применяют хирургические методики. Операции могут производиться как по эстетическим показаниям (устранение чрезмерно больших участков атрофии и дальнейшая пластика), так и по медицинским. В тяжелых случаях склероатрофического лишая возникают спайки, приводящие к сращению малых половых губ, сужению мочеиспускательного канала, фимозу. Все эти осложнения могут быть устранены только хирургическим путем – пластикой вульвы и мочеиспускательного канала, обрезанием (циркумцизио) у мужчин. Кроме того, хирургическое лечение показано при трансформации склероатрофического лишая в плоскоклеточный рак кожи.
Прогноз и профилактика склероатрофического лишая
Большинство дерматологов склонны относить склероатрофический лишай к заболеваниям с относительно неблагоприятным прогнозом. Это связано с неопределенным генезом патологии, в результате чего, несмотря на все терапевтические мероприятия, у больных остаются атрофические участки кожи различного размера. Всегда имеется риск таких осложнений, как развитие спаек, сужение мочеиспускательного канала, вторичная инфекция, злокачественное перерождение. Больные склероатрофическим лишаем должны каждые 2-3 месяца посещать дерматолога или онколога с целью как можно более раннего выявления вышеперечисленных грозных осложнений.
Склероатрофический лихен аногенитальной локализации: клинико-морфологические, дифференциально-диагностические особенности и комплексный метод лечения
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Склероатрофический лихен (СЛ) представляет собой хронический аутоиммунный дерматоз, протекающий с очаговой атрофией кожи и поражением тканей аногенитальной области. Аногенитальная локализация СЛ встречается чаще у женщин, чем у мужчин, в соотношении 3:1.
Цель исследования: выявить частоту поражения аногенитальной зоны при ограниченной склеродермии (ОС), установить дифференциально-диагностические клинические критерии поражения аногенитальной области при ОС, усовершенствовать метод лечения.
Материал и методы: в клинике им. В.А. Рахманова за период с 2017 по 2019 г. было обследовано 104 больных с установленным диагнозом ОС. Из всех пациентов (n=104) отобраны 62 пациента с СЛ аногенитальной локализации, из них мужчины составили 17,7%, женщины — 82,3%. Основная группа больных с поражением половых органов встречалась в возрастной медиане от 41 до 50 лет, что составило 17 человек (27,4%) и от 61 до 70 лет, что составило 15 человек (24,2%). Нами был оптимизирован протокол комплексного метода лечения ОС с учетом СЛ аногенитальной локализации и предложен новый подход, а именно применены бовгиалуронидазы азоксимер в виде суппозиториев, крем эстриол, гель с бактериофагами Фагогин. Всем пациенткам с СЛ аногенитальной зоны проводилось лечение фракционным СО2-лазером. В качестве наружной терапии СЛ аногенитальной зоны у мужчин мы применяли бовгиалуронидазу азоксимер методом фонофореза.
Результаты исследования: впервые выявлены поражения аногенитальной зоны у 59,6% (n=62) больных, среди них количество женщин значительно превышает количество мужчин (82,9% и 17,1% соответственно). Выявлена связь аногенитального СЛ с этиологическими факторами заболевания, в 71% случаев это инфекции, передаваемые половым путем и воспалительные заболевания малого таза.
Заключение: выявленная частота встречаемости СЛ аногенитальной локализации в структуре ОС 59,6%. Оптимизирован протокол комплексного метода лечения ОС с учетом склероатрофических поражений аногенитальной локализации и доказана его высокая клиническая эффективность, достигающая 98%.
Ключевые слова: дерматология, ограниченная склеродермия, склероатрофический лихен, аногенитальная локализация, склероатрофический лихен вульвы, склероатрофический лихен полового члена, частота встречаемости, вирусные инфекции, инфекции передающиеся половым путем, лечение.
Для цитирования: Снарская Е.С., Семенчак Ю.А. Склероатрофический лихен аногенитальной локализации: клинико-морфологические, дифференциально-диагностические особенности и комплексный метод лечения. РМЖ. Медицинское обозрение. 2019;3(12):9-13.
Anogenital lichen sclerosus: clinicopathologic, differential diagnostic features and complex treatment method
E.S. Snarskaya, Yu.A. Semenchak
Sechenov University, Moscow
Background: lichen sclerosus (LS) is a chronic autoimmune dermatosis that occurs with focal skin atrophy and anogenital tissue lesions. Anogenital lichen sclerosus (ALS) occurs more often in women than in men, in a ratio of 3:1.
Aim: to reveal the frequency and to establish differential diagnostic clinical criteria of anogenital lesions in circumscribed scleroderma (CS), to improve the treatment method.
Patients and Methods: for the period from 2017 to 2019, 104 patients with an established CS diagnosis were examined in the V.A. Rakhmanov Department of Skin and Venereal Diseases. Of all (n=104), 62 patients with ALS lesions were selected, of which men — 17.7%, women — 82.3%. Patients with genital lesions were distributed in the median age: 41–50, which was 17 people (27.4%) and 61–70 years, which was 15 people (24.2%). We have optimized the protocol of the complex CS treatment method, taking into account the ALS lesions, and proposed a new approach, namely the use of Bovhyaluronidaze azoximer in the suppository form, Estriol cream, and Phagogin gel with bacteriophages. All patients with ALS lesions were treated with fractional CO2 laser. We used Bovhyaluronidaze azoximer by phonophoresis method as topical treatment of ALS lesions in men.
Results: for the first time, anogenital lesions were detected in 59.6% (n=62) of patients. Among them, the number of women significantly exceeded the number of men (82.9% and 17.1%, respectively). The association of ALS with disease causative factors was revealed. In 71% of cases, STDs and pelvic inflammatory diseases were revealed.
Conclusion: the ALS incidence in the CS structure was detected in 59.6%. The protocol of the complex CS treatment method was optimized, taking into account anogenital sclerosus lesions. Also, its high clinical efficiency, reaching 98%, was proved.
Keywords: dermatology, circumscribed scleroderma, lichen sclerosus, anogenital region, vulvar lichen sclerosus, penile lichen sclerosus, incidence, viral infections, sexually transmitted diseases, treatment.
For citation: Snarskaya E.S., Semenchak Yu.A. Anogenital lichen sclerosus: clinicopathologic, differential diagnostic features and complex treatment method. RMJ. Medical Review. 2019;12:9–13.
В статье представлены результаты исследования, посвященного анализу клинико-морфологических характеристик, дифференциально-диагностическим особенностям и комплексному методу лечения склероатрофического лихена аногенитальной локализации
Введение
Склероатрофический лихен (СЛ) представляет собой хронический аутоиммунный дерматоз, протекающий с очаговой атрофией кожи и поражением тканей аногенитальной области [1–3]. Согласно общеклинической классификации, разработанной S. Peterson, СЛ является одним из клинических вариантов бляшечной ограниченной склеродермии (ОС) [4].
Особенностью клинического течения СЛ являются поражения как кожных покровов, так и тканей аногенитальной области, которые могут быть изолированными или сочетанными [5]. Аногенитальная локализация СЛ встречается чаще у женщин, чем у мужчин, в соотношении 3:1 [6, 7], кроме того, дерматоз может развиться в любом возрасте, однако пик заболеваемости приходится на препубертатный возраст (9–11 лет) и на климактерический и/или постклимактерический период (45–55 лет). У мужчин заболевание развивается обычно после 40 лет [6–8].
Вопросы этиологии и патогенеза СЛ до конца не изучены, однако известно что в патогенезе заболевания важную роль играют: генетическая предрасположенность; угнетение активности гипофизарно-надпочечниковой системы; дисфункция щитовидной и половых желез; вакцинация; травмы; острые и хронические инфекции (иксодовый клещевой боррелиоз (Borrelia burgdorferi), скарлатина, дифтерия, рожа, инфекции передающиеся половым путем (ИППП)); вирус папилломы человека (ВПЧ); вирус простого герпеса (ВПГ); гепатит В и С и др., возможен также паранеопластический генез [9–14]. В последние десятилетия, развитие СЛ аногенитальной локализации связывают с участием эстрогенов и прогестерона и их взаимосвязи с нарушениями в реакции синтеза коллагена и компонентов соединительной ткани [13, 14]. Данные литературы сообщают, что свободная фракция тестостерона и андростендиона значительно понижена у больных с генитальным СЛ, отмечена также аномальная активность фермента 5α-редуктазы [14]. В ряде исследований роль лидирующего фактора отводится гипоэстрогении, т. к. после 30-летнего возраста неуклонно понижается активность стероидогенеза (на 1–3% в год) и к 50 годам он уменьшается почти на 20% [14, 15]. Развитие СЛ в препубертатном периоде в большинстве случаев связано с низким содержанием эстрогенов и эстрогенной насыщенностью органов-мишеней [15]. Однако при развитии СЛ у детей в редких случаях возможен регресс патологических очагов, т. к. с возрастом уровень эстрадиола повышается [15, 16]. Особая роль в патогенезе СЛ отводится патологическому аутоиммунному процессу, развивающемуся в стенках мелких сосудов (капиллярит) и межуточном веществе соединительной ткани, в связи с высоким уровнем антигенной «коллагеновой» стимуляции [15–17].
Уменьшение активности фермента гиалуронидазы, накопление мукополисахаридов и прогрессирующая фибриноидная дегенерация соединительнотканных элементов в сочетании со спазмом сосудов вследствие накопления серотонина приводят к отечно-индуративным изменениям [2, 10, 15]. Запуск целого каскада аутоиммунных, сосудистых и обменных нарушений приводит к усиленному синтезу коллагена (I, III, IV и VII типов) и других компонентов экстрацеллюлярного матрикса, облитерации мелких сосудов, что клинически проявляется прогрессирующим атрофическим процессом тканей [15–17].
В целом ряде случаев поражение половых органов при СЛ может развиваться почти бессимптомно, особенно в начале заболевания [15]. Основными жалобами, предъявляемыми больными при неуклонном прогрессировании процесса, являются болезненность, парестезии, ощущение покалывания и «ползающих мурашек», умеренный зуд, а затем уплотнение тканей в зоне половых органов, выпадение волос и появление трещин. В процессе прогрессирования заболевания, наряду с нарастающими субъективными ощущениями, у больных появляется целый ряд других качественных симптомов. К ним относятся уринарный синдром, включающий персистирующие инфекции мочевыводящих путей, цистоуретрит [16], гастроинтестинальный синдром, проявляющийся болью при дефекации, хроническими запорами [17], и вульвовагинальный синдром, включающий диспареунию и целый спектр дисфункциональных сексуальных расстройств [16, 17].
Типичная клиническая картина СЛ представляет собой множество мелких (диаметром от 3 до 5 мм), четко контурированных участков атрофии, которые имеют тенденцию к слиянию. Элементы высыпаний могут быть рассеянными или сгруппированными. Постепенно их количество и размер увеличиваются, они сливаются и формируют обширные поля истонченного эпидермиса и атрофии, приводя к частичной редукции ткани. Окраска пораженной кожи белесоватая, с перламутровым или ливидным оттенком. Кожу трудно собрать в складку, на ней отсутствуют волосы, апокриновые и потовые железы также отсутствуют [15–18]. Прогрессирование склероатрофических изменений аногенитальной области у мужчин при локализации на коже полового члена, области ануса приводит к истончению крайней плоти, сужению и стриктуре уретры. Нередко развивается парафимоз, фимоз [18, 19]. Серьезным осложнением СЛ полового члена является плоскоклеточная карцинома, составляющая до 50% случаев рака соответствующей локализации [19, 20]. У женщин прогрессирование склероатрофических изменений аногенитальной области приводит к потере структуры вульвы и ее редукции. Вульва легко травмируется, возникает диспареуния. Складки половых губ уплощаются и сглаживаются, клитор и малые половые губы определить практически не удается (как и линию Гарта), из-за выраженного склероза тканей вход во влагалище сужается, уменьшаются размеры его преддверия и наружного отверстия мочеиспускательного канала. СЛ вульвы с хроническим гиперкератозом и эрозиями может осложниться плоскоклеточной карциномой [19–21].
Все эти явления, помимо неприятных субъективных ощущений, причиняют больным значительные моральные страдания и существенно снижают качество жизни, т. к. являются серьезным косметическим дефектом.
Важно также отметить, что пациенты с СЛ аногенитальной локализации наблюдаются в клиниках акушерско-гинекологического профиля, где данное заболевание воспринимается лишь как изолированное поражение гениталий, а не как форма ОС, требующая комплексного обследования и системного подхода к лечению.
Цель исследования: выявить частоту поражения аногенитальной зоны при основных клинических вариантах ОС, установить дифференциально-диагностические клинические критерии поражения аногенитальной области при ОС, усовершенствовать метод лечения с учетом аногенитальной локализации и оценить клиническую эффективность разработанного метода лечения.
Материал и методы
В клинике кожных и венерических болезней им. В.А. Рахманова за период с 2017 по 2019 г. нами было обследовано 104 больных с установленным диагнозом ОС (бляшечная склеродермия, линейная склеродермия, СЛ, атрофодермия Пазини — Пьерини). Из них 86 женщин (82,7%) и 18 мужчин (10,5%). По возрасту больные распределились следующим образом: от 20 до 30 лет — 18 человек (17,3%), от 31 года до 40 лет — 18 (17,3%), от 41 года до 50 лет — 13 (12,5%), от 51 года до 60 лет — 26 (25%), от 61 года до 70 лет — 23 (22,1%), от 71 года и старше — 6 (5,8%).
При проведении клинико-морфологического фенотипирования всех пациентов (n=104) нами были отобраны 62 пациента со склероатрофическими поражениями аногенитальной локализации.
Методика лечения
Курс комплексной терапии включает: инъекции бензилпенициллина в дозе 500 000 ЕД 4 р./сут внутримышечно (в/м) в течение 10 дней (курсовая доза 20 млн ЕД); пентоксифиллин в дозе 100 мг по 1 таблетке 3 р./сут в течение 1 мес.; бовгиалуронидаза азоксимер в виде вагинальных (для женщин) или ректальных (для мужчин) суппозиториев в дозировке 3000 МЕ 1 раз в 2 дня до курсовой дозы 30 тыс. МЕ; эстриол (крем вагинальный) — 1 аппликация (соответствующая 0,5 мг эстриола) 1 р./сут в течение 4 нед., затем 1 аппликация 2 р./нед. в течение 2 мес.; гель с бактериофагами Фагогин по 5–7 мл 3 р./сут в течение 1 мес.
В качестве наружной терапии склероатрофических поражений аногенитальной зоны у мужчин мы применяли бовгиалуронидазу азоксимер методом фонофореза. Курс лечения составил 10–12 процедур с кратностью 1–2 р./нед.
Результаты исследования
Больные с клиническим вариантом в виде бляшечной склеродермии составили 78 человек (75%), линейной склеродермией — 1 человек (0,9%), атрофодермией Пазини — Пьерини — 2 человека (1,9%), СЛ — 23 человека (22,2%).
Склероатрофические поражения аногенитальной локализации наблюдались у 40 больных бляшечной склеродермией (64,5%), у 21 больного СЛ (33,8%), у 1 больного линейной склеродермией (1,7%).
СЛ аногенитальной локализации наблюдался чаще у женщин — 82,9% (51 больная), чем у мужчин — 17,1% (11 больных). Основная группа больных с поражением половых органов встречается в возрастной медиане от 41 до 50 и от 61 до 70 лет, что соответствует периоду пре- и постменопаузы. Половозрастные особенности больных СЛ даны в таблице 1.

При анализе клинических особенностей распространенности склероатрофических поражений кожного покрова и слизистой половых органов нами установлено, что в 32,3% случаев склероатрофический процесс локализовался только в аногенитальной зоне, а в 67,7% случаев процесс носил сочетанный характер.
Так, согласно нашим данным, в 32,3% случаев (n=20) изолированное поражение аногенитальной локализации наблюдалось при склероатрофическом варианте ОС. При анализе сочетанных поражений кожи и аногенитальной зоны в 46,7% случаев (n=29) нами выявлены сочетание двух форм ОС: бляшечной формы на коже и СЛ аногенитальной зоны. В 19,4% случаев (n=12) нами выявлены сочетанные поражения СЛ кожи и аногенитальной зоны. В 1,7% случаев (n=1) очаги по типу СЛ в аногенитальной зоне сочетались с очагами поражения по типу линейной склеродермии на коже туловища.
При проведении подробного анализа особенностей локализации склероатрофических поражений аногенитальной зоны у женщин (n=51) установлено, что поражение вульвы встречалось в 41 случае (80,4%), поражение клитора — в 36 (70,5%), поражение ткани промежности — в 38 (74,5%), поражение перианальной области в 24 (47%) (рис. 1, 2).

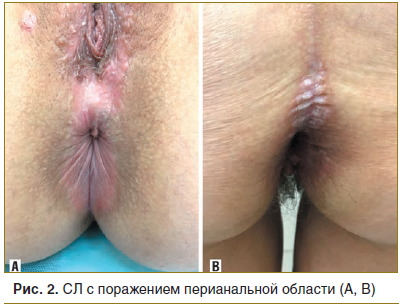
Анализ особенностей склероатрофических поражений у мужчин (n=11) показал склероатрофические поражения головки полового члена в 8 случаях (72,7%), поражение тканей уздечки — в 6 (54,5%), поражение кожи ствола полового члена — в 3 (27,3%), поражение перианальной области — в 4 случаях (36,4%) (рис. 3).

При анализе сопутствующей хронической патологии у исследуемых больных (n=62) нами установлено, что в 71% случаев (44 больных) выявлены ИППП и воспалительные заболевания малого таза, в 86,4% случаев (у 38 женщин) и в 17,1% случаев (у 6 мужчин). В 33,9% (21 больной) случаев обнаружены: ВПЧ высокого канцерогенного риска (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68) и ВПГ I и II типа — у 16 женщин (25,8%) и 5 мужчин (8,1%) (табл. 2).
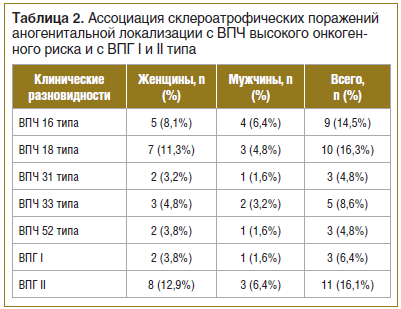
Склероатрофические поражения аногенитальной локализации сочетались с бактериальным вагинозом — в 27,4% случаев (17 больных), хламидиозом (Chlamydia trachomatis) — в 24,2% случаев (15 больных), трихомониазом (Trichomonas vaginalis) — в 17,7% случаев (11 больных), гонореей (Neisseria gonorrhoeae) — в 3,2% случаев (2 больных).
Склероатрофические поражения аногенитальной локализации сочетались с хронической персистирующей вирусной инфекцией: ВПГ II типа — в 16,1% случаев (11 больных), ВПГ I типа — в 6,4% случаев (3 больных) (см. табл. 2).
Также важно отметить, что наличие хронической персистирующей вирусной инфекции ВПЧ с высоким онкогенным потенциалом (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68) у пациентов с склероатрофическими поражениями половых органов вызывает значимый интерес ввиду высоких рисков развития злокачественной трансформации (см. табл. 2).
Нами проведен анализ сопутствующей хронической патологии у группы пациентов (n=62) с поражениями аногенитальной локализации. Большой интерес представляют заболевания органов малого таза, которые были выявлены в 40,3% случаев (n=25): миома матки — у 12 женщин, сальпингоофорит — у 5 женщин, сальпингит — у 3 женщин, цистит — у 2 женщин; простатит выявлен у 2 мужчин, аденома простаты — у 1.
Кроме того, была выявлена хроническая очаговая инфекция различной локализации в 27,4% случаев (n=17): у женщин — ринит у 5, хронический тонзиллит — у 3, хронический фарингит — у 3; у мужчин: ринит — у 3, хронический тонзиллит — у 2, хронический фарингит — у 1. Заболевания сердечно-сосудистой системы выявлены в 19,4% случаев (n=12): у женщин — артериальная гипертензия у 7, аритмия у 1; у мужчин — артериальная гипертензия у 3, сердечная недостаточность — у 1. Патология желудочно-кишечного тракта и гепатобилиарной системы встречалась в 3,2% случаев (n=2): у женщин — гастрит у 1, дискинезия желчного пузыря — у 1. Патология не выявлена в 9,7% случаев (n=6).
Эффективность курса проведенной терапии оценивали по положительной динамике кожного процесса: уменьшению плотности очагов, исчезновению или побледнению венчика гиперемии, отсутствию роста старых очагов и появления новых, уменьшению размеров старых очагов, уменьшению субъективных ощущений.
После первого курса комплексной терапии следовал перерыв в 1,5–2,0 мес., после которого проводился следующий курс комплексной терапии. При отсутствии и/или незначительности изменений после проведенного курса терапии больным назначался повторный курс (максимальное количество курсов не превышало 5).
Так, из 62 пациентов с ОС и поражением аногенитальной зоны основному количеству больных — 56,5% (35 человек) потребовалось 3 курса комплексной терапии, 16,1% (10 человек) — 4 курса, 11,3% (7 человек) — 2 курса, 6,4% (4 человека) — 1 курс и 8,1% (5 человек) — 5 курсов для полной стабилизации процесса.
На фоне проведенной комплексной терапии уменьшение плотности очагов наблюдалось у 48 (77,4%) больных, побледнение венчика гиперемии — у 28 (45,1%) больных. Отсутствие роста старых очагов и появления новых отмечено у 62 (100%) больных, уменьшение размеров очагов — у 39 (72,6%) больных (табл. 3).

Анализ динамики субъективных ощущений показал положительную тенденцию их уменьшения. Так, до лечения зуд аногенитальной области встречался в 77,4% случаев, после проведения комплексного лечения — в 24,2% случаев. Болезненные ощущения в очагах поражения до лечения наблюдались в 59,7% случаев, после лечения — в 17,7%. Парестезии до лечения наблюдались в 75,8% случаев, после лечения — лишь в 19,4% случаев. Чувство стягивания и сухость до лечения наблюдались в 80,6% случаев, после лечения — в 37,1%. Нарушения сна до лечения определялось в 77,4% случаев, после лечения — лишь в 8,1%. Нарушение сексуальной жизни до лечения встречалось в 51,6% случаев, после лечения — в 22,6% случаев (табл. 4).

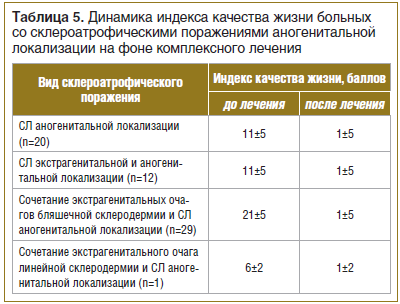
Всем больным (n=62) для оценки степени негативного влияния кожного заболевания на различные аспекты их жизни (отношения в семье с родственниками, с друзьями, коллегами по работе, занятия спортом, сексом, социальная активность и т. д.) был предложен опросник дерматологического индекса качества жизни (ДИКЖ) до и после лечения. После проведения комплексного курса лечения отмечено значительное повышение ДИКЖ у всех больных со склероатрофическими поражениями аногенитальной области (табл. 5).
Заключение
Нами впервые выявлена частота встречаемости СЛ аногенитальной локализации в структуре ОС, которая составила 59,6%.
Выявлена и проанализирована связь аногенитального СЛ с этиологическими факторами заболевания: в 71% случаев выявлены ИППП и воспалительные заболевания малого таза; в 33,8% случаев — ВПЧ высокого канцерогенного риска, ВПГ I и II типа; в 19,3% случаев — хронические воспалительные заболевания органов малого таза; в 27,4% случаев — хроническая очаговая инфекция различной локализации; в 19,4% случаев — заболевания сердечно-сосудистой системы; в 3,2% случаев — патология желудочно-кишечного тракта и гепатобилиарной системы.
Нами был оптимизирован протокол комплексного метода лечения ОС, включая склероатрофические поражения аногенитальной локализации. Протокол может быть рекомендован для усовершенствования лечения пациентов с данной патологией в связи с его высокой клинической эффективностью, достигающей 98%.
Только для зарегистрированных пользователей