Что такое платина, свойства драгоценного металла и его применение
«Плохое серебро» или «серебришко» — такое название получила платина, когда с ней впервые столкнулись европейцы. Недооцененная тогда, а в дальнейшем ставшая «королевой» среди благородных металлов, она и по сей день находится во главенстве ювелирного мира украшений. Так что же из себя представляет этот необычный и редкий сплав? Каковы свойства платины, ее состав, история и чем этот металл отличается от других?
Что такое платина и как она выглядит
Платина — это драгоценный металл серебристо-белого цвета, который является одним из самых дорогих и редких на планете. Такое название она получила благодаря испанским конкистадорам, которые считали ее грязным металлом. Золото, найденное в сплаве вместе с платиной, считалось гнилым, потому что его невозможно было очистить от «серебришка».

Долгое время платина стоила вдвое дешевле серебра. Испанская корона запретила ввозить ее в страну, а найденные самородки повелевала собирать и топить на глубине рек и морей, чтобы избежать подделки серебряных монет. Самое интересное, что позже Испания отменила этот запрет, потому что сама стала фальсифицировать золото и серебро с помощью платины.
В это же время сталкиваются с «плохим серебром» алхимики, считавшие до этого самым тяжелым металлом золото. Из-за своей плотности платина была намного тяжелее, поэтому «искатели философского камня» наделили ее адскими чертами. Позже во Франции именно из платины был изготовлен эталон метра, а затем и эталон килограмма.
В России с платиной впервые столкнулись на Урале, назвав вначале ее «белым золотом». Запасы «нового сибирского металла» были столь велики, что Россия заняла первое место по добыче в мире. Самый крупный самородок был назван «Уральским гигантом» с массой около восьми килограмм, который по сей день хранится в Алмазном фонде.
Какие украшения изготавливают из платины
Платина — это самый износостойкий металл с антикоррозийными свойствами, олицетворяющий собой символ твердости и надежности. Представьте себе обручальные или помолвочные кольца из платины — неподвластные времени, как и самая сильная любовь.

Большим недостатком украшений из этого сплава будет дороговизна, если сопоставить аналогичные изделия из белого золота и платины, то второе будет дороже примерно в три раза. Неслучайно приведено сравнение между этими двумя металлами, так как они внешне очень похожи. Именно спрос на белое золото породил такую популярность платины.
Отдельно стоит упомянуть о сочетании платины с бриллиантами. Только такая оправа из серо-белого цвета способна подчеркнуть глубину и прозрачность камней. Недаром ведь до того, как приобрели известность платина и белое золото, бриллианты крепили именно в серебро. А учитывая такую естественную твердость платины, вы будете всегда знать, что «камешки» всегда хорошо закреплены в кольце. Такое украшение способно подчеркнуть высокий уровень благосостояния и уверенности в себе.

Ювелирная отрасль не основная для этого благородного металла. В медицине из платины делают электроды для больных стенокардией, используют в зубоврачебном деле, при лечении онкозаболеваний. С ее помощью делают также зеркала для лазерной техники, изготавливают стабильные и долговечные электрические контакты.
Как отличить платину от других металлов
Белое золото отличается от платины тем, что платина — естественно белый металл, в то время как золото становится белым путем различных примесей к желтому сплаву серебра/никеля/палладия. Причем не так давно были открыты аллергические свойства никеля, поэтому его активно заменяют палладием. Золото достаточно часто покрывают родием для большей «серебристости» оттенка, который со временем тускнеет при ношении изделия.
Платина всегда будет «чище» других сплавов, обладая высокой 950 пробой, а это значит, что примесей других металлов практически нет, что снижает возникновение аллергических реакций до минимума. Достаточно редко встречаются пробы 850 и 900, изделия при этом получаются более тусклыми. Золото же изготавливается с пробой 500, 585 и в лучшем случае — 750.

Украшение из белого золота будет легче на десять процентов аналогичного из платины. Золото — очень мягкий металл, а платина — один из самых твёрдых сплавов, поэтому изделия не царапаются и не деформируются со временем.
Отличить платину от серебра ещё проще — последнее мягче даже золота и очень пластично. Более того, платина плотнее практически в два раза.
Исходя из всех достоинств и недостатков, несложно понять, лучше золото или платина? Помимо того, что платиновые украшения будут более долговечны и практичны, это еще и очень хороший способ вложения денег, ведь цена на металл продолжает регулярно расти.
Как определить подлинность платины в домашних условиях
По причине того, что платина очень дорогой металл, количество недобросовестных продавцов в интернете только растет. Покупать украшения лучше всего только в ювелирных магазинах, но даже и здесь можно встретить обман. Как же самостоятельно проверить платину в домашних условиях? Какими способами воспользоваться, чтобы удостовериться в подлинности изделия?

Один из самых простых способов распознать платину — это проверка на вид и на ощупь:
Имеются способы химического анализа подтверждения подлинности:
Если вы все еще не уверены в том, точно ли ваш аксессуар выполнен из платины, то обратитесь за помощью к надежному ювелиру. Специалист выполнит проверку более достоверно и в кратчайший срок.
Платина
В 1735 году испанский король издаёт указ, повелевающей платину впредь в Испанию не ввозить. При разработке россыпей в Колумбии повелевалось тщательно отделять её от золота и топить под надзором королевских чиновников в глубоких местах речки Рио-дель-Пинто, которую стали именовать Платино-дель-Пинто. А ту платину, которая уже привезена в Испанию, повелевалось всенародно и торжественно утопить в море.
В 1748 году испанский математик и мореплаватель А. де Ульоа первым привез на европейский континент образцы самородной платины, найденной в Перу. Впервые в чистом виде из руд платина была получена английским химиком У. Волластоном в 1803 году итальянский химик Джилиус Скалигер в 1835 году открыл неразложимость платины и таким образом доказал, что она является независимым химическим элементом.
В России еще в 1819 году в россыпном золоте, добытом на Урале был обнаружен «новый сибирский металл». Сначала его называли белым золотом, платина встречалась на Верх-Исетских, а затем и на Невьянских и Билимбаевских приисках. Богатые россыпи платины были открыты во второй половине 1824 года, а на следующий год в России началась ее добыча.
Происхождение названия
Название платине было дано испанскими конкистадорами, которые в середине XVI в. впервые познакомились в Южной Америке (на территории современной Колумбии) с новым металлом, внешне похожим на серебро ( plata ). Слово исп. Platina буквально означает «маленькое серебро», «серебришко» (платина против серебра стоила вдвое дешевле). Объясняется такое пренебрежительное название исключительной тугоплавкостью платины, которая не поддавалась переплавке, долгое время не находила применения и ценилась вдвое ниже, чем серебро.
Получение
Самородную платину добывают на приисках (см. подробнее в статье Благородные металлы)
Физические свойства
Серовато-белый пластичный металл, температуры плавления и кипения — 1769 °C и 3800 °C, удельное электрическое сопротивление — 0,098 мкОм•м. Платина — один из самых тяжелых (плотность 21,5 г/см³; атомная плотность 6.62•10 22 ат/см³) и самых редких металлов: среднее содержание в земной коре 5•10 −7 % по массе.
Химические свойства
По химическим свойствам платина похожа на палладий, но проявляет большую химическую устойчивость. Реагирует только с горячей царской водкой: 3Pt + 4HNO3 + 18HCl = 3H2[PtCl6] + 4NO + 8H2O
Платина медленно растворяется в горячей серной кислоте и жидком броме. Она не взаимодействует с другими минеральными и органическими кислотами. При нагревании реагирует со щелочами и пероксидом натрия, галогенами (особенно в присутствии галогенидов щелочных металлов): Pt + 2Cl2 + 2NaCl = Na2[PtCl6]. При нагревании платина реагирует с серой, селеном, теллуром, углеродом и кремнием. Как и палладий, платина может растворять молекулярный водород, но объем поглощаемого водорода меньше и способность его отдавать при нагревании у платины меньше.
При нагревании платина реагирует с кислородом с образованием летучих оксидов. Выделены следующие оксиды платины: черный PtO, коричневый PtO2, красновато-коричневый PtO3, а также Pt2O3 и Pt3O4.
C обнаруженного Н. Бартлеттом взаимодействия между Хе и PtF6, приводящего к образованию XePtF6, началась химия инертных газов. PtF6 получают фторированием платины при 1000 °C под давлением. Фторирование платины при нормальным давлении и температуре 350—400 °C даёт фторид Pt(IV): Pt + 2F2 = PtF4 Фториды платины гигроскопичны и разлагаются водой. Тетрахлорид платины (IV) с водой образует гидраты PtCl4·nH2O, где n = 1, 4, 5 и 7. Растворением PtCl4 в соляной кислоте получают платинохлористоводородные кислоты H[PtCl5] и H2[PtCl6]. Синтезированы такие галогениды платины как PtBr4, PtCl2, PtCl2·2PtCl3, PtBr2 и PtI2. Для платины характерно образование комплексных соединений состава [PtX4]2— и [PtX6]2-. Изучая комплексы платины, А. Вернер сформулировал теорию комплексных соединений и объяснил природу возникновения изомеров в комплексных соединениях.
Реакционная способность
Платина является одним из самых инертных металлов. Она нерастворима в кислотах и щелочах, за исключением царской водки. Платина также непосредственно реагирует с бромом, растворяясь в нём.
При нагревании платина становится более реакционноспособной. Она реагирует с пероксидами, а при контакте с кислородом воздуха — с щелочами. Тонкая платиновая проволока горит во фторе с выделением большого количества тепла. Реакции с другими неметаллами (хлором, серой, фосфором) происходят менее охотно. При более сильном нагревании платина реагирует с углеродом и кремнием, образуя твёрдые растворы, аналогично металлам группы железа.
В своих соединениях платина проявляет почти все степени окисления от 0 до +8, из которых наиболее устойчивы +2 и +4. Для платины характерно образование многочисленных комплексных соединений, которых известно много сотен. Многие из них носят имена изучавших их химиков (соли Косса, Магнуса, Пейроне, Цейзе, Чугаева и т. д.). Большой вклад в изучение таких соединений внес русский химик Л. А. Чугаев (1873−1922), первый директор созданного в 1918 году Института по изучению платины.
Гексафторид платины PtF6 является одним из сильнейших окислителей среди всех известных химических соединений. С помощью него, в частности, канадский химик Нейл Бартлетт в 1962 году получил первое настоящее химическое соединение ксенона XePtF6.
Катализатор
Платина, особенно в мелкодисперсном состоянии, является очень активным катализатором многих химических реакций, в том числе используемых в промышленных масштабах. Например, платина катализирует реакцию присоединения водорода к ароматическим соединениям даже при комнатной температуре и атмосферном давлении водорода. Еще в 1821 немецкий химик И. В.Дёберейнер обнаружил, что платиновая чернь способствует протеканию ряда химических реакций; при этом сама платина не претерпевала изменений. Так, платиновая чернь окисляла пары винного спирта до уксусной кислоты уже при обычной температуре. Через два года Дёберейнер открыл способность губчатой платины при комнатной температуре воспламенять водород. Если смесь водорода и кислорода (гремучий газ) ввести в соприкосновение с платиновой чернью или с губчатой платиной, то сначала идет сравнительно спокойная реакция горения. Но так как эта реакция сопровождается выделением большого количества теплоты, платиновая губка раскаляется, и гремучий газ взрывается. На основании своего открытия Дёберейнер сконструировал «водородное огниво» — прибор, широко применявшийся для получения огня до изобретения спичек.
Производство
До 1748 г. платина добывалась и производилась только на территории Америки и в Старом Свете не была известна.
Когда платину стали завозить в Европу её цена была вдвое ниже серебра. Ювелиры очень быстро обнаружили, что платина хорошо сплавляется с золотом, а так как плотность платины выше чем у золота, то незначительные добавки серебра позволила изготавливать подделки, которые невозможно было отличить от золотых изделий. Такого рода подделки получили столь широкое распространение, что испанский король приказал прекратить ввоз платины, а оставшиеся запасы утопить в море. Этот закон просуществовал до 1778 года. После отмены закона потребность в платине была небольшой, её использовали в основном для создания химического оборудования, приспособлений и в качестве катализаторов. Добываемой в Америке платины для этих целей было достаточно. Ни о каком значимом промышленном производстве говорить не приходится.
В 1819 году платину впервые обнаружили на Урале близ Екатеринбурга, а в 1824 г. были открыты платиновые россыпи в Нижнетагильском округе. Разведанные запасы платины были столь велики, что Россия почти сразу заняла первое место в мире по добыче этого метала. Только в 1828 году в России было добыто 1,5 т платины — больше, чем за 100 лет в Южной Америке. К концу XIX века в России добывалось платины в 40 раз больше чем во всех остальных странах мира. Причем, представлена она была и весьма увесистыми самородками. Например, один из найденных на Урале самородков весил 9,6 кг.
К середине XIX в. в Англии и Франции были проведены обширные исследования по аффинажу платины. В 1859 году французский химик Анри Этьен Сент-Клер Девиль впервые разработал промышленный способ получения слитков чистой платины. С этого времени, почти вся добываемая на Урале платина скупалась английскими и французскими фирмами, в частности, «Джонсон, Маттей и К°». Позже к закупкам платины у России подключились американские и немецкие компании.
Даже после значительных зарубежных закупок, большая часть добываемой Россией платины не находила достойного применения. Поэтому, начиная с 1828 года, по предложения министра финансов Егора Канкрина, в России начали выпускать платиновые монеты номиналом 3,6 и 12 рублей. При этом, 12-рублевая платиновая монета имела массу 41,41 г, а в рублевой серебряной монете было 18 г чистого серебра. То есть по стоимости металла платиновые монеты были дороже серебряных в 5,2 раза. С 1828 по 1845 гг. было выпушено 1 372 000 трехрублевых монет, 17 582 шестирублевых и 3 303 двенадцатирублевых общей массой 14,7 т. Основную выгоду от добычи получали владельцы рудников — Демидовы. Оцените, — только в 1840 было добыто 3,4 т платины. В 1845 году, по настоянию министра финансов Фёдора Вронченко выпуск платиновых монет был прекращён и все они были срочно изъяты из обращения. Основной версией столь поспешного шага считается повышение европейских цен на платину, в результате которого монеты стали дороже номинала. После прекращения чеканки монет производство платины в России упало в 20 раз и к 1915 году на долю России приходилось лишь 95 % от мирового производства платины. Оставшиеся 5 % производила Колумбия. Причем, почти вся российская платина поступала на экспорт. Например, в 1867 году Англия скупила весь запас российской платины — более 16 т.
К концу XIX в. Россия производила 4,5 т. платины в год.
До Первой мировой войны второй после России страной по объемам добычи платины была Колумбия; с 1930-х гг. стала Канада, а после Второй мировой войны — Южная Африка.
В 1952 году Колумбия добыла 0,75 т платины, США — 0,88 т, в Канада — 3,75 т, а Южно-Африканский Союз — 7,2 т. В СССР данные по добыче платины были засекречены.
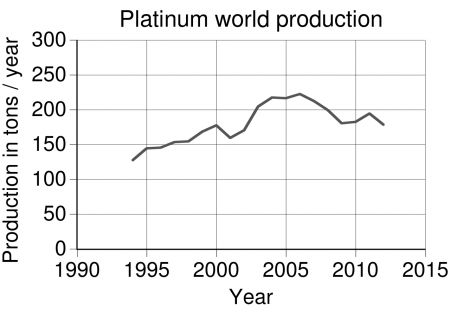
В 2007 году в мире было добыто 213 т платины, а в 2008 году — 200 т. Лидерами добычи были: ЮАР (в 2007 году добыто 166,0 т, а в 2008 году — 153,0 т), Россия (27,0/25,0), Канада (6,2/7,2), Зимбабве (5,3/5,6), США (3,9/3,7), Колумбия (1,4/1,7). [3]
Лидером добычи платины в России является ГМК «Норильский никель».
Разведанные мировые запасы металлов платиновой группы составляют около 80 000 т и распределены, в основном, между Южной Африкой (87,5 %), Россией (8,3 %) и США (2,5 %).
Применение
В технике
В медицине
Соединения платины (преимущественно, тетрахлорплатинаты) применяются, как цитостатики («цис-платина»). Однако в настоящее время имеются более эффективные противораковые лекарственные средства.
В ювелирном деле
Платина и её сплавы широко используются для производства ювелирных изделий.
Ежегодно мировая ювелирная промышленность потребляет около 50 тонн платины. До 2001 года большая часть ювелирных изделий из платины потреблялась в Японии. С 2001 года на долю Китая приходится примерно 50 % мировых продаж. В 1980 г. Китай потреблял около 1 % ювелирных изделий из платины. В настоящее время в Китае ежегодно продаётся около 10 млн изделий из платины общей массой около 25 тонн.
Российский спрос на ювелирную платину составляет 0,1 % от мирового уровня.
Монетарная функция
Платина, золото и серебро — основные металлы, выполняющие монетарную функцию. Однако платину стали использовать для изготовления монет на несколько тысячелетий позже золота и серебра.
Первые в мире платиновые монеты были выпущены и находились в обращении в Российской империи с 1828 по 1845 год. Чеканка началась с трехрублевиков. В 1829 г. «были учреждены платиновые дуплоны» (шестирублевики), а в 1830 г.— «квадрупли» (двенадцати-рублевики). Были отчеканены следующие номиналы монет: достоинством 3, 6 и 12 рублей. Трехрублевиков было отчеканено 1 371 691 шт., шестирубле-виков — 14 847 шт. и двенадцатирублевиков — 3474 шт. [2]
В 1846 г. чеканка платиновой монеты была прекращена, хотя к этому году добыча уральской платины составила около 2000 пудов или 32 000 кг, из которых в монету было перечеканено 14 669 кг. Громадной количество платины, скопившейся на Петербургском монетном дворе частью в виде монеты, а частью в необработанном виде (по разным данным от 720 до 2000 пудов), было продано английской фирме Джонсон, Маттэ и Ко. В результате Англия, которая не добывала ни одного грамма платины, долго была в этой отрасли монополистом. [5]
После 1846 года ни одна страна не позволяла себе «роскоши» вводить в обращение платиновые монеты. Выпускаемые разными странами в настоящее время платиновые монеты являются инвестиционными монетами. В период с 1992 по 1995 год инвестиционные платиновые монеты номиналами 25, 50 и 150 рублей выпускал Банк России.
Платина
(молярная масса)
(первый электрон)
470 кДж/моль
гранецентрированная
Содержание
История
В Старом Свете платина не была известна до середины XVI века, однако цивилизации Анд (инки и чибча) добывали и использовали её с незапамятных времён. Первыми европейцами, познакомившимися с платиной в середине XVI века, были конкистадоры. Считается, что первым в литературе упомянул о платине Скалигер в опубликованной в 1557 году книге «Экзотерические упражнения в 15 книгах», где он, полемизируя с Кардано о понятии «металл», рассказал о некоем веществе из Гондураса, которое нельзя расплавить. Вероятно, этим веществом и была платина.
В 1735 году испанский король издаёт указ, повелевающий платину впредь в Испанию не ввозить. При разработке россыпей в Колумбии повелевалось тщательно отделять её от золота и топить под надзором королевских чиновников в глубоких местах речки Рио-дель-Пинто (приток Рио-Сан-Хуан (англ.) русск. ), которую стали именовать Платино-дель-Пинто. А ту платину, которая уже привезена в Испанию, повелевалось всенародно и торжественно утопить в море. Королевское распоряжение было отменено через 40 лет, когда мадридские власти приказали доставлять платину в Испанию, чтобы самим фальсифицировать золотые и серебряные монеты. В 1820 году в Европу было доставлено от 3 до 7 тонн платины. Здесь с нею познакомились алхимики, считавшие самым тяжёлым металлом золото. Необычайно плотная платина оказалась тяжелее золота, поэтому алхимики посчитали её непригодным металлом и наделили адскими чертами. Некоторое применение платина нашла позже во Франции, когда из неё был изготовлен эталон метра, а позже эталон килограмма.
Согласно некоторым источникам, испанский математик и мореплаватель А. де Ульоа в 1744 году привёз образцы платины в Лондон, он поместил описание платины в своём отчёте о путешествии в Южную Америку, опубликованном в 1748 году. В 1789 А. Лавуазье включил платину в список простых веществ. Впервые в чистом виде из руд платина была получена английским химиком У. Волластоном в 1803 году.
В России ещё в 1819 году в россыпном золоте, добытом на Урале, был обнаружен «новый сибирский металл», который сначала называли белым золотом. Платина встречалась на Верх-Исетских, а затем и на Невьянских и Билимбаевских приисках. Богатые россыпи платины были открыты во второй половине 1824 года, а на следующий год в России началась её добыча. В 1826 году П. Г. Соболевский и В. В. Любарский изобрели метод выработки ковкой платины с помощью прессования и последующей выдержки в раскалённом добела состоянии.
Происхождение названия
Название платине было дано испанскими конкистадорами, которые в середине XVI в. впервые познакомились в Южной Америке (на территории современной Колумбии) с новым металлом, внешне похожим на серебро (исп. plata ). Слово буквально означает «маленькое серебро», «серебришко». Объясняется такое пренебрежительное название исключительной тугоплавкостью платины, которая не поддавалась переплавке, долгое время не находила применения и ценилась вдвое ниже, чем серебро.
Нахождение в природе
Изотопы
Месторождения
Платина является одним из самых редких металлов: её среднее содержание в земной коре (кларк) составляет 5⋅10 −7 % по массе. Даже так называемая самородная платина является сплавом, содержащим от 75 до 92 процентов платины, до 20 процентов железа, а также иридий, палладий, родий, осмий, реже медь и никель.
Основная часть месторождений платины (более 90 %) заключена в недрах пяти стран. К этим странам относятся ЮАР (Бушвелдский комплекс), США, Россия, Зимбабве, Китай.
Получение
Самородную платину добывают на приисках (см. подробнее в статье Благородные металлы), менее богаты рассыпные месторождения платины, которые разведываются, в основном, способом шлихового опробования.
Производство платины в виде порошка началось в 1805 году английским ученым У. Х. Волластоном из южноамериканской руды.
Получаемую таким образом губчатую платину подвергают дальнейшей очистке повторным растворением в царской водке, осаждением (NH4)2PtCl6 и прокаливанием остатка. Затем очищенную губчатую платину переплавляют в слитки. При восстановлении растворов солей платины химическим или электрохимическим способом получают мелкодисперсную платину — платиновую чернь.
Физические свойства
Серовато-белый пластичный металл, температуры плавления и кипения — 2041,4 K ( 1768,3 °C ) и 4098 K ( 3825 °C ) соответственно, удельное электрическое сопротивление — 0,098 мкОм·м (при 0 °С ). Платина — один из самых тяжёлых (плотность 21,09—21,45 г/см³ ; атомная плотность 6,62⋅10 22 ат/см³ ) металлов. Твёрдость по Бринеллю — 50 кгс/мм 2 (по Моосу 3,5).
Платина устойчива к вакууму и может применяться в космической технике.
Химические свойства
По химическим свойствам платина похожа на палладий, но проявляет бо́льшую химическую устойчивость. При комнатной температуре реагирует с царской водкой:
Платина медленно растворяется в горячей концентрированной серной кислоте и жидком броме. Она не взаимодействует с другими минеральными и органическими кислотами. При нагревании реагирует со щелочами и пероксидом натрия, галогенами (особенно в присутствии галогенидов щелочных металлов):
При нагревании платина реагирует с серой, селеном, теллуром, углеродом и кремнием. Как и палладий, платина может растворять молекулярный водород, но объём поглощаемого водорода и способность его отдавать при нагревании у платины меньше.
При нагревании платина реагирует с кислородом с образованием летучих оксидов. Выделены следующие оксиды платины: чёрный PtO, коричневый PtO2, красновато-коричневый PtO3, а также Pt2O3 и смешанный Pt3O4, в котором платина проявляет степени окисления II и IV.
Для платины известны гидроксиды Pt(OH)2 и Pt(OH)4. Получают их при щелочном гидролизе соответствующих хлороплатинатов, например:
Эти гидроксиды проявляют амфотерные свойства:
Гексафторид платины PtF6 является одним из сильнейших окислителей среди всех известных химических соединений, способный окислить молекулы кислорода и ксенона:
Соединение O2 + [PtF6] − (гексафтороплатинат(V) диоксигенила) летуче и разлагается водой на фтороплатинат(IV), небольшое количество гидратированного диоксида платины и кислород с примесью озона.
С помощью гексафторида платины, в частности, канадский химик Нейл Бартлетт в 1962 году получил первое настоящее химическое соединение ксенона Xe[PtF6].
C обнаруженного Н. Бартлеттом взаимодействия между Хе и PtF6, приводящего к образованию Xe[PtF6], началась химия инертных газов. PtF6 получают фторированием платины при 1000 °C под давлением.
Фторирование платины при нормальным давлении и температуре 350—400 °C даёт фторид платины(IV):
Фториды платины гигроскопичны и разлагаются водой.
Синтезированы такие галогениды платины, как PtBr4, PtCl2, PtCl2·2PtCl3, PtBr2 и PtI2.
Реакционная способность
Платина является одним из самых инертных металлов. Она нерастворима в кислотах и щелочах, за исключением царской водки. Платина также непосредственно реагирует с бромом, растворяясь в нём.
При нагревании платина становится более реакционноспособной. Она реагирует с пероксидами, а при контакте с кислородом воздуха — с щелочами. Тонкая платиновая проволока горит во фторе с выделением большого количества тепла. Реакции с другими неметаллами (хлором, серой, фосфором) происходят менее активно. При более сильном нагревании платина реагирует с углеродом и кремнием, образуя твёрдые растворы, аналогично металлам группы железа.
В своих соединениях платина проявляет почти все степени окисления от 0 до +6, из которых наиболее устойчивы +2 и +4. Для платины характерно образование многочисленных комплексных соединений, которых известно много сотен. Многие из них носят имена изучавших их химиков (соли Косса, Магнуса, Пейроне, Цейзе, Чугаева и т. д.). Большой вклад в изучение таких соединений внес русский химик Л. А. Чугаев (1873−1922), первый директор созданного в 1918 году Института по изучению платины.
Катализатор
Платина, особенно в мелкодисперсном состоянии, является очень активным катализатором многих химических реакций, в том числе используемых в промышленных масштабах. Например, платина катализирует реакцию присоединения водорода к ароматическим соединениям даже при комнатной температуре и атмосферном давлении водорода. Ещё в 1821 немецкий химик И. В. Дёберейнер обнаружил, что платиновая чернь способствует протеканию ряда химических реакций; при этом сама платина не претерпевала изменений. Так, платиновая чернь окисляла пары винного спирта (этанола) до уксусной кислоты уже при обычной температуре. Через два года Дёберейнер открыл способность губчатой платины при комнатной температуре воспламенять водород. Если смесь водорода и кислорода (гремучий газ) ввести в соприкосновение с платиновой чернью или с губчатой платиной, то сначала идет сравнительно спокойная реакция горения. Но так как эта реакция сопровождается выделением большого количества теплоты, платиновая губка раскаляется, и гремучий газ взрывается. На основании своего открытия Дёберейнер сконструировал «водородное огниво» — прибор, широко применявшийся для получения огня до изобретения спичек.
Добыча и производство
До 1748 г. платина добывалась и производилась только на территории Америки, а в Старом Свете не была известна.
Когда платину стали завозить в Европу, её цена была вдвое ниже серебра. Ювелиры очень быстро обнаружили, что платина хорошо сплавляется с золотом, а так как плотность платины выше, чем у золота, то незначительные добавки платины позволили изготавливать подделки, которые невозможно было отличить от золотых изделий. Такого рода подделки получили столь широкое распространение, что испанский король приказал прекратить ввоз платины, а оставшиеся запасы утопить в море. Этот закон просуществовал до 1778 года. После отмены закона потребность в платине была небольшой, её использовали в основном для создания химического оборудования, приспособлений и в качестве катализаторов. Добываемой в Америке платины для этих целей было достаточно. Ни о каком значимом промышленном производстве говорить не приходилось.
В 1819 году платину впервые обнаружили на Урале близ Екатеринбурга, а в 1824 г. были открыты платиновые россыпи в Нижнетагильском округе. Разведанные запасы платины были столь велики, что Россия почти сразу заняла первое место в мире по добыче этого металла. Только в 1828 году в России было добыто 1,5 т платины — больше, чем за 100 лет в Южной Америке. На Урале появились целые платинодобывающие районы, из которых наиболее важными в промышленном отношении стали Исовской и Тагильский.
К середине XIX в. в Англии и Франции были проведены обширные исследования по аффинажу платины. В 1859 году французский химик Анри Этьен Сент-Клер Девиль впервые разработал промышленный способ получения слитков чистой платины. С этого времени почти вся добываемая на Урале платина скупалась английскими и французскими фирмами, в частности, «Джонсон, Маттей и К°». Позже к закупкам платины у Российской империи подключились американские и немецкие компании.
К концу XIX в. Российская империя добывала 4,5 тонны платины в год.
До Первой мировой войны второй после Российской империи страной по объёмам добычи платины была Колумбия; с 1930-х гг. стала Канада, а после Второй мировой войны — Южная Африка.
В 2014 году в мире была добыта 161 т платины. Лидерами добычи были:
Лидером добычи платины в России является ГМК «Норильский никель».
Кроме того, на территории Хабаровского края располагается прииск Кондёр, который является крупнейшим в мире россыпным месторождением платины; его разработку ведёт Артель старателей «Амур» (входит в Группу компаний «Русская платина»), по итогам 2011 года на прииске добыто около 3,7 тонны платины.
Разведанные мировые запасы металлов платиновой группы составляют около 80 000 т и распределены, в основном, между ЮАР (87,5 %), Россией (8,3 %) и США (2,5 %).