Что лучше азитромицин или амоксициллин при отите
Отоларинголог рассказала о течении отита у взрослых
Воспалительные процессы в разных отделах уха приводят к раздражению нервов, отеку и сильной боли. Лечение отита нужно начать как можно быстрее, в противном случае могут быть серьезные последствия.
АЛЕНА ПАРЕЦКАЯ
Врач-патофизиолог, иммунолог, член
Санкт-Петербургского общества патофизиологов
СВЕТЛАНА КОМАРОВА
Врач-отоларинголог, заместитель
главного врача по КЭР в «СМ-Клиника»
Острая боль в ухе – одно из самых мучительных ощущений. Многие пациенты сравнивают ее силу с зубной болью и тяжелыми травмами, а женщины – с процессом родов. Чаще всего ухо болит из-за отита.
Что нужно знать об отите у взрослых
Что такое отит
Отит – это общее название для воспалительных процессов в области уха. Воспаление может быть острым либо хроническим, затрагивая различные отделы уха.
Если воспаление локализовано в ушное раковине и слуховом проходе до границы барабанной перепонки – это наружный отит, воспаление в барабанной полости – средний отит, если затрагивается область улитки, внутренняя часть уха – это внутренний отит или лабиринтит.
Эти патологии крайне болезненны, сопровождаются лихорадкой, нарушениями слуха, выделениями из наружного прохода. Кроме того, без лечения отиты могут угрожать тяжелыми осложнениями – тугоухостью или полной глухотой, парезом в области лицевого нерва, поражением костей или мозга.
Причины отита у взрослых
Наиболее частой причиной наружного отита являются травмы, инфекции кожи и подлежащих тканей в области слухового прохода. Возможна и химическая травма уха, раздражение и воспаление из-за серных пробок, попадания в ухо воды, образования фурункулов.
Средний отит – самая частая форма болезни. Он обычно провоцируется бактериальными инфекциями, реже – вирусами, патогенными грибками, а также микст-инфекцией. Наиболее частые возбудители:
Факторами риска, повышающими вероятность отита, является шмыганье носом, избыток слизи в носоглотке. перепад давления при нырянии, погружении на глубину. Нередко средний отит становится осложнением простуды, ЛОР-патологий (аденоидит, тонзиллит, фарингит, ринит). Риск выше у людей с имунодефицитами.
Симптомы отита у взрослых
При наружном отите самыми частыми жалобами будут:
При хронической форме может возникать мезотимпанит – воспаление локализуется в зоне евстахиевой трубы и нижней, средней части барабанной полости. В перепонке формируется отверстие, но сама перепонка натянута.
Лечение отита у взрослых
Диагностика
Диагноз можно заподозрить на основании типичных жалоб, но врач подробно будет расспрашивать – где и как болит ухо, нажмет на козелок, потянет мочку уха вниз, чтоб определить, есть ли боль. Кроме того, оториноларинголог проведет осмотр уха с использованием приборов и подсветки, чтобы прицельно осмотреть слуховой проход, барабанную перепонку, понять, есть ли в ней гной и перфорация. Чтобы определить чувствительность к антибиотикам, выполняется посев на флору. Также врач может назначить:
Современные методы лечения
Мы попросили рассказать о том, как сегодня лечат отиты у взрослых врача-оториноларинголога Светлану Комарову. По ее словам, медикаментозная терапия может включать:
При осложненном течении отита или не эффективности консервативной терапии показано хирургическое лечение (миринготомия, шунтирование барабанной полости, радикальная операция на среднем ухе), направленное на санацию очага инфекции, восстановление слуха, профилактику рецидивов.
Какие антибиотики эффективны при отите?
– Системная антибактериальная терапия показана во всех случаях среднетяжелого и тяжелого течения острого среднего отита, – говорит врач-оториноларинголог Светлана Ковалева, – а также у пациентов с иммунодефицитными состояниями. При легком течении отита (отсутствии выраженных симптомов интоксикации, болевого синдрома, гипертермии до 38 °С) от назначения антибиотиков можно воздержаться. Однако при отсутствии положительной динамики в течение 48 часов следует прибегнуть к антибиотикотерапии.
При отите назначаются антибиотики широкого спектра действия, эффективные в отношении типичных возбудителей: Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis, Streptococcus pyogenes, Staphylococcus aureus.
Препаратом выбора является Амоксициллин.
При легком и среднетяжелом течении показано пероральное применение антибиотиков. При тяжелом и осложненном течении отита начинают с внутривенного или внутримышечного введения препарата, а далее продолжают лечение перорально.
Самостоятельно применять антибиотики не стоит, необходимо проконсультироваться с врачом-оториноларингологом. Отит может быть вызван грибковой флорой или герпетической инфекцией. Применение антибиотиков в данном случае может усугубить течение заболевания.
Профилактика отита у взрослых в домашних условиях
Для профилактики отита необходимо избегать переохлаждений, мыть руки после улицы, орошать слизистую носа морской водой после посещения мест с большим скоплением народа, заниматься закаливанием организма, спортом, ежедневно употреблять свежие фрукты, овощи, кисломолочные продукты.
Если так случилось, что вы заболели и стал беспокоить насморк, то сморкаться нужно крайне осторожно, при этом освобождать только одну ноздрю, иначе выделения из носа могут попасть через слуховую трубу в ухо и спровоцировать отит.
Необходимо соблюдать правильную гигиену ушей. Не рекомендуется использовать ватные палочки – ими в ухо можно занести бактериальную или грибковую инфекцию. Для гигиены ушей применяйте капли, состоящие из комбинации поверхностно-активных веществ (Аллантоин, Бензетоина хлорид) очищающих, увлажняющих и защищающих кожу наружного слухового прохода.
Популярные вопросы и ответы
Мы обсудили риски осложнений отитов и возможности их лечения при помощи народных методов терапии с ЛОР-врачом Светланой Ковалевой.
Какие могут быть осложнения при отите?
Нерациональное лечение среднего отита может привести к формированию рубцовой ткани в полости среднего уха и к стойкому снижению слуха.
При наружном отите может встречаться поражение черепных нервов в виде парезов и параличей.
Могут развиваться осложнения, которые представляют опасность для жизни. К ним относятся:
Незамедлительно обратится к врачу нужно при наличии следующих симптомов:
Народная медицина не используется в официальной клинической практике, так как не имеет доказательной базы. Фитотерапией можно поддерживать основное лечение при легком течении отита.
В качестве антибактериальных и противовоспалительных средств рекомендуется закладывать в ушную раковину тампоны, смоченные готовой аптечной настойкой календулы.
Антимикробная терапия острого среднего отита в педиатрической практике
Острый средний отит (ОСО) является одним из частых воспалительных заболеваний у детей младшего и среднего возраста [2, 5, 7]. По числу осложнений ОСО занимает второе место среди ЛОР-патологии [4, 10, 11], у 30% детей приобретает затяжное течение и склонно
Острый средний отит (ОСО) является одним из частых воспалительных заболеваний у детей младшего и среднего возраста [2, 5, 7]. По числу осложнений ОСО занимает второе место среди ЛОР-патологии [4, 10, 11], у 30% детей приобретает затяжное течение и склонность к рецидивированию [1]. Острый средний отит — это остро развившееся воспаление полостей среднего уха (барабанной полости, сосцевидного отростка, слуховой трубы), проявляющееся одним или несколькими симптомами (боль в ухе, повышение температуры тела, выделения из уха, у маленьких детей понос, тошнота).
Довольно часто ОСО являются так называемым бактериальным осложнением острых респираторных вирусных инфекций (ОРВИ). При этом может отсутствовать болевой синдром и снижение слуха, а симптомы наблюдающейся общей интоксикации нередко расцениваются врачом как клиническое проявление основного заболевания. Острое воспаление среднего уха выявляется у 19,7% детей, больных ОРВИ (обследовано 3567 пациентов) [8].
При типичном остром среднем отите воспалительный процесс в полостях среднего уха не выходит за рамки выстилающей их слизистой оболочки. Отражающая этот процесс патолого-анатомическая картина достаточно типична и характеризуется отеком, капиллярной гиперемией и лейкоцитарной инфильтрацией слизистой оболочки, особенно ее субэпителиального слоя. А в эпителиальном, покровном слое отмечается некоторое увеличение числа продуцирующих слизь бокаловидных клеток, поэтому в экссудате, образующемся при остром воспалении среднего уха, всегда есть та или иная примесь слизи. В совокупности указанные изменения приводят к выраженной гиперплазии слизистой оболочки среднего уха, особенно в барабанной полости, где ее толщина способна увеличиваться в 30 раз и более. Происходит накопление экссудата, который поначалу может быть серозным, затем серомукозным и далее — мукозно-гнойным и гнойным. Слуховые косточки, которые оказываются погруженными в утолщенную слизистую оболочку барабанной полости и скопившийся в ней экссудат, в значительной степени теряют свою подвижность, что вместе с тугоподвижностью воспалительно-измененной барабанной перепонки обусловливает существенное ухудшение слуховой функции. При увеличении количества экссудата в среднем ухе, давление, оказываемое им на барабанную перепонку, повышается, и это приводит к нарушению микроциркуляции, трофическим и некротическим изменениям барабанной перепонки, следствием которых является образование ее перфорации и появление трансмеатальной отореи.
В детском возрасте острый средний отит имеет ряд особенностей и возникает чаще, чем у взрослых, прежде всего из-за анатомо-физиологических особенностей: более широкая, короткая и горизонтально расположенная слуховая труба, наличие аденоидных вегетаций, более быстрое нарушение функции мерцательного эпителия при воспалении. Несформированный иммунитет может приводить к реактивному и часто осложненному течению детских инфекционных заболеваний. В младенческом возрасте увеличивается риск развития внутричерепных осложнений из-за незаращения каменисто-чешуйчатой щели височной кости, через которую инфекция может проникать в полость черепа, поражая мозговые структуры. Следует отметить, что диагностика отита у детей раннего возраста осложнена из-за ограниченного вербального контакта и затруднений при отоскопии [3].
Основными профилактическими мероприятиями острого среднего отита являются предупреждение и своевременное лечение простудных заболеваний, обучение правильному туалету носа (поочередно правой и левой половин).
Лечение острого среднего отита должно быть комплексным и включать адекватные терапевтические мероприятия, которые можно разделить на местные и общие. Для уменьшения отека в области носоглоточного устья слуховой трубы и восстановления ее вентиляционной и дренирующей функций используют назальные сосудосуживающие капли (Нафтизин, Тизин и т. п.), которые необходимо закапывать в нос при запрокинутой назад голове. Обязательным является лечение сопутствующего ринита или риносинусита. Препараты, вводимые в слуховой проход, должны быть комбинированными и обладать противовоспалительным действием, противобактериальным и противогрибковым, антиаллергическим и обезболивающим эффектами. В ряде случаев, в частности при тяжелом течении отита, необходимо прибегать к антибиотикам системного действия.
При выборе лекарственного средства следует учитывать эпидемиологическую ситуацию, особенности клинической картины, возраст пациента, наличие сопутствующих заболеваний, сведения о ранее проводимой антибактериальной терапии и переносимости лекарственных препаратов.
Антибиотик, применяемый для терапии отитов, должен обладать не только высокой эффективностью, широким спектром антибактериального действия и хорошим проникновением в очаг воспаления, но и низкой токсичностью, удобством приема.
Микробиологическая диагностика средних отитов основана на бактериологическом исследовании содержимого среднего уха, полученного при парацентезе или тимпанопункции. Исследования, проведенные в США, Европе и Японии, показали, что самым распространенным возбудителем острого среднего отита является Streptococcus pneumoniae, на втором месте — нетипируемые штаммы Haemophilus influenzae, на третьем месте — Moraxella catarrhalis. Менее чем 10% ОСО вызываются другими микроорганизмами, например стрептококками группы А и Staphylococcus aureus. Этиология ОСО не может быть установлена по клинической картине, однако следует отметить, что пневмококковый ОСО обычно протекает тяжелее, чаще приводит к развитию осложнений и не склонен к саморазрешению. Из 90 серотипов S. pneumoniae только несколько вызывают ОСО. Наиболее распространены из них серотипы 19, 23, 6, 14, 3 и 18. Использование вакцины, содержащей капсульные полисахариды 7–8 наиболее часто встречаемых серотипов S. pneumoniae, способно предотвратить более чем 80% ОСО пневмококковой этиологии. Большинство штаммов H. influenzae, вызывающих ОСО, являются нетипируемыми. По современным данным, около 20–50% H. influenzae, выделяемых при ОСО, продуцируют бета-лактамазы [9].
Результаты многочисленных многолетних исследований сходны с результатами зарубежных авторов и показывают, что наиболее вероятными возбудителями острого среднего отита в России являются St. aureus, St. epidermidis, S. pneumoniae и H. influenzae, несколько реже Streptococcus pyogenes, S. viridans, M. catarrhalis анаэробы.
В лечении ОСО многочисленными исследованиями достоверно доказана эффективность цефалоспоринов как антибактериальных препаратов широкого спектра действия, в частности Cупракса (цефиксима) — представителя 3-го поколения цефалоспоринов. Супракс обладает высоким уровнем антибактериальной активности, улучшенными фармакокинетическими свойствами, расширенным, по сравнению с цефалоспоринами предыдущих поколений, спектром действия. Бактерицидное действие препарата обусловлено ингибированием пептидогликана — основного структурного компонента клеточной стенки бактерий. Биодоступность препарата (около 50%) позволяет исключить парентеральный путь введения. Максимальная концентрация в крови достигается уже через 4 ч. Супракс хорошо проникает в место инфицирования. Период полувыведения зависит от дозы и составляет 3–4 ч, а в тканях препарат задерживается на более длительный срок, что позволяет принимать его 1 раз в сутки. Препарат хорошо переносится больными. Эти свойства Супракса позволяют считать целесообразным его применение в детской оториноларингологической практике.
Было проведено обследование и лечение 30 детей с ОСО 7–12 лет (девочек — 14, мальчиков — 16). Всем пациентам проводили лечение Супраксом из расчета 5 мг/кг 2 раза в сутки в течение 6 дней.
В качестве контрольных использовали результаты, полученные при наблюдении за аналогичной в количественном и возрастном отношении группой детей, получавших амоксициллина клавуланат (2 дозировочные ложечки по 5 мл (312 мг) 3 раза в сутки парентерально в течение 6 дней).
Обследование включало: ЛОР-осмотр, аудиометрию, тимпанометрию, компьютерную томографию околоносовых пазух, рентгенографию височных костей по Шюллеру и Майеру, клинический анализ крови, бактериологическое исследование отделяемого из слухового прохода при наличии перфорации барабанной перепонки.
По данным микробиологического исследования отделяемого, полученного из слухового прохода у 18 детей обеих групп, среди возбудителей преобладал S. pneumoniae — у 11 детей, реже встречались St. aureus — у 4, H. influenzae — у 2 пациентов, в одном случае роста микрофлоры получено не было.
В результате лечения зафиксировано уменьшение клинических проявлений и положительная динамика объективных критериев заболевания у детей из основной и контрольной групп (тимпанометрия, аудиометрия, клинический анализ крови). Эффективность Супракса была сравнимой с амоксициллина клавуланатом, считающимся препаратом выбора при ОСО [6].
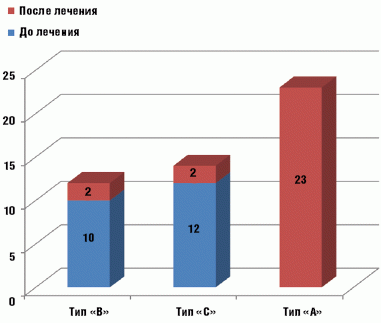
В основной группе до начала лечения у всех детей зарегистрирована кондуктивная тугоухость, тимпанограмма типа «В» выявлена у 10, «С» у 12 детей, 8 детям тимпанометрия не проводилась из-за наличия перфорации. По окончании курса лечения Супраксом кондуктивная тугоухость сохранялась у 7 пациентов, тимпанограмма «А» зафиксирована у 23, «В» у 2 и «С» у 2 пациентов, 3 детям тимпанометрия не проводилась из-за наличия перфорации (рис. 1).
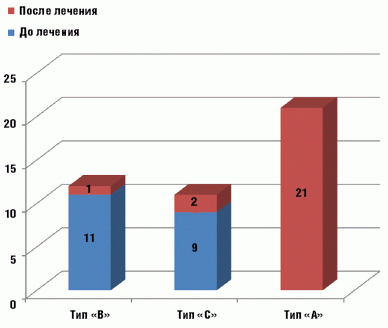
В контрольной группе до начала лечения у всех детей зарегистрирована кондуктивная тугоухость, тимпанограмма типа «В» выявлена у 11, «С» — у 9 больных, 10 детям тимпанометрия не проводилась из-за наличия перфорации. По завершении 6-дневного курса терапии амоксициллина клавуланатом кондуктивная тугоухость сохранялась у 9 пациентов, тимпанограмма типа «А» зафиксирована у 21, «В» — у 1, «С» — у 2 детей, 6 пациентам тимпанометрия не проводилась из-за наличия перфорации (рис. 2).
Нежелательных эффектов, требующих отмены препаратов, ни в одной из групп зафиксировано не было.
Таким образом, подтверждена высокая эффективность и безопасность препарата Супракс при остром среднем отите у детей. Супракс может быть рекомендован для широкого применения в детской оториноларингологической практике.
Литература
О. В. Зайцева, кандидат медицинских наук
ФГУ НКЦ оториноларингологии ФМБА России, Москва
Почему азитромицин остается препаратом выбора при внебольничных инфекциях нижних дыхательных путей
Инфекционно-воспалительные заболевания дыхательных путей занимают первое место в структуре инфекционной патологии. Пневмония является наиболее частой инфекционной причиной смерти в мире.
Инфекционно-воспалительные заболевания дыхательных путей занимают первое место в структуре инфекционной патологии. Пневмония является наиболее частой инфекционной причиной смерти в мире. В России ежегодно около 1,5 млн человек переносят пневмонию. В связи с этим остается актуальной проблема рационального выбора антибактериального средства для лечения инфекций нижних дыхательных путей. Выбор препарата для антибактериальной терапии должен основываться на его спектре действия, охватывающем выделенный или предполагаемый возбудитель, чувствительный к данному антибиотику, фармакокинетических свойствах антибактериального средства, обеспечивающих его проникновение в терапевтической концентрации в соответствующие ткани, клетки и жидкости организма, данных о безопасности антибиотика (побочных эффектах, противопоказаниях и возможном нежелательном взаимодействии с другими лекарствами), характеристиках лекарственной формы, способе введения и режиме дозирования, обеспечивающих высокий комплаенс терапии, фармакоэкономических аспектах лечения [4, 6, 8].
Инфекции нижних дыхательных путей и принципы выбора антибиотика
При неспецифических внебольничных инфекциях выбор антибактериального препарата в большинстве случаев основывается на статистических данных о наиболее частых их возбудителях, а также сведениях о подтвержденной в контролируемых клинических исследованиях эффективности тех или иных антибиотиков при инфекциях известной этиологии. Вынужденно эмпирический подход к лечению связан с отсутствием возможности микробиологического исследования в амбулаторных лечебных учреждениях, длительностью бактериологической идентификации возбудителя и определения его чувствительности к антибиотикам (3–5 дней, а в случае «атипичных» патогенов и больше), невозможностью в ряде случаев получить биологический материал для посева или бактериоскопии (например, около 30% больных пневмониями имеют непродуктивный кашель, что не позволяет исследовать мокроту), трудностями в разграничении истинных возбудителей и сапрофитов (обычно микроорганизмов ротоглотки, попадающих в исследуемый материал). Сложности выбора лекарственного средства в амбулаторных условиях определяются также отсутствием полноценного наблюдения за течением заболевания и, следовательно, своевременной коррекции лечения при его неэффективности. Антибиотики по-разному проникают в различные ткани и биологические жидкости. Лишь некоторые из них хорошо проникают в клетку (макролиды, тетрациклины, фторхинолоны, в меньшей степени — клиндамицин и сульфаниламиды). Поэтому, даже если препарат in vitro проявляет высокую активность в отношении данного возбудителя, но не достигает в месте его локализации уровня, превышающего минимальную подавляющую концентрацию (МПК) для данного микроорганизма, клинического эффекта он не окажет, хотя микробная резистентность к нему будет вырабатываться. Не менее важным аспектом антибактериальной терапии является ее безопасность, особенно для амбулаторного больного, лишенного повседневного медицинского наблюдения. В амбулаторных условиях следует отдавать предпочтение пероральному приему антибиотиков. В педиатрической практике имеют значение органолептические свойства препарата. Для повышения исполняемости пациентом врачебных назначений режим дозирования антибиотика должен быть максимально простым, т. е. предпочтительнее препараты с минимальной кратностью приема и коротким курсом лечения.
Возбудители неспецифических внебольничных инфекций нижних дыхательных путей
Острые респираторные вирусные инфекции (ОРВИ), протекающие с синдромом бронхита, в ряде случаев, чаще в детском возрасте, могут осложняться присоединением бактериальной флоры с развитием острого бронхита. Возбудителями острого бактериального бронхита в детском возрасте являются пневмококк, микоплазма или хламидия, реже гемофильная палочка, моракселла или стафилококк. Острый бактериальный бронхиолит у детей вызывают моракселла, микоплазма и возбудитель коклюша. Острый гнойный трахеобронхит у взрослых в 50% случаев вызывает гемофильная палочка, в остальных случаях пневмококк, реже моракселла (5–8% случаев) или внутриклеточные микроорганизмы (5% случаев).
Среди бактериальных возбудителей обострений хронического бронхита главную роль играют Haеmophilus influenzae (30–70% случаев), Streptococcus pneumoniae и Moraxella catarrhalis. Для курильщиков наиболее характерна ассоциация H. influenzae и M. catarrhalis. В отягощенных клинических ситуациях (возраст старше 65 лет, многолетнее течение болезни — более 10 лет, частые обострения — более 4 раз в год, сопутствующие заболевания, выраженные нарушения бронхиальной проходимости — объем форсированного выдоха за первую секунду (ОФВ1)
С. В. Лукьянов, доктор медицинских наук, профессор ФГУ «Консультативно-методический центр лицензирования» Росздравнадзора, Москва
Значение азитромицина при инфекциях дыхательных путей и ЛОР-органов у детей в амбулаторных условиях
к. м. н. И.А. Дронов
Кафедра детских болезней первого МГМУ им. И.М. Сеченова
В современных условиях более чем в 80% случаев показаниями для назначения антибиотиков в педиатрической практике являются инфекции дыхательных путей и ЛОР-органов. При этом в большинстве случаев антибактериальная терапия проводится в амбулаторных условиях. К антибиотикам, применяемым у детей в амбулаторных условиях, предъявляется ряд важных требований, обеспечивающих успешное лечение.
Высокая эффективность при данном заболевании. В большинстве случаев в амбулаторных условиях проводится эмпирическая антибактериальная терапия, без лабораторного выявления конкретного возбудителя. В связи с этим необходимо, чтобы применяемый антибиотик воздействовал на максимально широкий спектр потенциальных возбудителей.
Высокий профиль безопасности. В амбулаторных условиях, в отличии от стационара, отсутствует перманентное наблюдение медицинского персонала за пациентом и, соответственно, ограничены возможности по раннему выявлению побочных действий при использовании лекарственных средств и проведению своевременной коррекции. В данных условиях риск развития нежелательных лекарственных явлений должен быть сведен к минимуму.
Высокая комплаентность. С современных позиций считается недопустимым применение инъекционных лекарственных средств у детей в амбулаторных условиях, кроме отдельных исключительных случаев (например, отказ родителей от госпитализации). Соответственно, для лечения на дому необходимы лекарственноые средства, которые можно принимать перорально. Также важным условием является использование у детей, особенно раннего возраста, специальной жидкой формы препарата (суспензия, сироп, раствор для приема внутрь). В связи с этим возникает еще ряд важных обстоятельств, например, необходимость приспособления для правильной и удобной дозировки лекарственного средства, а также, если требуется, простота приготовления готовой формы препарата. Также крайне важен оптимальный режим применения лекарственного средства. К основным методам, повышающим комплаентность лечения, относятся уменьшение кратности приема препарата и длительности курса лечения.
Указанным требованиям в полной мере соответствует препарат из группы макролидов азитромицин (Сумамед®). Азитромицин (Сумамед®) – полусинтетический антибиотик, по химической структуре является единственным применяемым в клинической практике представителем особой подгруппы 15-членных макролидов, содержащих в своем составе атом азота, в связи с чем препарат часто выделяют в отдельную группу – азалиды. Наличие атома азота определяет многократно большую кислотоустойчивость азитромицина по сравнению с другими макролидами (в 300 раз выше, чем у эритромицина) [1].
Спектр активности
Азитромицин, как и другие макролиды, обладает высокой активностью в отношении многих грамположительных бактерий: стафилококков (метициллин-чувствительных), стрептококков (включая Streptococcus pneumoniae), Listeria monocytogenes, Corynebacterium diphtheriae. Азитромицин отличается от других макролидов существенно большей активностью в отношении грамотрицательных бактерий. Он превосходит другие препараты группы по эффективности против Haemophilus spp., Moraxella catarrhalis, Neisseria spp., Bartonella spp. и Campylobacter jejuni; в отличие от других макролидов в больших концентрациях способен подавлять рост многих бактерий семейства Enterobacteriaceae (Escherichia coli, Salmonella spp., Shigella spp. и др.); также как другие макролиды проявляет активность в отношении Bordetella pertussis, Helicobacter pylori и некоторых других. Как и другие макролиды, азитромицин высокоактивен в отношении внутриклеточных возбудителей: Mycoplasma spp., Chlamydia spp., Legionella pneumophila и др. Кроме того, азитромицин наряду с другими макролидами обладает определенной активностью в отношении риккетсий, спирохет, некоторых микобактерий, анаэробных бактерий и простейших (возбудителей токсоплазмоза, криптоспоридиоза и малярии) 3.
Азитромицин, как и другие макролиды, оказывает преимущественно бактериостатическое действие, которое обусловлено подавлением синтеза белка на рибосомах бактерий. Однако на основных бактериальных возбудителей респираторных инфекций – Streptococcus pyogenes, S.pneumoniae, Haemophilus influenzae препарат оказывает бактерицидное действие 2. В отношении этих же возбудителей азитромицин проявляет постантибиотический эффект (подавления роста бактерий, продолжающееся в течение некоторого времени после элиминации антибиотика) [1].
Фармакокинетика
Азитромицин имеет уникальную фармакокинетику, выгодно отличающую препарат от всех макролидов и многих антибиотиков из других групп. Биодоступность азитромицина после приема внутрь составляет 37-38% 3. Благодаря высокой кислотоустойчивости препарат не разрушается в желудке. Пища не влияет на всасывание препарата в форме суспензии, но снижает биодоступность при использовании азитромицина в виде капсул [1]. Максимальная концентрация препарата в крови после приема внутрь наблюдается в среднем через 2-3 часа. Связывание препарата с белками плазмы находится в обратной зависимости от концентрации в крови и составляет от 7 до 51%. Азитромицин в очень большом количестве накапливается внутриклеточно, благодаря чему его концентрация во многих тканях организма в 10-200 раз превышает концентрацию в крови. Наиболее высокие концентрации препарата создаются в миндалинах, аденоидах, бронхиальном секрете, слизистой бронхов, жидкости, выстилающей эпителий альвеол, экссудате среднего уха. Именно там они намного превышают МПК для большинства бактериальных возбудителей, вызывающих инфекции данной локализации. Накапливаясь в большом количестве в фагоцитах, азитромицин с помощью этих клеток транспортируется в очаг воспаления, где происходит постепенное высвобождение препарата. Азитромицин имеет очень большой период полувыведения – от 2 до 4 суток (в среднем 68 часов), благодаря чему эффективная концентрация препарата в тканях сохраняется в течение 4-7 дней после завершения курса лечения. Большая часть азитромицина выводится с желчью, небольшая (4,5-6%) – с мочой 1.
По данным большинства исследований, частота нежелательных явлений на фоне приема азитромицина составляет около 9%. При этом в большинстве случаев отмечаются умеренные реакции со стороны желудочно-кишечного тракта (боли в животе, тошнота, рвота, диарея и др.), которые, как правило, не требуют отмены препарата. Редко или очень редко наблюдаются изменения со стороны нервной системы (головная боль, головокружение, сонливость и др.), изменения лабораторных показателей (уровень печеночных ферментов и др.), аллергические реакции (кожная сыпь, отек Квинке и др.), развитие вагинального кандидоза и интерстициального нефрита 4.
Применение в педиатрии
В России оригинальный препарат азитромицина – Сумамед® зарегистрирован в виде капсул в дозе 250 мг, таблеток, покрытых оболочкой, в дозе 125 и 500 мг, порошка для приготовления суспензии для приема внутрь в дозе 100 мг/5 мл и 200 мг/5 мл (Сумамед® форте), а также в виде лиофилизата для приготовления раствора для инфузии в дозе 500 мг. Пероральные формы препарата не имеют возрастных ограничений, но рекомендуется для применения детьми старше 6 месяцев в виде суспензии для приема внутрь и таблеток в дозе 125 мг. Необходимо отметить, что препарат в форме порошка для приготовления суспензии поставляется в комплекте с дозировочной 2-сторонней ложкой (на 2,5 и 5 мл) и дозировочным шприцем (на 5 мл), что обеспечивает удобство приема препарата.
Показаниями к применению азитромицина у детей являются инфекции верхних дыхательных путей и уха (бактериальный фарингит, тонзиллит, синусит, средний отит), инфекции нижних отделов дыхательных путей (бактериальный бронхит, пневмония, обострение хронического бронхита), а также инфекции кожи и мягких тканей, вызванные чувствительными к препарату бактериями. Фармакокинетические свойства препарата дают основания применять его при большинстве инфекций дыхательных путей и ЛОР-органов у детей один раз в сутки в виде коротких курсов (до 5 дней) в суммарной дозе от 30 до 60 мг/кг. Отдельного рассмотрения требуют вопросы рационального применения азитромицина при различных заболеваниях.
Стрептококковый тонзиллофарингит
Стрептококковый тонзиллит (ангина) и стрептококковый фарингит, согласно Международной классификацией болезней 10 пересмотра, являются отдельными заболеваниями, вызванными одним возбудителем – β-гемолитическим стрептококком группы А (S. pyogenes, БГСА). Однако, поскольку в большинстве случаев отмечается сочетанное поражение миндалин и глотки, оба заболевания имеют сходные проявления, вызывают одни и те же осложнения и требуют одинакового лечения, в настоящее время во многих зарубежных и ряде отечественных руководств используется термин стрептококковый тонзиллофарингит. Стрептококковый тонзиллофарингит опасен развитием тяжелых осложнений, которые делятся на 2 группы:
При стрептококковом тонзиллофарингите обязательно проводится антибактериальная терапия, которая направлена не только на излечение пациента, но и на эрадикацию БГСА из организма, что позволяет избежать развития тяжелых поздних осложнений и рецидивов заболевания, а также предотвратить распространение инфекции. БГСА не способен формировать резистентность к пенициллинам, поэтому в качестве препаратов выбора рассматриваются феноксиметилпенициллин и амоксициллин, в особых случаях также может быть использована однократная инъекция бензатина бензилпенициллина. Однако клинический эффект при использовании пенициллинов достигается не всегда. Одной из ведущих является феноменом ко-патогенности – продукцией другими бактериями полости рта (стафилококки, анаэробные бактерии). В этом случае рекомендуется применение альтернативных препаратов, устойчивых к β-лактамазам – ингибиторо-защищенных пенициллинов или цефалоспоринов 1-го поколения. Второй ведущей причиной неэффективности пенициллинов является низкая комплаентность 10-дневного курса лечения, который требуется для эрадикации БГСА. Макролиды, в том числе азитромицин, а также линкозамиды позиционируются при стрептококковом тонзиллофарингите как альтернативные средства, прежде всего при аллергии на β-лактамные антибиотики 5.
Причина ограниченного применения макролидов при стрептококковых инфекциях – наличие у БГСА механизмов резистентности к этим антибиотикам. Поэтому вопрос о применении макролидов при стрептококковом тонзиллофарнигите должен решаться с учетом локальных данных о чувствительности возбудителя к антибиотикам. По результатам российского мультицентрового исследования ПеГАС-I, проведенного в 16 городах России, резистентность S. pyogenes (включая умеренно-резистентные штаммы) к макролидам в 2001-2003 гг. составляла от 0,3% к мидекамицину до 8% к эритромицину и азитромицину [7]. Однако, по предварительным данным последнего аналогичного исследования ПеГАС-III, резистентность БГСА к эритромицину в 2006-2009 гг. составляла 3% [8]. Полученные результаты свидетельствуют в пользу того, что резистентность S. pyogenes к маролидам в России не только не увеличивается, но и уменьшается. Безусловно, это является предиктором высокой эффективности макролидов при стрептококковом тонзиллофарингите.
Для всех альтернативных препаратов рекомендуемый курс терапии при стрептококковом тонзиллофарингите также составляет 10 дней. Единственным исключением является азитромицин, который может применяться более коротким курсом. Это обусловлено особенностями фармакокинетики препарата, в частности тем, что после перорального приема в небных миндалинах длительно отмечается очень высокая концентрация азитромицина, многократно превышающая МПК для БГСА. В научной литературе представлены данные многочисленных исследований эффективности азитромицина при стрептококковом тонзиллофарингите у детей. По данным кокрановского систематического обзора, короткие курсы азитромицина (3-6 дней) при стрептококковом тонзиллофарингите у детей обладают высокой эффективностью, не уступающей препарату выбора – феноксиметилпенициллину [9]. Однако до настоящего времени окончательно не решен вопрос об оптимальной длительности и курсовой дозе азитромицина при стрептококковом тонзиллофарингите. В частности, в исследовании швейцарской группы по изучению фарингита установлено, что 3-дневный курс азитромицина обеспечивает эрадикацию возбудителя в 2 раза реже по сравнению с 10-дневным курсом феноксиметилпенициллина (38 и 81%, соответственно), при одинаково высокой клинической эффективности [10]. Российские эксперты рекомендуют для лечения стрептококкового тонзиллофарингита у детей использовать азитромицин в течение 5 дней в суточной дозе 12 мг/кг [11]. Аналогичной рекомендации придерживается Американская кардиологической ассоциация [12].
Острый средний отит
Среди бактерий наиболее частыми возбудителями острого среднего отита являются H. influenzae и S. pneumoniae. Несмотря на то, что до 70% случаев заболевания может проходить без применения антибактериальной терапии, чаще всего антибиотики должны быть назначены. Это связано с серьезными осложнениями, которые нередко наблюдаются при остром среднем отите – перфорация барабанной перепонки, формирование хронического гнойного отита, гнойный менингит, абсцесс головного мозга и другие.
Препаратом выбора для лечения острого среднего отита является амоксициллин, который в подавляющем большинстве случаев высокоэффективен против гемофильной палочки и пневмококка. В случае неэффективности стартовой терапии амоксициллином в течении 3 дней рекомендуется его замена на ингибиторо-защищенный пенициллин или цефалоспорины 2-3-го поколения, которые устойчивы к воздействию β-лактамаз H. influenzae. В качестве альтернативной терапии, прежде всего при аллергии на β-лактамные антибиотики, рекомендуется использовать прежде всего азитромицин, который является единственным макролидом с высокой активностью против гемофильной палочки: МПК кларитромицина в 4-8 раз выше, а другие макролиды не обладают клинически значимой активностью против H. influenzae [1-3, 5]. По данным российского исследования антимикробной резистентности ПеГАС-III, проведенного в 2006-2009 гг. в нескольких десятках городов страны, азитромицин сохраняет высокую активность в отношении 92,7% штаммов S. pneumoniae [13].
Острый средний отит
Среди бактерий наиболее частыми возбудителями острого среднего отита являются H. influenzae и S. pneumoniae. Несмотря на то, что до 70% случаев заболевания может проходить без применения антибактериальной терапии, чаще всего антибиотики должны быть назначены. Это связано с серьезными осложнениями, которые нередко наблюдаются при остром среднем отите – перфорация барабанной перепонки, формирование хронического гнойного отита, гнойный менингит, абсцесс головного мозга и другие.
Препаратом выбора для лечения острого среднего отита является амоксициллин, который в подавляющем большинстве случаев высокоэффективен против гемофильной палочки и пневмококка. В случае неэффективности стартовой терапии амоксициллином в течении 3 дней рекомендуется его замена на ингибиторо-защищенный пенициллин или цефалоспорины 2-3-го поколения, которые устойчивы к воздействию β-лактамаз H. influenzae. В качестве альтернативной терапии, прежде всего при аллергии на β-лактамные антибиотики, рекомендуется использовать прежде всего азитромицин, который является единственным макролидом с высокой активностью против гемофильной палочки: МПК кларитромицина в 4-8 раз выше, а другие макролиды не обладают клинически значимой активностью против H. influenzae [1-3, 5]. По данным российского исследования антимикробной резистентности ПеГАС-III, проведенного в 2006-2009 гг. в нескольких десятках городов страны, азитромицин сохраняет высокую активность в отношении 92,7% штаммов S. pneumoniae [13].
Рекомендуемая длительность антибактериальной терапии острого среднего отита составляет 7-10 дней для всех препаратов, кроме азитромицина, который можно использовать только 3 дня. По данным кокрановского систематического обзора, короткие курсы азитромицина не уступают по эффективности стандартным курсам других антибиотиков (более 7 дней), но при этом на фоне приема азитромицина существенно реже отмечаются нежелательные лекарственные реакции со стороны желудочно-кишечного тракта [14].
В научной литературе представлено большое количество доказательных клинических исследований, в которых сравнивалась эффективность азитромицина с другими антибиотиками (прежде всего с ко-амоксиклавом) при остром среднем отите у детей. В ряде работ было показано, что клиническая эффективность 3-дневного курса азитромицина (в дозе 10 мг/кг в сутки) сопоставима со стандартным курсом ко-амоксиклава (7-10 дней в дозе 40-45 мг/кг в сутки в расчете на амоксициллин) 17. Также сопоставимая эффективность терапии была получена у детей с рецидивирующим и персистирующим острым средним отитом при использовании высоких доз азитромицина (20 мг/кг в сутки) в течение 3 дней и ко-амоксиклава в течение 10 дней (в дозе 90 мг/кг в сутки в расчете на амоксициллин). При этом комплаентность лечения была выше у пациентов, получавших азитромицин [18]. В то же время, по данным другого исследования, 5-дневный курс азитромицина в стандартной курсовой дозе (10 мг/кг в первые сутки, затем 5 мг/кг в сутки) уступает по клинической и микробиологической эффективности применению ко-амоксиклава в высоких дозах (90 мг/кг в сутки в расчете на амоксициллин) в течение 10 дней [19].
Гнойный риносинусит
При нетяжелом риносинусите лечение может проводиться в амбулаторных условиях. Основными возбудителями риносинусита, так же как и острого среднего отита, являются S. pneumoniae и H. influenzae. У детей до 5 лет частым возбудителем также является M. catarrhalis. Рекомендуется использовать те же антибиотики, что и при остром среднем отите 6. Азитромицин при риносинусите, также как при остром среднем отите, назначается на 3 дня. В ряде исследований было показана, что клиническая эффективность 3-дневного курса азитромицина (в дозе 10 мг/кг в сутки) при остром и подостром синусите у детей сопоставима со стандартным курсом ко-амоксиклава (10 дней в дозе 45 мг/кг в сутки в расчете на амоксициллин) 21.
Внебольничная пневмония
Возбудители пневмонии существенно различаются у детей разного возраста. Лечение пневмонии у детей старше 6 месяцев во многих случаях может проводиться амбулаторно. У детей старше 6 месяцев ведущим возбудителем внебольничной пневмонии является S. pneumoniae. В редких случаях пневмонию у детей (как правило, до 6 лет) может вызывать H. influenzae. В то же время частыми возбудителями пневмонии являются атипичные бактерии – Mycoplasma pneumoniae и Chlamydia pneumoniae, доля которых существенно увеличивается с возрастом, и у подростков они играют основную этиологическую роль при внебольничной пневмонии [5]. В амбулаторных условиях для лечения пневмонии, вызванной типичными возбудителями, препаратами выбора являются амоксициллин и ингибиторо-защищенные пенициллины. В качестве альтернативных средств рассматриваются цефуроксима аксетил, а также макролиды, эффективные в отношении гемофильной палочки – азитромицин и кларитромицин. При пневмонии, вызванной атипичными возбудителями, у детей используются макролиды, которые обладают высокой стабильной активностью в отношении M. pneumoniaе и C. pneumoniaе. Другие антибактериальные средства при пневмонии данной этиологии не применяются либо из-за отсутствия активности против данных возбудителей (все β-лактамные антибиотики, аминогликозиды, линкозамиды), либо из-за возрастных ограничений (фторхинолоны, тетрациклины).
При нетяжелой пневмонии, вызванной типичными бактериями, продолжительность антибактериальной терапии, как правило, составляет 5-10 дней. При пневмонии, вызванной атипичными бактериями, лечение должно быть более длительным – до 14 дней. В тоже время, независимо от этиологии, курс лечения азитромицином составляет 3 дня.
Учитывая, что в клинической практике далеко не всегда можно дифференцировать пневмонию, вызванную типичными и атипичными возбудителями, для стартовой эмпирической терапии нетяжелой внебольничной пневмонии у детей наиболее рационально использовать антибиотики из группы макролидов, прежде всего азитромицин, который обладает высокой активностью как в отношении типичных (S. pneumoniae, H. influenzae), так и в отношении атипичных возбудителей. Кроме того, целесообразность использования азитромицина при пневмонии основывается на фармококинетических свойствах препарата, поскольку в легочной ткани создаются его высокие концентрации.
Проведенные доказательные исследования показали, что по клинической эффективности при внебольничной пневмонии у детей азитромицин не уступает другим антибиотикам. В двух рандомизированных клинических исследованиях было показано, что эмпирическая терапия азитромицином в течение 5 дней у детей в возрасте с 6 месяцев до 16 лет обладает таким же высоким клиническим эффектом, как терапия ко-амоксиклавом (у детей до 5 лет) или эритромицином (у детей старше 5 лет) в течение 10 дней. При этом нежелательные явления при использовании азитромицина наблюдались существенно реже 22. Еще в одном исследовании азитромицин (длительность курса – 3 дня) показал несколько большую эффективность по сравнению с целенаправленной антибактериальной терапией: при пневмонии, вызванной типичными бактериями, назначали амоксициллин на 7 дней, а при пневмонии, вызванной антипичными бактериями, применяли эритромицин в течение 14 дней [24].
Таким образом, анализ научной литературы показывает, что препарат азитромицин (Сумамед®) обладает оптимальными качествами для антибактериальной терапии при инфекциях дыхательных путей и ЛОР-органов у детей в амбулаторных условиях.