Пантогам и Элькар как средства «метаболической» коррекции у часто болеющих детей.
Дети дошкольного возраста с донозологическими (пограничными) отклонениями в состоянии здоровья составляют около 60–80% в популяции. Пограничные состояния (предболезнь) означают высокий риск формирования хронической патологии и требуют организации своевременных реабилитационных мероприятий с использованием новых медицинских технологий (С.О.Ключников и соавт, 2005; О.В. Зайцева, 2004).
В этом плане перспективным является революционно развивающееся в последние десятилетия так называемое «метаболическое» направление, имеющее своей целью теоретический и прикладной анализ нарушений обменных процессов на различных уровнях, составляющих основу или фон при формировании многих заболеваний (В.С. Сухоруков,Е.А. Николаева, 2004).
Результаты многочисленных эпидемиологических исследований свидетельствуют о том, что в среднем каждый ребенок переносит от 3 до 5 эпизодов ОРЗ в год. Наибольшая заболеваемость острыми респираторными инфекциями встречается у детей раннего возраста, дошкольников и младших школьников. Дети первых 3-х лет жизни болеют ОРЗ в течение года в 2–2,5 раза чаще, чем дети в возрасте 10 лет и старше. Рецидивирующие респираторные инфекции приводят к нарушениям функционального состояния организма, могут обуславливать срыв адаптации и вызывать развитие хронической патологии. В связи с этим именно дети раннего и дошкольного возраста нуждаются в пристальном внимании, как педиатров, так и узких специалистов.
Часто болеющий ребенок – это не нозологическая форма. По мнению большинства отечественных педиатров, в группу часто болеющих принято относить детей, подверженных частым респираторным заболеваниям, вследствие преходящих нарушений в защитных системах организма (Н.А. Коровина; В.К. Таточенко; Г.А. Самсыгина; и др.).
Следует выделять комплекс факторов,влияющих на повышенную частоту ОРЗ у детей: анатомо-физиологические особенности респираторного тракта у детей (узкие просветы дыхательных путей, недостаточное развитие эластической ткани и др.), запаздывание созревания иммунной системы, социальные условия жизни (питание, бытовые условия) и др.
К факторам риска повторных респираторных заболеваний у детей также можно отнести: неблагоприятные жилищные условия, низкий уровень образования и санитарной культуры в семье, вредные привычки родителей, плохие взаимоотношения между супругами и частые стрессовые ситуации в семье. Особо следует отметить «пассивное курение», приводящее к снижению местного иммунитета слизистых респираторного тракта и повышению аллергизации организма.
Одним из важных факторов, влияющих на частоту простудных заболеваний, является проживание в экологически неблагоприятных районах. Повышение содержания различных ксенобиотиков в воздухе, воде, продуктах питания сопровождается накоплением их в организме, что приводит к изменениям клеточного метаболизма, нарушениям гомеостаза и иммунной защиты. Риск развития ОРЗ у детей значительно возрастает вследствие ятрогенного воздействия на организм при нерациональном использовании различных лекарственных средств – длительное и необоснованное применение антибиотиков, сульфаниламидов, салицилатов и др.
Резюмируя многочисленные научные исследования можно констатировать, что патогенетической основой частых и длительных респираторных заболеваний является изменение иммунологической реактивности организма ребенка. Изменения при этом неспецифичны, разнонаправлены и могут затрагивать все звенья иммунитета. Однако в основе снижения противоинфекционной резистентности детей лежат транзиторные, функциональные изменения не только иммунной системы, но и всего гомеостаза, что необходимо учитывать при составлении реабилитационных программ(В.К. Таточенко, Н.А. Коровина, 2002).
Проведенные нами комплексные исследования (более 300 детей) свидетельствуют о возможности использования целого ряда доступных в практической педиатрии и высоко информативных методов объективной индивидуальной оценки адаптационных возможностей у детей различного возраста.
Все обследованные дети имели осложненное течение внутриутробного развития(хроническая и/или острая гипоксия), различную патологию на первом году жизни(рахит, анемия, дисбиоз и др.), частые простудные заболевания, что было общим и неспецифичным набором факторов неблагоприятного преморбидного фона у данной категории детей. На основании результатов кардиоинтервалографии у подавляющего числа часто болеющих детей обнаружено нарушение вегетативной регуляции, что выражалось в виде изменения исходного вегетативного тонуса в сочетании с нарушением вегетативной реактивности. Наиболее неблагоприятными считались исходная ваготония в сочетании с гиперсимпатикотонической вегетативной реактивностью и исходная гиперсимпатикотония в сочетании с асимпатикотонической вегетативной реактивностью.
Использование метода Л.Х. Гаркави (расчет по относительному содержанию лимфоцитов) позволил выделить среди всех обследованных часто болеющих детей 5 групп с различным уровнем адаптации: реакция тренировки, спокойной активации, повышенной активации, стресса и переактивации (Е.А. Кантимирова, 2005).
Данные группы детей различались между собой как по целому ряду клинических проявлений (хронический тонзиллит, увеличение аденоидных вегетаций, гастродуоденит, кардиопатии и др.), так и по характеристикам вегетативной реактивности организма. Так, например, для детей 1-й группы (реакция стресса) характерно наибольшее число случаев увеличения аденоидных вегетаций, хронического синусита и изменений со стороны ЦНС (задержка темпов речевого развития, астеноневротический синдром); для 2-й группы (реакция тренировки) – значительно реже диагностирован хронический тонзиллит; тогда как у детей 5-й группы (реакция переактивации) этот показатель был наибольшим и именно у них чаще диагностированы функциональные нарушения со стороны ЖКТ и сердечно-сосудистой системы.
При обследовании детей отмечена четкая взаимосвязь показателей вегетативной регуляции (по данным кардиоинтервалографии) и определенного типа неспецифической адаптационной реакции. С переходом от реакций стресса через реакции тренировки к реакциям спокойной активации наблюдается отчетливое усиление влияния симпатической нервной системы в регуляции сердечного ритма. На это указывает уменьшение абсолютного значения кардиоинтервалов, увеличение их однородности, снижение вариационного размаха и значительное возрастание уровня функционирования центрального контура регуляции ритма сердца. Подобная направленность вегетативных изменений сохраняется и у детей 4-й группы (реакция повышенной активации), однако динамика значений кардиоинтервалов и вариационного размаха, еще более выраженная у детей 5-й группы (реакция переактивации), свидетельствует о снижении функционирования центрального контура ритма сердца и происходящей перестройки в автономном контуре взаимосвязей симпатического и парасимпатического отделов вегетативной нервной системы.
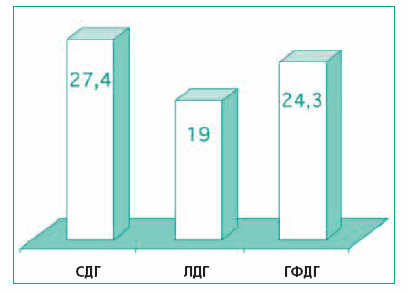
Определенная зависимость при этом обнаружена и с активностью митохондриальных ферментов (СДГ, ГФДГ и ЛДГ), разнонаправленные изменения которых наблюдались в подавляющем большинстве случаев и свидетельствовали о значительных метаболических и регуляторных сдвигах у часто болеющих детей (С.О. Ключников и соавт.,2005). Сходные изменения активности митохондриальных ферментов лимфоцитов у данной категории детей были обнаружены и в исследовании Е.И. Шабельниковой(2005).
Использование в качестве метаболиче ской коррекции таких лекарственных препаратов как Пантогам и L-карнитин (Элькар 20%) позволило существенно улучшить состояние здоровья и компенсаторные возможности детей, степень нормализации которых во многом зависела от исходного адаптационного уровня и глубины митохондриальной дисфункции. Дозы препаратов назначались в соответствии с утвержденными инструкциями с учетом возраста детей. Препараты применялись однократно: Элькар – до 10 часов утра, Пантогам – с 12 до 13 часов. Длительность терапии составила один месяц. Необходимо отметить, что в данной группе (28 детей) не применялись какие-либо иммунотропные препараты.
Рис. 1 Изменение вегетативной реактивности у часто болеющих детей
(%) на фоне комплексной терапии (Пантогам + Элькар).
На фоне терапии в 100% наблюдений отмечена положительная динамика клинических проявлений (жалобы, эмоциональная лабильность, качество сна, аппетита, устойчивость к нагрузкам и др.) наряду с нормализацией показателей вегетативной реактивности (рис. 1). Индивидуальный анализ показал, что наиболее значительная положительная динамика вегетативной реактивности характерна для детей с 1-й и 4-й группами крови, тогда как у детей с 3-й группой крови эти показатели были подвержены наименьшим изменениям. Значение фенотипических особенностей для развития и течения заболеваний, эффективности медикаментозной терапии подтверждаются раннее проведенными исследованиями О.К. Ботвиньева (1985) и некоторых других исследователей. Однако полученные в наших исследованиях результаты (в связи с небольшим объемом наблюдений) могут рассматриваться как предварительные, хотя и могут иметь важное практическое значение.
Рис. 2. Динамика активности митохондриальных ферментов
у часто болеющих детей на фоне комплексной терапии (%).
Динамика клинических признаков у наблюдавшихся часто болеющих детей тесно коррелировала с восстановлением ферментативной активности лимфоцитов (рис. 2).
Положительная динамика изменений активности митохондриальных ферментов была зарегистрирована во всех наблюдениях, хотя и варьировала в достаточно больших пределах от 8,7% до 62,3% (в среднем от 19,5% до 24,3%). Одной из ведущей при-чин столь значительной вариабельности показателей клеточного энергообмена являются существенные различия в исходной глубине нарушений и уровне адаптационноприспособительных процессов у детей, только по частоте острых респираторных заболеваний искусственно объединяемых в одну группу «часто болеющих».
Тем не менее, можно констатировать, что примененная в работе комплексная терапия в виде Пантогама и Элькара может рассматриваться как «неспецифическая» для данной категории детей. Важной особенностью применявшихся препаратов явилось отсутствие каких-либо побочных эффектов даже у детей с отягощенным аллергоанамнезом и наличием признаков резидуального поражения центральной нервной системы. Особое значение приобретают и фармакоэкономические преимущества «метаболической» коррекции, что, однако, требует самостоятельного обсуждения.
Таким образом, данный подход (комплексное применение Пантогама и Элькара)позволяет существенно улучшить состояние здоровья часто болеющих детей, нормализуя механизмы вегетативной регуляции организма и стабилизируя клеточный энергообмен. При этом в каждом конкретном случае должны учитываться индивидуальные особенности организма ребенка, в том числе и наличие различных функциональных изменений, что необходимо для выбора адекватной программы лечения и реабилитации, включающей средства метаболической коррекции.
Элькар в практике педиатра
Фармакология
Е.Николаева, доктор медицинских наук, Московский НИИ педиатрии и детской хирургии Росздрава
Карнитин относится к незаменимым витаминоподобным веществам. В 1905 г. П.З. Кримбергом и В.С. Гулевичем он был впервые выделен из экстракта мышечной ткани. Основные метаболические функции карнитина связаны с процессами преобразования биологической энергии, поэтому в особенно больших количествах он содержится в тканях, нуждающихся в высоком энергетическом обеспечении, — скелетных мышцах, миокарде сердца, головном мозге, печени и почках.
Карнитин обеспечивает перенос жирных кислот в митохондрии, где происходит их окисление и высвобождение ацетил-КоА – субстрата для цикла Кребса. Карнитин осуществляет модуляцию внутриклеточного гомеостаза кофермента А в матриксе митохондрий, таким образом регулируя интенсивность биоэнергетического метаболизма. Исключительно важна (его) роль карнитина в детоксикации и выведении из тканей избытка уксусной и ряда других органических кислот, накапливающихся в ходе окислительно-восстановительных превращений. Кроме того, карнитин участвует в процессах гликолиза, синтеза жирных кислот, обмена кетоновых тел и холина [5]. У взрослых потребность организма в карнитине, составляющая 200—500 мг/сут, удовлетворяется за счет эндогенного его образования не более чем на 10—25% Синтез карнитина осуществляется главным образом клетками печени (в меньшей степени — почек) путем трансформации двух аминокислот: лизина и метионина. Источником аминокислот служат белки пищевых продуктов, а также собственные протеины мышечной ткани. В синтезе карнитина участвуют витамины С,В3, В6,В12, фолиевая кислота и железо.
Отмечено, что потребность в карнитине резко возрастает при стрессе, физических, умственных и эмоциональных перегрузках, интеркуррентных заболеваниях, недостаточном питании, а также в период беременности и лактации. Именно в ситуациях высокого расходования энергетических ресурсов, требующих повышенного катаболизма, становится очевидным исключительное значение для организма карнитинзависимых биологических процессов.
У детей, особенно раннего возраста, эндогенный синтез карнитина крайне ограничен, причем на активность эндогенного образования влияет функциональное состояние печени и почек, а выведение карнитина из организма значительно усиливается при интеркуррентных заболеваниях, дисфункции почечных канальцев, расстройствах деятельности желудочно-кишечного тракта. Обычный пищевой рацион далеко не полностью обеспечивает потребность в карнитине [1].
Таким образом, недостаточность эндогенного синтеза карнитина и его поступления с пищевыми продуктами создают возможность для развития дефицита этого вещества в организме, особенно при состояниях, способствующих повышенному выведению и нарушению всасывания. В результате нередко развивается недостаточность карнитина с ее многообразными системными проявлениями.
Главными органами-мишенями служат скелетные мышцы и миокард, во вторую очередь страдают клетки головного мозга, печень и почки. Основные признаки дефицита L-карнитина являются следствием развивающихся нарушений энергетического обмена и метаболизма липидов и связанных с этим расстройств других видов обмена веществ (быстрая утомляемость, мышечная слабость, гипотония, отставание физического и психомоторного развития, снижение успеваемости, сонливость или раздражительность, нарушение функции сердца и печени). Все это обусловливает необходимость использования дополнительных источников карнитина для лечения и профилактики его недостаточности карнитина в организме.
Существуют две изомерные формы карнитина: D- и L-стереоизомеры.
Установлено, что в тканях млекопитающих присутствует только L-стереоизомер, и именно он биологически эффективен. В настоящее время в большинстве стран мира используют только препараты на основе L-карнитина. Сведений о каких-либо значительных побочных эффектах их применения нет.
D-изомер карнитина — синтетического происхождения; в изолированном виде он не используется, однако имеются лекарственные формы на основе рацемической смеси D,L-карнитинов. Экспериментальные исследования с чистыми изомерами показали, что D-карнитин — не просто неэффективное или биологически инертное вещество, а потенциально токсичное соединение, которое негативно влияет на биосинтез в печени, конкурентно ингибирует процессы усвоения L-карнитина и нарушает его проникновение в миокард, мышечную ткань и почки [6].
Эффективность элькара при различных заболеваниях у детей, изучалась в ведущих медицинских учреждениях страны — Московском НИИ педиатрии и детской хирургии Росздрава, Научном центре здоровья детей РАМН, Российском государственном медицинском университете, Тверской государственной медицинской академии, Волгоградском государственном медицинском университете и др.
В МНИИ педиатрии и детской хирургии элькар уже в течение 5 лет применяется при лечении наследственных заболеваний (в том числе сердечно-сосудистой системы и врожденной патологии), для коррекции развития детей раннего возраста, в психоневрологии, при радиационном риске и т.д.
На фоне длительного лечения элькаром (в суточной дозе 30—50 мг на 1 кг массы тела; в течение 4 мес) у 35 детей с митохондриальными заболеваниями отмечено достоверное улучшение клинического статуса: снижение утомляемости, повышение мышечного тонуса и силы мышц, улучшение походки и координации движений, повышение умственной работоспособности. При этом зарегистрированы снижение уровня лактата и пирувата в крови, улучшение перекисного окисления липидов. У 11 больных с доказанным низким уровнем общего карнитина в крови отмечено достоверное его повышение после приема элькара в течение 3 нед. Ликвидация недостаточности карнитина при митохондриальных заболеваниях — важное средство борьбы с лактат-ацидозом и коррекции энергетического дефицита. В период лечения элькаром ухудшения состояния детей(;) не зафиксировано; у пациентов с митохондриальным синдромом MELAS отсутствовали инсультоподобные приступы. Длительное лечение элькаром (в суточной дозе 50—100 мг/кг; в течение 4 мес) 12 детей с органическими ацидемиями способствовало стабилизации их общего состояния (улучшение аппетита, купирование приступов тошноты и рвоты, повышение мышечного тонуса, нормализация метаболических показателей). После 3-недельного приема элькара у 6 детей с резко пониженным уровнем карнитина в крови он достоверно повысился, преодолев нижнюю границу нормы. Одновременно произошло достоверное снижение ранее повышенного уровня лактата в крови и уменьшилась патологическая почечная экскреция органических кислот.
Использование элькара (суточная доза 20—30 мг/кг; в течение 3 мес) у 36 детей с синдромами Марфана и Элерса—Данло привело к повышению толерантности к физической нагрузке, уменьшению частоты и интенсивности головной боли, увеличению мышечной силы и тонуса. У всех больных с доказанным дефицитом карнитина (23 ребенка с синдромом Элерса—Данло и 8 — с синдромом Марфана) после терапии элькаром в течение 3 нед его содержание в крови увеличилось [4].
При лечении 30 больных с синдромом Ретта (элькар в суточной дозе 30—50 мг/кг; в течение 3 мес) установлено (оценка с помощью балльной шкалы) достоверное снижение выраженности большинства клинических показателей: уменьшились проявления аутизма, повысилась психическая активность и социализация поведения, активизировалась речевая деятельность, улучшились эмоциональные реакции, целенаправленные движения рук и мышечный тонус, появились новые моторные навыки (ходьба, сидение и др.).
После применения элькара (суточная доза 20—30 мг/кг; в течение 3 мес) у всех 50 пациентов с туберозным склерозом отмечены повышение двигательной и общей психической активности, общего фона настроения и параметров устойчивости внимания. У детей школьного возраста улучшались качество оперативной памяти, концентрация, распределение и переключение внимания.
Использование элькара (суточная доза 20 мг/кг : в течение 2 мес — 3 курса в год) у 30 детей с резким дефицитом длины тела, страдающих моногенными синдромами (Нунан, Рассела—Сильвера, Рубинштейна—Тейби и др.), способствовало увеличению скорости роста, достоверному улучшению переносимости физической нагрузки, уменьшению функциональных изменений ЦНС.
Анализ эффективности элькара при выхаживании 87 недоношенных детей и новорожденных с последствиями родовой травмы продемонстрировал, что после 1,5-месячного курса (суточная доза 50 – 100 мг/кг в 3 равных приема перед едой) у всех детей улучшился аппетит, произошла заметная прибавка массы тела, повысилась двигательная активность, улучшилась реакция захвата предметов, значительно активизировалась познавательная деятельность, появилась реакция на музыкальные звуки.
Препараты L-карнитина входят в число основных лекарственных средств, назначаемых в комплексной терапии при заболеваниях сердца, особенно при кардиомиопатиях у детей. Эффективность использования сердечной мышцей жирных кислот в качестве источника энергии тесно связана с уровнем L-карнитина в миокарде. Как показали наблюдения, прием элькара заметно улучшил сократимость сердечной мышцы у 65 детей с кардиомиопатией различной природы (дилатационной, гипертрофической, на фоне первичных митохондриальных синдромов); стойко уменьшилась выраженность симптомов сердечной недостаточности, сократились размеры сердца, более благоприятным стал отдаленный прогноз [5].
В Тверской государственной медицинской академии проанализирована эффективность элькара у 15 детей, страдавших диабетической кардиомиопатией. Его назначали дополнительно к общепринятой метаболической терапии — с целью нормализации метаболических процессов в миокардиоцитах и улучшения выработки энергии в форме АТФ (30 мг/кг в сутки в 2—3 приема в течение 3—4 нед). В результате проведенного лечения у больных нормализовалась диастолическая функция левого желудочка. По данным допплер-эхокардиографии, улучшились скоростные показатели трансмитрального диастолического потока, уменьшилась ригидность миокарда в фазу диастолы. Кроме того, отмечен переход от гипокинетического типа гемодинамики к эукинетическому, что проявлялось увеличением конечного диастолического и ударного индексов, снижением общего периферического сопротивления сосудов. У 11 детей, не получавших элькар в составе кардиометаболической терапии, достоверной положительной динамики показателей трансмитрального диастолического потока и центральной гемодинамики не отмечалось [1].
Сотрудниками Волгоградского государственного медицинского университета проведено динамическое клинико-биохимическое исследование 24 детей в возрасте от 4 до 32 дней жизни, находившихся на лечении в отделении патологии новорожденных по поводу патологической гипербилирубинемии. Комплекс консервативной терапии, помимо внутривенной инфузии растворов глюкозы, эссенциале, энтерального приема витаминов В2, Е, метионина, фенобарбитала и др., дополнительно включал элькар в суточной дозе 50—150 мг/кг (в 2 приема; длительность курса лечения от 14 до 28 дней). Группой сравнения служили 10 новорожденных, получавших то же лечение, за исключением элькара. Исследование показало, что применение элькара в комплексной консервативной терапии неонатальной желтухи способствует ускорению темпов регресса симптомов желтухи, достоверному снижению уровня непрямого билирубина и повышению коэффициента снижения билирубина [3].
В научном Центре здоровья детей РАМН элькар использовался для лечения 170 детей разного возраста (от первых месяцев жизни до 18 лет) с перинатальным неблагополучием в анамнезе и различным исходом патологии нервной системы. При назначении элькара ориентировались на средние возрастные дозы; длительность курсов лечения составляла 1—3 мес.
Клинические эффекты элькара отмечены в сенсорной, двигательной, вегетативной сферах и психическом реагировании при различных патологических состояниях нервной системы. Действие препарата более отчетливо проявилось в ведущем звене нарушения развития (в частности, отмечены улучшение регуляторных процессов у детей с расторможенностью, повышение эмоциональной устойчивости и коммуникативной функции при аутизме) [1].
Таким образом, многочисленные и разносторонние исследования убедительно доказали эффективность элькара для лечения и профилактики различных заболеваний у детей, начиная с самого раннего возраста.
Элькар ® (Elcar ® ) инструкция по применению
Владелец регистрационного удостоверения:
Произведено:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Элькар ®
Гранулы шипучие для приготовления раствора для приема внутрь белые или белые с желтоватым оттенком, со слабым лимонным запахом; после растворения гранул образуется бесцветный или с желтоватым оттенком слабо опалесцирующий раствор со слабым лимонным запахом.
| 1 пак. | |
| левокарнитин | 1000 мг |
Фармакологическое действие
Препарат для коррекции метаболических процессов.
Улучшает белковый и жировой обмен, повышает секрецию и ферментативную активность желудочного и кишечного соков, улучшает усвоение пищи, снижает избыточную массу тела и уменьшает содержание жира в мышцах. Повышает устойчивость к физическим нагрузкам, угнетает образование кетокислот и анаэробный гликолиз, уменьшает степень лактатацидоза, способствует экономному расходованию гликогена и увеличивает его запасы в печени и в мышцах.
Оказывает анаболическое и липолитическое действие. Нормализует повышенный основной обмен при гипертиреозе, являясь периферическим (косвенным) антагонистом действия тиреоидных гормонов, а не прямым ингибитором функции щитовидной железы.
Улучшает обмен веществ и энергообеспечение тканей.
Фармакокинетика
Всасывание и распределение
Метаболизм и выведение
Выводится почками, преимущественно в виде ацильных эфиров.
Показания препарата Элькар ®
В составе комплексной терапии у взрослых:
В спортивной медицине и при интенсивных тренировках (в период тренировочного процесса при отработке аэробной производительности):
Открыть список кодов МКБ-10
| Код МКБ-10 | Показание |
| E05 | Тиреотоксикоз [гипертиреоз] |
| E56.8 | Недостаточность других витаминов |
| E71.3 | Нарушения обмена жирных кислот |
| F07 | Расстройства личности и поведения, обусловленные болезнью, повреждением или дисфункцией головного мозга |
| F50.0 | Нервная анорексия |
| G71.3 | Митохондриальная миопатия, не классифицированная в других рубриках |
| G72.8 | Другие уточненные миопатии |
| G92 | Токсическая энцефалопатия |
| G93.4 | Энцефалопатия неуточненная |
| I42 | Кардиомиопатия |
| I67.4 | Гипертензивная энцефалопатия |
| I69 | Последствия цереброваскулярных болезней |
| K29 | Гастрит и дуоденит |
| K86.1 | Другие хронические панкреатиты |
| L21 | Себорейный дерматит |
| L40 | Псориаз |
| L93.0 | Дискоидная красная волчанка |
| L94.0 | Локализованная склеродермия [morphea] |
| P05 | Замедленный рост и недостаточность питания плода |
| P15.8 | Другие уточненные родовые травмы |
| P21 | Асфиксия в родах |
| P92.2 | Вялое сосание новорожденного |
| P94 | Нарушения мышечного тонуса у новорожденного |
| R62 | Отсутствие ожидаемого нормального физиологического развития |
| S06 | Внутричерепная травма |
| T90 | Последствия травм головы |
| Z54 | Состояние выздоровления |
| Z54.0 | Состояние выздоровления после хирургического вмешательства |
| Z73.0 | Переутомление |
| Z73.3 | Стрессовые состояния, не классифицированные в других рубриках (физическое и умственное напряжение) |
Режим дозирования
Препарат принимают внутрь, за 30 мин до еды. Содержимое пакетика растворяют в 100-200 мл воды комнатной температуры (15-25°С) и принимают сразу после приготовления. 1 пакетик содержит 1000 мг (1 г) карнитина.
При интенсивных и длительных физических нагрузках, психоэмоциональных нагрузках назначают по 1-2 г (1-2 пакетика) 3 раза/сут.
Побочное действие
Побочные реакции, которые могут возникнуть во время применения препарата, относятся к категории очень редких ( ®
Препарат следует хранить в недоступном для детей, защищенном от света, сухом месте при температуре не выше 25°C.