Что меньше днк или клетка
Что меньше днк или клетка
ДНК (сокращение от дезоксирибонуклеиновая кислота) – это одна из важнейших для живых существ молекула, в которой содержится вся генетическая информация о них. Если представить, что живое существо – это какой-нибудь сложный прибор, например, магнитофон, то ДНК можно сравнить с пленкой, на которой записаны инструкции по созданию магнитофона и его функционированию.
Молекулы ДНК есть в каждой клетке нашего организма, и они хранятся в ядре (существует еще одна внеядерная разновидность ДНК –митохондриальная, она кратко описана в словаре). Если достать ДНК всего лишь из одной клетки и вытянуть, то длина полученной нити составит около двух метров. При этом размеры клеточного ядра не превышают шести микрометров (микрометр – это одна миллионная часть метра). ДНК помещается в ядро за счет того, что она многократно свернута и уложена в компактные тельца – хромосомы. У человека в ядре каждой клетки хранятся 23 пары хромосом – один набор приходит от отца, второй – от матери. Исключением являются половые клетки – яйцеклетка и сперматозоид, которые несут только половину всех хромосом. Такое «сокращение» необходимо, чтобы при слиянии сперматозоида и яйцеклетки образовался бы организм с нормальным набором хромосом.
В каждой клетке есть специальные системы, которые считывают заложенную в ДНК информацию и на ее основе создают новые белки (белки выполняют в клетке огромное число функций – от строительства до регуляции прочтения заложенных в ДНК инструкций). Хранящиеся в ДНК «послания» особым образом закодированы. Код ДНК состоит из четырех «символов», или нуклеотидов. Эти четыре разновидности нуклеотидов обозначаются буквами А (аденин), Т (тимин), Г (гуанин) и Ц (цитозин).
В нитях ДНК нуклеотиды соединены один за другим в длинные цепочки. В итоге закодированная информация выглядит примерно так: ААТГЦГТААГЦЦ… и так далее. Для непосвященного человека подобный набор букв кажется бессмысленным, однако клеточные «шифровальщики» точно знают, как на основе заложенной в ДНК информации синтезировать нужные клетке белки.«Шифровальщики» узнают определенные последовательности нуклеотидов, называемые генами. Каждый ген кодирует один белок. Именно поэтому гены называют элементарными единицами наследственности.
Если спросить человека на улице, что приходит ему в голову, когда он слышит слово «ДНК», то, скорее всего, ответом будет «двойная спираль». У нас пока о двойной спирали не было ни слова. Что же это такое, и почему за ее открытие американские ученые Джеймс Уотсон и Френсис Крик получили Нобелевскую премию по физиологии и медицине?
Двойная спираль – это пространственная структура, в форме которой существует ДНК. Дело в том, что нити ДНК «не любят» быть поодиночке. У каждой нити есть напарница, с которой они переплетаются на всем своем протяжении. В итоге как раз и образуется двойная спираль. Нити ДНК объединяются в пары не просто так. Во-первых, двойная спираль значительно более стабильна, чем одиночная нить. Во-вторых, сдвоенные цепочки ДНК не путаются, поэтому считывание информации проходит без проблем. В-третьих, вторая цепь необходима в качестве гарантии сохранности информации. Нити ДНК соединяются в пары случайным образом, а, как говорят ученые, по принципу комплементарности. Это означает, что напротив каждого нуклеотида в одной нити всегда находится строго определенный нуклеотид из второй нити. Парой для А всегда выступает Т, а напарником Г является Ц.
Эта особенность ДНК позволяет однозначно восстановить последовательность нити, имея на руках ее комплементарную копию. Если ДНК каким-либо образом повреждается и теряются кусочки одной из нитей, специальные белки заполняют возникшие бреши, используя в качестве матрицы для синтеза новой нити ее напарницу.
Существует еще один критически важный для клетки процесс, который требует существования двойной спирали. Это деление клеток. Перед тем как удвоиться, клетка синтезирует вторую копию всей своей ДНК. Это происходит так: двойные спирали расплетаются, и специальные белки создают новые комплементарные копии к каждой из оставшихся поодиночке нитей. В итоге снова образуются двойные спирали, но их уже вдвое больше, чем было исходно. Когда клетка разделяется надвое, каждая половинка получает по одному полному комплекту ДНК.
Механизмы синтеза новых цепей работают очень точно, однако иногда происходят сбои, и на месте, скажем, нуклеотида А появляется нуклеотид Г. Причем ошибка может произойти не только в одном нуклеотиде: из цепи ДНК могут выпасть (или появиться) сразу несколько «букв». Ошибки размером в один нуклеотид получили название однонуклеотидных полиморфизмов, ошибки большего размера специального названия не имеют и объединяются под термином «мутации» (сюда входят и однонуклеотидные полиморфизмы).
Мутации могут никак не сказываться на работе клетки (например, если они произошли между генами), могут улучшить ее работу, а могут вызвать серьезный сбой. Последнее часто происходит в том случае, если из-за мутаций нарушается синтез того или иного белка. Именно мутации являются причиной многих наследственных заболеваний.
Чтоб убедиться в абсурдности самозарождения, давайте посмотрим, как устроен микромир. Отметим, что рассмотрим мы его лишь поверхностно, так как он чересчур сложен.
Клетка — элементарная единица строения и жизнедеятельности всех живых организмов. Она обладает собственным обменом веществ, способна к самостоятельному существованию, самовоспроизведению и развитию. Каждая клетка – это город в миниатюре, состоящий из электростанций, путепроводов, очистных сооружений и т.д. Клетка состоит из ядра, мембраны, цитоплазмы, хромосом, рибосом, ДНК, РНК, белков и многих других элементов, каждый из которых, в свою очередь, имеет собственный микромир. Естественно, клетка может существовать и выполнять свои функции, если все эти структуры созданы одновременно.
Молекула белка (протеина) состоит из 50 – 40000 соединенных между собой аминокислот.
Рис. Принцип строения белка из аминокислот
Причем разнообразие белковых структур, создаваемых из 20 видов аминокислот, трудно переоценить. Так, цепочка из 100 аминокислот (небольшой белок) может быть представлена более чем в 10 в 130 степени вариантах, попросту говоря, 10 и 130 нолей. Для примера: в мировом океане 10 в 40 степени молекул воды (10 и 40 нолей). Причем, месторасположение каждой аминокислоты в структуре белка имеет огромное значение, как в компьютерной программе. Если хоть один элемент переставить местами, молекула протеина не будет работать, а значит, не сможет функционировать и выполнять свое предназначение и клетка, то есть часть организма, в которой нужны клетки с этими белками не будут работать. Представьте, как ничтожно мала возможность спонтанного появления самого простого протеина и тем более конкретного который нужен клетке и как следствие организму! А ведь для функционирования простейших клетки и организма нужны тысячи различных протеинов.
Без рибосом и РНК аминокислоты не могут соединиться в протеин, тем более именно в такой, какой необходим на данном этапе конкретной клетке. РНК берет информацию об этом нужном белке из ДНК, а рибосомы выступают в качестве строительной площадки.
Рис. Синтез белка в клетке
В молекуле ДНК хромосом человека насчитывается от 50 до 245 миллионов сложно выстроенных пар азотистых оснований. Биохимики посчитали, что в 1 молекуле ДНК возможно 10 в 87 степени вариантов соединения находящегося в ней материала. И лишь один вариант позволит создать Вас лично – со всеми правильно функционирующими органами и индивидуальными качествами. Ученые-материалисты считают, что земле 4,5 млрд. лет. Этот период времени соответствует 10 в 25 степени секунд. То есть, если каждую секунду придумывать один вариант ДНК, то и возраста Земли не хватит, для того чтоб создать одну функционирующую ДНК. Но дело не только в колоссальной сложности ДНК. Дело в том, что ДНК является программой, которую можно сравнить с компьютерным кодом. Только этот код по своей величине и сложности превосходит программы, созданные человеком. Знаменитый программист Билл Гейтс так говорил о ДНК: «Человеческая ДНК подобна компьютерной программе, только бесконечно совершеннее». Задумайтесь, раз есть программа, то нужен и считывающий механизм, иначе любая программа всего лишь мусор. Так вот, ДНК содержит и код для создания механизма для считывания информации с себя и дальнейшего строительства по этой программе всего организма. В ДНК записано где и в какое время в человеке должен быть создан определенный белок и другие элементы. Из одной клетки, в которой находится ДНК, начинается самостроительство любого организма. Делиться молекуле ДНК позволяет ее строение. Она состоит из двух параллельных идентичных ниток нуклеотидов, связанных слабой химической водородной связью. Когда молекула делится, цепочка разрывается, оставляя всю информацию в каждой из полученных новых клеток.
Здесь уместно вспомнить о риторическом вопросе, на который материалисты никогда не смогут найти ответа: «Что было ранее курица или яйцо?». Не смотря на кажущуюся комичность вопроса, он очень серьезен. Курица, не могла бы появиться без яйца – совершенного устройства для образования эмбриона, роста зародыша и развития его в курицу. Так и яйцо не могло появиться вдруг неоткуда без курицы. Данная взаимоисключающая аналогия накладывается и на другие спорные моменты материалистической теории эволюции. Как было выше отмечено, любой организм имеет ДНК, в которую записана вся информация о нем. Без этого готового ДНК с заложенной в него информацией не было бы этого совершенного организма. Так и ДНК можно взять только из уже созданного существа.
Сэр Фред Хойль профессор астрономии в Кембридже посвятил много времени математическому вычислению возможности случайного возникновения жизни и впоследствии заявил: «Скорее смерч, промчавшийся через кладбище старых автомобилей, может собрать «Боинг-747» из хлама, поднятого в воздух, чем из неживой природы сможет возникнуть живая».
Поэтому, наука до сих пор не может привести повторяющегося примера самозарождения жизни!
Сколько у нас генов?
Сколько у нас генов?
Найти ответ на этот вопрос оказалось куда сложнее, чем кто-либо предполагал
Автор
Редактор
Статья на конкурс «био/мол/текст»: Это интересный вопрос, ответ на который должен был дать проект «Геном человека», завершившийся в 2003 году. После того как ученые получили основную информацию о геноме человека, они попытались определить число генов, но эта задача оказалось не такой простой. Цель настоящей статьи — суммировать и проанализировать научные данные по составлению каталога генов у человека.
Конкурс «био/мол/текст»-2018
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2018.
Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Спонсором приза зрительских симпатий выступил медико-генетический центр Genotek.
Как же мало известно о генах! Первый раз я остро ощутила это, находясь на практике в лаборатории медицинской генетики Харбинского медицинского университета. Исследовательская группа, где я проходила стажировку, занималась изучением онкогена Sei-1, который индуцирует образование двухминутных хромосом (DM), что способствует развитию онкогенеза. Однако механизм образования онкогена Sei-1 остается неизвестным до сих пор. А ведь различные мутации генов являются причиной возникновения и других опасных заболеваний человека, помимо рака. Итак, в данной статье мы изложим некоторые соображения о том, почему мы все еще многое не знаем о генах, а также сформулируем наше мнение о том, сколько генов у человека.
В 1977 году Фредерик Сэнгер впервые разработал метод секвенирования ДНК [1], основанный на терминации ДНК-полимеразной реакции с помощью дидезоксинуклеотидов, за что в 1980 году был удостоен Нобелевской премии в области химии. В этом же году Нобелевскую премию получили Максам и Гилберт, которые предложили метод секвенирования ДНК путем химической деградации. В 1985 году была выявлена первая полная последовательность ДНК бактерии (Haemophilus influenzae), в 1996 году получен первый геном эукариотической клетки (дрожжи Saccharomyces ceravisiae), а в 1998 году расшифрован геном дождевого червя (Caenorhabditis elegans). Завершение в 2003 году проекта «Геном человека» привело к публикации полной последовательности человеческого генома. Но «полной» ее можно назвать весьма условно, учитывая, что около 8% не секвенировано и по сей день [2].
Проект «Геном человека» и полный список генов
Выявление полного списка генов необходимо для выяснения молекулярных механизмов возникновения и развития рака, шизофрении [3], деменции, а также многих других заболеваний человека. Секвенирование ДНК, выделенной из тканей больных, позволяет выявлять такие мутации, как нуклеотидные замены, делеции и вставки, ответственные за возникновение этих заболеваний.
Рисунок 1. Арт-проект на выставке «Геном — расшифровка кода жизни» в Национальном музее естественной истории в Вашингтоне
Собственно, ради этого и затевался проект «Геном человека» (Human genome project, HGP), который продолжался с 1990 по 2003 год. Его основной задачей было определение нуклеотидной последовательности ДНК человека и локализации 100 000 человеческих генов (как тогда полагали) [4]. Параллельно с этим планировалось изучить ДНК набора модельных организмов, чтобы получить сравнительную информацию, необходимую для понимания функционирования генома человека. Предполагалось, что информация, полученная в результате HGP, станет настольной книгой для биомедицинской науки в XXI веке [5]. Целями данных исследований являлось получение информации о причинах ряда болезней [6] и, в конечном итоге, разработка способов лечения более чем 4000 генетических заболеваний, которые затрагивают человечество, включая многофакторные, в которых генетическая предрасположенность играет важную роль. Считалось, что результаты секвенирования генома позволят определить локализацию каждого гена и их общее количество. Однако последовавшие за этим события доказали обратное: сегодня существует несколько баз данных генов, которые существенно отличаются друг от друга. Причем число белок-кодирующих генов совпадает, а число генов других типов расходится.
Проект «Протеом человека»
В 2010 году по инициативе Организации по изучению протеома человека (Human proteome organization, HUPO) был начат проект «Протеом человека» (HPP), целью которого является создание полного списка белков вида Homo sapiens [7]. Для этого, во-первых, предполагается идентифицировать и охарактеризовать, по крайней мере, по одному белковому продукту белок-кодирующих генов, их однонуклеотидные полиморфизмы и варианты сплайсинга, а также виды посттрансляционной модификации белков [8]. Во-вторых, данные протеомики, полученные в результате реализации HPP, способствуют, в дополнение к геномным данным, решению различных биомедицинских задач и созданию новых аннотированных баз знаний, таких как neXtProt [9].
В настоящее время neXtProt содержит информацию о 17 487 белках, существование которых экспериментально подтверждено, 1728 белках, подтвержденных на уровне транскриптов, 515-и, определенных на основании гомологии, 76-и предсказанных и 571-м неизвестной природы. Особый интерес вызывают белки, существование которых экспериментально не доказано, хотя данные о том, что они кодируются геномом, существуют. Это так называемые «потерянные» белки, которые составляют примерно 18% всех кодируемых белков. Для выявления и характеристики таких белков создан ресурс MissingProteinPedia [7].
«Протеом человека» является продолжением проекта «Геном человека». Предполагается, что благодаря проекту по изучению протеома мы узнаем точное количество белок-кодирующих генов, что впоследствии позволит понять, сколько всего генов у человека.
Немного о РНК
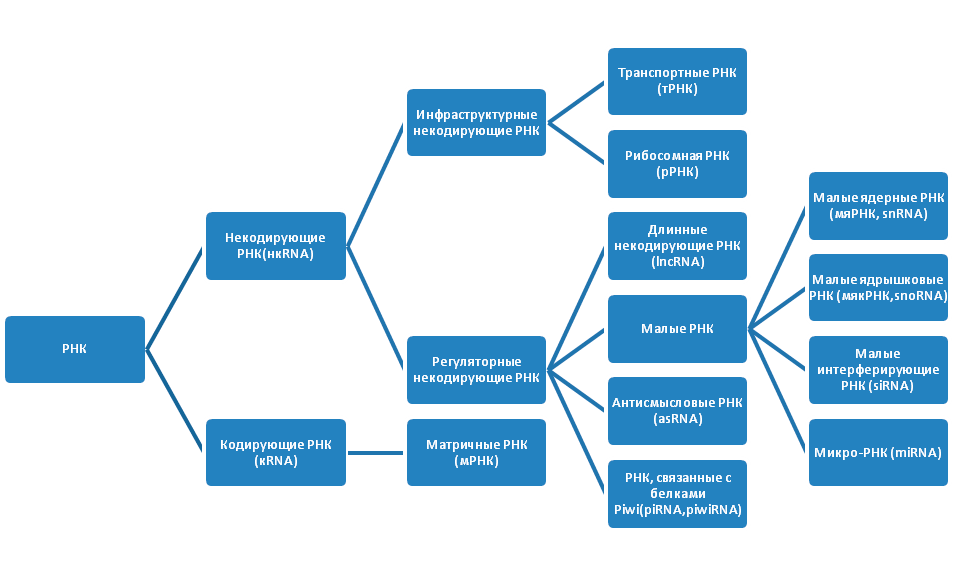
Проект «Геном человека» показал, что молекулы РНК также важны для жизни, как и ДНК. Внутри клеток существует множество РНК (рис. 2). Изначально РНК подразделяются на некодирующие РНК (нкРНК), которые не транслируются в белки, и кодирующие РНК (мРНК), служащие матрицей для синтеза полипептидных цепей белка. Некодирующие РНК имеют более сложную классификацию. Они бывают инфраструктурными и регуляторными. Инфраструктурные РНК представлены рибосомными РНК (рРНК) и транспортными РНК (тРНК). Молекулы рРНК синтезируются в ядрышке и составляют основу рибосомы, а также кодируют белки субъединиц рибосомы. После того, как рРНК полностью собраны, они переходят в цитоплазму, где в качестве ключевых регуляторов трансляции, участвуют в чтении кода мРНК. Последовательность из трех азотистых оснований в мРНК указывает на включение определенной аминокислоты в последовательность белка. Молекулы тРНК, приносят указанные аминокислоты на рибосомы, где синтезируется белок.
Рисунок 2. Виды РНК
рисунок автора статьи
Регуляторные нкРНК очень широко представлены в организме, классифицируются в зависимости от размера и выполняют ряд важных функций (табл. 1).
| Название | Обозначение | Длина | Функции | |
|---|---|---|---|---|
| Длинные некодирующие РНК | днкРНК, lncRNA | 200 нуклеотидов | 1. Регулируют избирательное метилирование ДНК, направляя ДНК-метилтрансферазу 2. Руководят избирательной посадкой репрессорных комплексов polycomb | |
| Малые РНК | Малые ядерные РНК | мяРНК, snRNA | 150 нуклеотидов | 1. Участвуют в сплайсинге 2. Регулируют активность факторов транскрипции 3. Поддерживают целостность теломер [13] |
| Малые ядрышковые РНК | мякРНК, snoRNA | 60–300 нуклеотидов | 1. Участвуют в химической модификации рРНК, тРНК и мяРНК 2. Возможно, участвуют в стабилизации структуры рРНК и защите от действия гидролаз | |
| Малые интерферирующие РНК | миРНК, siRNA | 21–22 нуклеотидов | 1. Осуществляют антивирусную иммунную защиту 2. Подавляют активность собственных генов | |
| Микро-РНК | мкРНК, miRNA | 18–25 нуклеотидов | Подавляют трансляцию путем РНК-интерференции | |
| Антисмысловые РНК [14] | asRNA | 1. Короткие: менее 200 нуклеотидов 2. Длинные: более 200 нуклеотидов | Блокируют трансляцию, образуя гибриды с мРНК | |
| РНК, связанные с белками Piwi | piRNA, piwiRNA | 26–32 нуклеотидов | Их также называют «стражами генома», они подавляют активность мобильных генетических элементов во время эмбриогенеза | |
Проблема терминологии
Прежде чем ответить на вопрос: «Сколько у нас генов?», нужно понять, что же такое ген?
Основное внимание HGP было направлено на белок-кодирующие гены [15]. Однако, как было указано в первоначальном докладе HGP в 2001 году, «тысячи генов человека продуцируют некодирующие РНК (нкРНК), являющиеся их конечным продуктом», хотя на тот момент было известно около 706 генов нкРНК [2]. В своей недавней статье, опубликованной в журнале BMC Biology Стивен Зальцберг (Steven L. Salzberg) дает следующее определение гена [16]:
Ген любой участок хромосомной ДНК, который транскрибируется в функциональную молекулу РНК или сначала транскрибируется в РНК, а затем транслируется в функциональный белок.
Это определение включает как гены некодирующих РНК, так и белок-кодирующие гены, и позволяет определять все варианты альтернативного сплайсинга в одном локусе как варианты одного и того же гена. Это позволяет исключить псевдогены – нефункциональные остатки структурных генов, утратившие способность кодировать белок.
Результаты двух первых исследований свидетельствовали о наличии у человека 31 000 [2] и 26 588 белок-кодирующих генов [17], а в 2004 появилась полная последовательность генома человека [4], и авторы подсчитали, что полный каталог насчитывает 24 000 белок-кодирующих генов. Каталог человеческих генов Ensembl включает 22 287 белок-кодирующих генов и 34 214 транскриптов [18].
Секвенирование нового поколения (NGS)
Появление высокопроизводительных методов параллельного секвенирования (в ходе такого секвенирования миллионы фрагментов ДНК из одного образца секвенируются одновременно) или секвенирования нового (следующего) поколения (next-generation sequencing, NGS) [1] позволило значительно ускорить поиск функциональных участков генома [4]. Биотехнологические компании разработали и коммерциализировали различные платформы для NG-секвенирования, позволяющие секвенировать от 1 млн до десятков млрд коротких последовательностей (ридов, reads) длиной 50–600 нуклеотидов каждая. К наиболее популярным платформам относятся такие, как Illumina и IonTorrent, использующие амплификацию ДНК с помощью ПЦР [19], а также платформы одномолекулярного секвенирования, такие как Helicos Biosciences HeliScope, Pacific Biosciences SMRT (single molecule real-time sequencing), и нанопорового секвенирования Oxford Nanopore, осуществляющие секвенирование в реальном времени и позволяющие прочитывать значительно более длинные риды — до 10–60 тыс. нуклеотидов. Кроме того, изобретение секвенирования РНК (RNA-seq) в 2008 году, которое создавалось для количественного определения экспрессии генов, также способствовало обнаружению транскрибируемых последовательностей, как кодирующих, так и некодирующих РНК [20].
Благодаря NGS, базы данных днкРНК и других генов РНК (таких как микро-РНК) резко выросли за десятилетие, и текущие каталоги генов человека теперь содержат больше генов, кодирующих РНК, чем белки (табл. 2).
| Типы генов | Gencode | Ensembl | RefSeq | CHESS |
|---|---|---|---|---|
| Белок-кодирующие гены | 19 901 | 20 376 | 20 345 | 21 306 |
| Гены длинных некодирующих РНК | 15 779 | 14 720 | 17 712 | 18 484 |
| Антисмысловые РНК | 5501 | — | 28 | 2694 |
| Другие некодирующие РНК | 2213 | 2222 | 13 899 | 4347 |
| Псевдогены | 14 723 | 1740 | 15 952 | — |
| Общее число транскриптов | 203 835 | 203 903 | 154 484 | 323 827 |
Рисунок 3. Последовательность ДНК, получаемая после секвенирования человеческого генома
В ходе секвенирования РНК обнаружилось, что альтернативный сплайсинг, альтернативное инициирование транскрипции и альтернативное прерывание транскрипции проиcходят гораздо чаще, чем полагали, затрагивая до 95% человеческих генов. Следовательно, даже если известно местоположение всех генов, сначала нужно выявить все изоформы этих генов, а также определить, выполняют ли эти изоформы какие-либо функции или они просто представляют собой ошибки сплайсинга.
Базы данных генов человека
Задача по составлению каталога всех генов по-прежнему не решена. Проблема заключается в том, что за последние 15 лет только две исследовательские группы составили список доминантных генов: RefSeq, которая поддерживается Национальным центром биотехнологической информации (NCBI) при Национальных институтах здоровья (NIH), и Ensembl/Gencode, которая поддерживается Европейской молекулярно-биологической лабораторией (EMBL). Однако, несмотря на большой прогресс, сейчас в каталогах различается количество белок-колирующих генов, генов длинных некодирующих РНК, псевдогенов, а также варьирует количество антисмысловых РНК и других некодирующих РНК (табл. 2). Каталоги еще дорабатываются: например, в прошлом году сотни генов, кодирующих белок, были добавлены или удалены из списка Gencode. Эти разногласия объясняют проблему создания полного каталога человеческих генов.
В 2017 году была создана новая база данных генов человека — CHESS. Примечательно, что она включает все белок-кодирующие гены как Gencode, так и RefSeq, так что пользователям CHESS не нужно решать, какую базу данных они предпочитают. Бóльшее количество генов может вызывать больше ошибок, но создатели считают, что бóльший набор окажется полезным при исследовании болезней человека, которые еще не отнесены к генетическим. Набор генов CHESS в настоящее время в версии 2.0 еще не окончательный, и, безусловно, создатели работают над его усовершенствованием.
Таким образом, все еще неизвестно, сколько всего генов у человека. Существует ряд проблем, затрудняющих эту задачу. Например, многие гены (особенно, гены днкРНК), видимо, имеют высокую тканеспецифичность. Из этого следует, что пока ученые подробно не исследуют все типы клеток человека, они не могут быть уверены, что обнаружили все человеческие гены и транскрипты. Безусловно, сегодня знания о человеческих генах стали значительно обширнее, чем в начале проекта «Геном человека», а технологии совершеннее. Это дает надежду на то, что в скором времени мы узнаем точный ответ на поставленный вопрос.