Что меньше молекула воды или молекула кислорода
Из чего состоит все вокруг или что такое молекула?
Каждый раз, когда два атома соединяются вместе, они образуют молекулу. На самом деле все, что нас окружает – да и мы сами – состоит из триллионов различных типов молекул. Понятие молекулы было принято в 1860 году на международном съезде химиков в Карлсруэ. Согласно принятому определению молекула – это наименьшая частица химического вещества, которая обладает всеми его химическими свойствами (растворимость, вкус, способность вступать в соединения и пр). Введение понятия молекулы подтолкнуло развитие физики, химии и других естественных наук. В более общем понимании молекулой называют частицу, образованную из двух или более атомов, соединенных между собой ковалентными связями.
Молекула воды содержит 1 атом кислорода и 2 атома водорода
Атом – мельчайшая частица вещества, которая обладает всеми его физическими свойствами (цвет, твердость, плотность и пр.)
Когда атомы различных типов элементов соединяются вместе, они образуют молекулы, называемые соединениями. Так, вода состоит из сложных молекул, состоящих из 2 атомов водорода и 1 атома кислорода. Вот почему она называется H2O: у молекулы воды всегда будет в 2 раза больше атомов водорода, чем атомов кислорода. Существует чуть более 100 типов атомов, но типов различных веществ миллионы. Причина такого неравенства кроется в том, что они состоят из различных типов молекул.
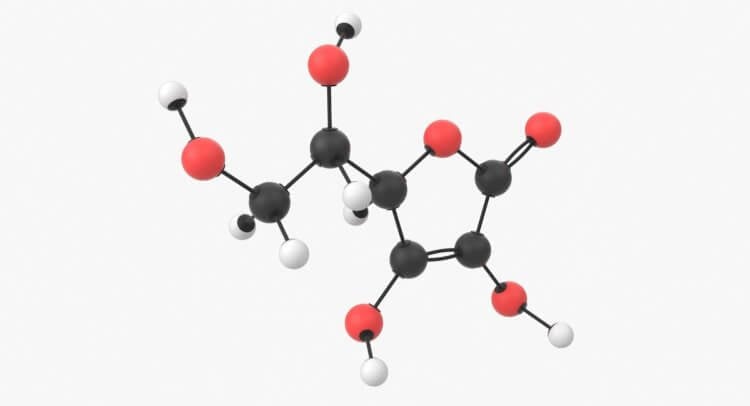
Важно понимать, что молекулы состоят не только из различных типов атомов, но и из различных соотношений. Как и в приведенном выше примере с водой, молекула воды состоит из двух атома водорода и одного атома кислорода, что записывается как H2O. Другими примерами являются углекислый газ (C02), аммиак (NH3) и сахар или глюкоза (C6H12O6). Некоторые молекулярные формулы могут получиться довольно длинными и сложными. Давайте посмотрим на молекулу сахара:
Чтобы она получилась, нужны определенные атомы в определенном количестве. Но молекулы могут быть гораздо больше. Одна молекула витамина С состоит из 20 атомов (6 атомов углерода, 8 атомов водорода и 6 атомов кислорода – C6H8O6). Если взять эти 20 атомов витамина С и смешать, соединяя их вместе в другом порядке, то получится совершенно другая молекула, которая не только выглядит по-другому, но и действует иначе.
Молекула витамина С выглядит так
Некоторые молекулы, особенно некоторые белки, содержат сотни или даже тысячи атомов, которые соединяются вместе в цепи, которые могут достигать значительной длины. Жидкости, содержащие такие молекулы, иногда ведут себя странно. Например, жидкость может продолжать вытекать из колбы, из которой была вылита некоторая ее часть, даже после того, как колба будет возвращена в вертикальное положение.
Факты о молекулах
Чтобы всегда быть в курсе последних научных открытий, подписывайтесь на наш новостной канал в Telegram
Химические связи
Молекулы и соединения удерживаются вместе силами, называемыми химическими связями. Существует четыре типа химических связей, которые удерживают большинство соединений вместе: ковалентные связи, ионные связи, водородные и металлические, однако в качестве основных выделяют ковалентные и ионные, так как они связаны с электронами. Как известно, электроны вращаются вокруг атомов в оболочках. Эти оболочки хотят быть «полными» электронов. Когда они не заполнены, то будут пытаться соединиться с другими атомами, чтобы получить нужное количество электронов и заполнить их оболочки.
Ковалентные связи делят электроны между атомами. Это происходит, когда получается, что атомы делятся своими электронами, чтобы заполнить свои внешние оболочки. В свою очередь ионные связи образуются, когда один электрон передается другому. Это происходит, когда один атом отдает электрон другому, чтобы сформировать баланс и, следовательно, молекулу или соединение.
Еще больше увлекательных статей о том, как ученые дробят реальность на атомы, читайте на нашем канале в Яндекс.Дзен. Там выходят статьи, которых нет на сайте!
Знания о свойствах и строении молекул легли в основу современной науки и нашего понимания Вселенной
Немаловажным также является тот факт, что молекулы всегда находятся в движении. В твердых телах и жидкостях они находятся очень близко друг к другу, а их движение можно сравнить с быстрой вибрацией. В жидкостях молекулы могут свободно перемещаться между собой, как бы скользя. В газе плотность молекул обычно меньше, чем в жидкости или твердом теле того же химического соединения, а потому молекулы движутся даже более свободно, чем в жидкости. Для конкретного соединения в данном состоянии (твердом, жидком или газообразном) скорость молекулярного движения возрастает с увеличением абсолютной температуры.
dymontiger
Интересное в сети!
Курьезы, юмор, а иногда и жесть, все это вы найдете здесь;)
Все разнообразие нашего мира построено из атомов и молекул. Удивительно, как проявления форм жизни образовались лишь на основе протонов, нейтронов и электронов. Элементарная основа позволяет каждому веществу и организму выполнять свою функцию. Так из семи нот пишется музыка разных направлений, разных стилей. Мы собрали 10 самых интересных фактов об атомах и молекулах.
Самый легкий из атомов – атом водорода
В периодической таблице химических элементов водород стоит на первом месте. Его ядро состоит лишь из одного протона, вокруг которого вращается единственный электрон. Простейшее строение определяет минимальную массу, которую может иметь атом – 1,008 а.е.м. или 1,7х10-24 г.
На Земле водород существует в виде соединений с другими веществами или образует двухатомную молекулу Н2. Если считать в массовом отношении, на его долю приходится 1% земной коры. Если перевести массу в количество атомов, то содержание водорода окажется более внушительным – 17%. Этот показатель ставит элемент на второе место после кислорода (52%).
Во Вселенной водород составляет 88,6% от общей доли атомов, находящихся в космосе в виде звездного вещества и космической пыли.
Главной молекулой живой природы является молекула ДНК
В молекуле ДНК сосредоточена информация о строении каждой клетки живого организма, словно это проектное бюро города, где собраны подробные планы всех зданий. Внешне она напоминает перевитую веревочную лестницу, состоящую из двух нитей и соединенную водородными связями. ДНК вирусов может представлять одну цепочку.
Информация зашифрована в генах, то есть участках молекулы. Ген представляет собой определенную последовательность нуклеотидов, способных передать код для построения белков и РНК (информационных, транспортных, рибосомных, матричных).
Спираль ДНК человека, если ее вытянуть, протянется почти на 2 м. Это тем более удивительно, что она умещается в ядре размером меньше микрометра. Свернуться в компактную хромосому молекуле помогают нуклеосомы. На них ДНК наматывается, как на катушку.
Пыль – это частица, состоящая из квадриллиона атомов
Пылью называют твердые минеральные или органические частицы размером не более 0,05 мм. Природа образования может быть как естественной, так и связанной с деятельностью человека (антропогенной). В воздух поднимаются вулканический пепел, морская соль, сухая почва, продукты горения после пожаров, пыльца растений. Человек способствует загрязнению воздуха продуктами отопления и горных разработок, выхлопами автотранспорта, удобрениями. Вспашка земли и оголение почвы выкосами травы опасны выветриванием и переносом верхнего слоя грунта ветром.
Если сравнивать твердую взвесь с газообразными загрязнителями воздуха, то последние присутствуют в виде отдельных молекул. Пыль же в каждой частице содержит огромное число молекул и еще большее число атомов.
Атом может иметь электрический заряд
В составе атома электроны несут отрицательный заряд, протоны – положительный. Нейтроны не имеют заряда, то есть нейтральны. Когда количество протонов равно количеству электронов, заряд атома равен нулю. В случае, если электронов больше или меньше, чем протонов, у атома появляется заряд. Он становится ионом.
Ядро, состоящее из нейтронов и протонов, обладает ощутимой массой. Нужно определенное количество энергии, чтобы заставить его терять протоны. Электроны, которые вращаются вокруг него, значительно легче могут перемещаться от одного атома к другому. Добавление электронов приводит к образованию отрицательного заряда, потеря частиц – положительного. Атомы с положительным зарядом называют катионами, атомы с избытком электронов становятся анионами.
Самый тяжелый из атомов – атом урана
Из природных элементов атом урана имеет самую большую массу – 238,0289 а.е.м. В природе находится в основном в виде изотопа U-238. Атом с его 92 протонами чрезвычайно перегружен, при любой возможности выбрасывает протоны и нейтроны с огромной скоростью.
Открыл элемент германский химик Мартин Клапрот в 1789 году при анализе отработанной руды после добычи серебра. «Странное вещество», похожее на металл было диоксидом урана, но выяснилось это только через 50 лет. Клапрот назвал находку в честь далекой планеты, открытой к этому времени Гершелем.
В конце 19 века во Франции Анри Беккерель обнаружил радиоактивность урана, то есть способность терять частицы. Распад может иметь 14 циклов. Уран превращается в радий, радон и другие элементы, образуя на последней стадии свинец.
Слово «атом» происходит из древнегреческого языка и означает «неделимый»
Еще в Древней Греции философ и математик Демокрит предположил, что окружающее состоит из мельчайших частичек. Отсюда произошел термин «атом» или «atomos». Однако подтверждение теория получила только в результате работы ученых в последние 150 лет и с помощью изобретенного микроскопа.
Первое исследование провел англичанин Джон Дальтон на рубеже 18-19 веков. Он установил, что химические элементы вступают в реакции в строго определенном соотношении (закон кратных отношений).
Сейчас мы знаем, что атом представляет собой наименьшую частицу химического элемента и не всегда является неделимым. В состав атома входит ядро с протонами и нейтронами или просто нуклонами от латинского слова «nucleus» – ядро. Снаружи вокруг атома расположено электронное облако.
Стекло не является твердым телом
Твердость вещества – характеристика, основанная на прочности химических связей между атомами и молекулами. В жидкости частицы могут перемещаться относительно друг друга. В твердых телах они лишены такой возможности.
При производстве стекла молекулы кремния, обычно принимающие структуру кристаллической решетки, не успевают занят положенное им место. Стекло быстро остывает и частицы остаются перемешанными хаотично. Такое вещество называют аморфным, однако все же оно твердое.
Вязкость стекла сопоставима с вязкостью свинца, но ведь свинец никто не называет жидкостью. Бытует мнение, что со временем оконные стекла «стекают» вниз. В пример ставят витражи в средневековых храмах. Следует уточнить, что утолщения в их основании появились не с течением времени, а были изначально. Причина кроется в несовершенстве технологии производства.
Молекула меньше яблока во столько же раз, во сколько яблоко меньше Земли
Чтобы представить видимые и невидимые параметры окружающего мира, представим все молекулы одного кубического сантиметра воздуха в виде кирпичей. Их количества хватило бы для покрытия поверхности планеты на высоту 40-этажного дома.
Размеры молекул и атомов настолько малы, что в решении задач молекулярной физики используют относительные величины. Установить их удалось лишь с изобретением электронного микроскопа. Средний диаметр атома и простейшей молекулы составляет порядка 10-10 м. Так, размер молекулы белка – 43х10-10 м. Крупные молекулы достигают 10-7 м.
В ионный микроскоп можно разглядеть строение кристалла и даже определить межатомные расстояния.
Ученые смогли охладить молекулы монофторида стронция практически до абсолютного нуля
Выбор пал на монофторид стронция (SrF) неслучайно. Принцип охлаждения атомов основан на периодическом повторении поглощения и испускания фотонов под воздействием лазера. Таким образом атом теряет кинетическую энергию. Молекулы не настолько чувствительны. Мешает колебательная и вращательная энергия межатомных связей. У фторида стронция эти явления минимальны.
Группа ученых Йельского университета во главе с Д. Демиллем добилась охлаждения молекулы до 300 мкК (0,0003 К). За счет подобранной длины волны лазер погасил вращательные межатомные движения. В дальнейшем молекулы вели себя аналогично атому.
Практически такое достижение в перспективе можно использовать в квантовых компьютерах.
Скорость движения молекул воды может достигать 650 м/с
Молекулы воды находятся в постоянном тепловом движении. Они колеблются с большой частотой (одно колебание за 10-12 … 10-13 с) возле определенного положения, изредка прыгая на освободившееся соседнее место. Скорость движения при этом может приближаться к 600-650 м/с.
И все же молекулы не разлетаются, остаются жидкостью. Происходит это за счет водородных связей. В молекуле H2O пары электронов смещены в сторону кислорода. Водород, оставшийся практически без электрона, представляет собой положительно заряженное ядро. В результате протон водорода притягивает соседние атомы кислорода, образуя прочную межмолекулярную связь.
Благодаря такому сцеплению вода в условиях Земли принимает в основном жидкое состояние, а не кипит как аналогичные гидриды (серы, селена) при –80°С. Водородные связи определяют физические и химические свойства воды, на которых основана жизнь на нашей планете.
©
O2 и H2O
Когда вода переходит в газообразное состояние, она подымаеться вверх, так как масса молекулы воды меньше массы молекулы воздуха. Тут все понятно и логично.
Вопрос: почему вода (вещество) не летает?
Далее идет просто размышление на тему.
Ответ: Плотность строения.
Получается, что гравитация влияeт не на массу атома, или отдельной молекулы, а на взаимодействие молекул между собой. Другими словами, гравитация влияет не на само вещество, а на его состояние.
Это опровергает ускорение свободного падения, в котором говорится (или говорилось?) что все тела (с идеинтичной поверхностью и формой, но разной массой) падают на землю с одинаковой скоростью.
Вопрос: Почему по отдельности молекулы воды взлетают, а когда соединяются вместе, падают вниз?
Да пока до дома ехал, сам догадался. Образуется обьект с общей массой. Но тогда закон ускорения свободного падения опровергается, разве нет?
Держатся вместе и боятся улететь. Вот и всё.
А если они уже улетели, и потом нашли друг друга, почему падают?
а электронов сколько в каждой из молекул?
_Garik_, Даю подсказку- ВОДОРОДНАЯ СВЯЗЬ
пудель Смерти, водородная связь ну тут просто не причем.
_Garik_,
Я к тому, что общая масса соединенных молекул будет существенной и будет притягиваться к земле.
А еще действие магнитного поля земли, диа и параганэтизм повлият не могут?
EvilMaster
Все в этом мире связано. Мы являемся его частью, он являеться частью нас. Я считаю, что понимание внешнего мира приводит к более глубокому пониманию внутреннего.
Agent, ты обещания держать неумеешь. Будь хорошим, делай то, что обещал.
водородная связь ну тут просто не причем.
пудель Смерти, спс за подсказку.
А еще действие магнитного поля земли, диа и параганэтизм повлият не могут?
Образуеться водородная связь, что считаеться единым обьектом, соответственнно, масса молекул складываеться, что увиличивает массу обьекта относительно молекул воздуха. Соответственно, он начинает вытеснять молекулы воздуха, падая при этом вниз. Это значит, что гравитация действует сильней на обьект с большем массой. Это опровергает второй закон ньютона.
Все тела на поверхности Земли испытывают действие силы тяжести, направленной к центру нашей планеты. По закону всемирного тяготения величина этой силы F пропорциональная массе тела:
где G — гравитационная постоянная, M — масса Земли, R — радиус Земли, m — масса тела. Однако по второму закону Ньютона ускорение a, приобретаемое телом под действием силы тяжести, обратно пропорционально его массе:
Подставляя в это уравнение приведенное выше выражение для силы тяготения, обнаруживаем, что масса тела m сокращается, а значит, ускорение, приобретаемое телом под действием силы тяжести, не зависит от массы тела. Это ускорение называют ускорением свободного падения и обозначают буквой g:
Соответственно, сила тяжести на поверхности Земли вычисляется по формуле:
Если подставить в приведенную выше формул для g средние параметры Земли, то получится величина ускорения свободного падения:
Однако в технических расчетах обычно принимают
Точное значение величины g на поверхности Земли меняется по трем причинам:
* Форма Земли (геоид) отличается от сферической, из-за чего на полюсах мы находимся примерно на 21 км ближе к центру Земли, чем на экваторе. Соответственно, величина R2 (в знаменателе) на полюсах на 0,7% больше, чем на экваторе. Из-за этого значение g на полюсах увеличивается на 0,07 м/с2.
* Тела, находящиеся на экваторе, из-за вращения Земли испывают центробежное ускорение, равное 0,03 м/с2.
* Неоднородности вещества, слагающего земную кору и верхнюю мантию, приводят к небольшим локальным вариациям величины g, которые называют гравитационными аномалиями.
Первые два фактора приводят к тому, что ускорение свободного падения на пути от экватора к полюсу возрастает более чем на 1%. Настолько возрастет при таком путешествии, скажем, вес (не масса!) килограмма золота.
Нет, не зависит абсолютно от массы. Земля действует на любое тело с одинаковой силой, как и это тело действует на землю.
Наверное тоже в плотности дело. И водородной связи тогда уж. Молекулы принадлежат общей паре, и масса становится больше.
Поставщик загробных мук
и гидрогенные связи кстати тоже, но меньше, гораздо меньше, но влияют
Гравитация взаимодействует с весом ядер отдельных молекул, иначе бы молекулы воды не подымались «в воздух».
Если гравитация взаимодействует с плотностью вещества, то, если взать две сферы одинакового размера, одну изо льда (Плотность: 0,917 г/см³), другую из свинца (Плотность: 11,3415[1] г/см³), то гравитационное воздействие должно быть больше на сферу из свинца. Что не совсем опровергает второй закон ньютона, а делает его бессмысленным. Или делает «теорию плотности» бесмысленной.
В добавок, если дело в плотности, то соединение молекул между собой должно порождать что-то новое, что довольно значительно начинает взаимодействовать с земной гравитацией. Что это?
Водородная звязь сюда не подходит:
Энергия водородной связи значительно меньше энергии обычной ковалентной связи (не превышает 40 кДж/моль). Однако этой энергии достаточно, чтобы вызвать ассоциацию молекул, то есть их объединение в димеры или полимеры. Именно ассоциация молекул служит причиной аномально высоких температур плавления и кипения таких веществ, как фтороводород, вода, аммиак. Водородная связь в значительной мере определяет свойства и таких биологически важных веществ, как белки и нуклеиновые кислоты.
[править] Факторы, влияющие на прочность водородной связи
Прочность водородной связи (энтальпия образования комплекса) зависит от полярности комплекса и колеблется от
6 кДж/моль для комплексов молекул галогеноводородов с инертными газами до 160 кДж/моль для ион-молекулярных комплексов (AHB)±; так, для комплекса (H2O•H•OH2)+ образованного H2O и H3O+ — 132 кДж/моль в газовой фазе.
[править] Влияние водородной связи на физические свойства
Связь этого типа, хотя и слабее ионной и ковалентной связей, тем не менее играет очень важную роль во внутри- и межмолекулярных взаимодействиях. В частности, элементы вторичной структуры (например, α-спирали, β-складки) в молекулах белков стабилизированы водородными связями. Водородные связи во многом обусловливают физические свойства воды и многих органических жидкостей (спирты, карбоновые кислоты, амиды карбоновых кислот, сложные эфиры).
Если гравитация взаимодействует с плотностью вещества, то, если взать две сферы одинакового размера, одну изо льда (Плотность: 0,917 г/см³), другую из свинца (Плотность: 11,3415[1] г/см³), то гравитационное воздействие должно быть больше на сферу из свинца. Что не совсем опровергает второй закон ньютона, а делает его бессмысленным. Или делает «теорию плотности» бесмысленной.
Если за плотность брать количество молекул а не вес адра, тогда вопрос на половину решен, если предположить, что количество молекул в обоих сферах одинаково.
Но, тогда перестает играть масса ядра. Разве молекула свинца не потонет в воде?
Получается, что гравитация воздействует как на массу ядра, так и на состояние вешества. Причем, можно сказать, по разному для разного вещества. Что если жидкий кислород поместить в воду. По идее, если бы он не перешел в газообразное состояние, он должен утонуть изза большей плотности (1,141 г/см³).
Значит, гравитация не влияет одинаково на все вешества в одинаковых состояниях. Либо определения состояний вещества не совсем точные. Она влияет по разному на одни и те же вешества в разных состояниях?
В газообразном состоянии вода легче воздуха. В жиждком состоянии, вода опять легче чем кислород, в жидком состоянии. И все бы ничего, но, как только молекулы воздуха, попавшие в воду, находят друг друга, образуются пузыри, которые стремительно подымаются вверх.
Как так получается. Считается, что кислород, которым мы все дышим, пребывает в газообразном состоянии.
Вики
В современной физике выделяют следующие агрегатные состояния: твёрдое тело, жидкость, газ, плазма
Молекулы кислорода тяжелей, оседают на дне бассеина (и мне, когда я лежу в ванне), собираются вместе в пузырь и вода выталкивает их наружу. Вроде молекулы в пузыре прибывают в состоянии газа (сами по себе), но, при этом, они образовывают нечто целое, что не образовывают молекулы воды в газообразном состоянии.
Так можно обьяснить кипение воды. Тот момент, когда она начинает кипеть. Вода нагревается возле дна сосуда, соответвтвенно меняется ее состояние, она становится менее стабильной, нарушается структура, что позволает поиманым молекулам кислорода быстрей упасть на дно и собраться вместе. Они тут же становятся легче воды и подымаются. Если вода только начинает закипать, то теплый пузырь кислорода остывает, что меняет состоание вещества о он исчезает, недолетев до поверхности.
Может газообразное состояние кислорода нельзя сравнивать с газообразным состоянием воды? Значит существует некое промежуточное состояние.
Вспоминаю про кварки и глюонные облака, которые ими порождаются. Такое ощущение, что пузыри воздуха в воде, некая аналогия глюонным облакам.
Тогда может получится, что гравитация действует на вещества по разному.
Vita sine libertate nihil est
Может газообразное состояние кислорода нельзя сравнивать с газообразным состоянием воды? Значит существует некое промежуточное состояние.
Тогда может получится, что гравитация действует на вещества по разному.
Между молекулами должно образовываться какое-то «поле» (электромагнитное? гравитационное?), которое взаимодействует с гравитацией Земли или чем-то еще. Так оно и есть, но на мой взгляд этому не придается достаточно значения.
Почему это поле существует:
Когда отдельная молекула воды находится среди молекул кислорода, она подымается вверх. Засчет гравитации?
Когда молекулы воды соединяються они падают вниз. Опять гравитация?
Когда отдельная молекула воздуха находится в воде (среди молекул воды), она падает вниз. Гравитация?
Когда молекулы воздуха объеденяются в воде (расстояние сокращается до определенного и они начинают взаимодействовать), то пузыри воздуха стремяться вверх. Снова гравитация.
Соответственно, при сближении образуется некое поле, которое делает очень вущественную разницу на взаимодействие вещества и гравитационного поля земли. Я мало знаю про магнитное поле. Оно может притягивать воздух вверх?
Наукой занимаются в институтах
На форумах, конечно, выносят мозг, но не настолько же
Но, тогда эти пузыри должны вакумными. А значит они не должны стремится на поверхность. Значит образование пузырей не такой уж простой процесс. По идее, если разогреть воду до 100 градусов не только снизу, то пузыри должны были бы образовываться просто внутри воды, где-нить по середине. Как провести такой эксперемент, я незнаю. Но, в нашем случае они образуються на дне сосуда. Соответственно это должен быть кислород.
Интересно, как счас в школе обьясняется процесс кипения воды? Вообще, существует дословное описание процесса, а именно образование пузырей? Посмотрим.
http://fizikaftf5.student.nov.ru/kipenie.htm
Через некоторое время мы увидим, как дно и стенки сосуда покроются пузырьками. Они образуются в результате расширения мельчайших пузырьков воздуха, существующих в углублениях и микротрещинах не полностью смачиваемых стенок сосуда.
Рассмотрим пузырек, возникающий около горячего дна (демонстрация №1). Увеличиваясь в объеме, пузырек увеличивает площадь своего соприкосновения с еще недостаточно прогревшейся водой. В результате воздух и пар внутри пузырька охлаждаются, их давление уменьшается, и тяжесть слоя воды «захлопывает» пузырек. В этот момент закипающая вода издает характерный шум. Он возникает из-за ударов воды о дно сосуда там, где захлопываются пузырьки.
По мере роста температуры интенсивность испарения воды внутрь этих пузырьков возрастает. Поэтому количество водяного пара, а вместе с ним и давление внутри пузырьков постепенно увеличиваются. При приближении температуры нижних слоев воды к 100 °С давление внутри пузырьков сравнивается с давлением, существующим вокруг них, после чего пузырьки начинают расширяться. С увеличением объема пузырьков растет и действующая на них выталкивающая (архимедова) сила. Под действием этой силы наиболее крупные пузырьки отрываются от стенок сосуда и поднимаются вверх. Если верхние слои воды еще не успели нагреться до 100 °С, то в такой (более холодной) воде часть водяного пара внутри пузырьков конденсируется и уходит в воду; пузырьки при этом сокращаются в размерах, и сила тяжести заставляет их снова опускаться вниз. Здесь они опять увеличиваются и вновь начинают всплывать вверх (демонстрация №2).
Попеременное увеличение и уменьшение пузырьков внутри воды сопровождается возникновением в ней характерных звуковых волн: закипающая вода «шумит».
Когда вся вода прогреется до 100 °С, поднявшиеся наверх пузырьки уже не сокращаются в размерах, а лопаются на поверхности воды, выбрасывая пар наружу. Возникает характерное бульканье — вода кипит (демонстрация №3).
Кипением называется интенсивное парообразование, при котором внутри жидкости растут и поднимаются вверх пузырьки пара. Оно начинается после того, как давление внутри пузырьков сравнивается с давлением в. окружающей жидкости.
http://otvet.mail.ru/question/32350634/
При медленном пузырьковом кипении в жидкости (а точнее, как правило на стенках или на дне сосуда) появляются пузырьки, наполненные паром. За счёт интенсивного испарения жидкости внутрь пузырьков, они растут, всплывают, и пар высвобождается в паровую фазу над жидкостью.
http://www.edu.yar.ru/russian/projects/socnav/prep/phis001/par.html
По мере нагревания сосуда с водой дно и стенки сосуда будут покрываться пузырьками, в которых находятся воздух и пары воды. С увеличением температуры объем пузырьков увеличивается в такой мере, что сумма давления воздуха и пара внутри пузырька всегда равна внешнему давлению. При дальшенйшем увеличении объема пузырька выталкивающая сила заставляет его подниматься вверх.
Архимедова сила. Но она же выталкивает пузыри иненно вверх. Соответственно, либо их что-то притягивает вверху, либо толкает снизу. Не понимаю Архимедову силу пока еще.
http://www.izbrannoe.ru/41750.html
Кроме того, пузырьки воздуха, которые застревают в нанолесу являются катализаторами кипения.
http://works.tarefer.ru/89/100339/index.html
На твердой поверхности силы сцепления между молекулами жидкости и твердого тела меньше нежели между молекулами
жидкости. Вероятность образования пузырька на поверхности больше чем в жидкости.
В некоторых случаях говориться что пузырьки образуються за счет пойманых поверхностью сосуда молекул воздуха. В последнем случае говориться что образование пузырьков возможно просто внутри жидкости.
В одном случае, по идее, если поверхность будет стирильной без поиманых пузырьков, вода кипеть не должна, варней недолжны образовываться пузыри.В добавок, пузыри никогда не кончаются, заметили?
В другом случае, пузыри должны образовываться как на дне сосуда, так и просто внутри жидкоски, хотябы рядом с дном. Но они же всегда образовываються на дне. В добавок, в такой ситуации, говорить про пойманые молекулы кислорода микротрещинами сосуда, просто не имеет смысла.
Вот такая вот физика. Выглядит очень неопределенно.
Надо переработать инфу.
Наукой занимаются в институтах
На форумах, конечно, выносят мозг, но не настолько же
Лучше бы обьяснила феномен.
Смысл этого поста не вынести мозг, а наоборот, навести порядок. На самом деле, я был бы очень признателен человеку, кто смог бы это обьяснить.
всё не читал, может уже говорилось. но.
закон архимеда