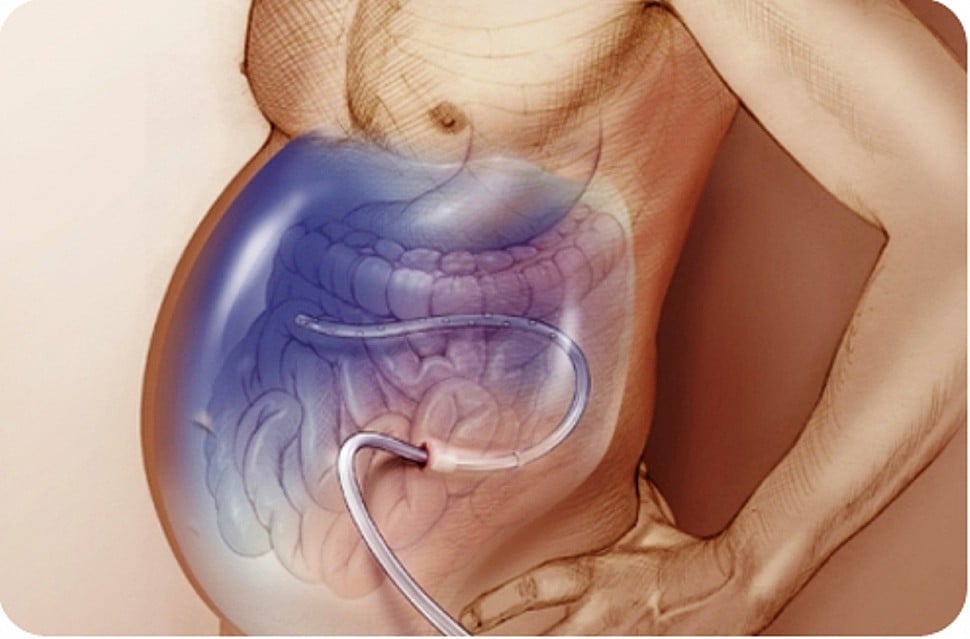
Что можно пить при асците
Асцит при онкологической патологии
Асцит (скопление жидкости в брюшной полости) определяют у 50% больных на ранних стадиях онкологических заболеваний и почти у всех пациентов, у которых раковый процесс находится на последней стадии.
Клиника онкологии Юсуповской больницы оснащена новейшей диагностической аппаратурой ведущих мировых производителей, с помощью которой онкологи выявляют ранние стадии онкологической патологии. Химиотерапевты, радиологи, онкологи проводят лечение пациентов с асцитом в соответствии с международными стандартами оказания медицинской помощи. В то же время врачи индивидуально подходят к выбору метода лечения каждого пациента.
Причины развития
Асцит является грозным осложнением рака желудка и толстой кишки, колоректального рака, злокачественных опухолей поджелудочной железы, онкологической патологии молочных желез, яичников и матки. При накоплении в брюшной полости большого объёма жидкости повышается внутрибрюшное давление, диафрагма смещается в грудную полость. Это приводит к нарушению работы сердца, лёгких. Происходит нарушение кровообращения по сосудам.
При наличии асцита организм пациента теряет большое количество белка. Нарушается обмен веществ, развивается сердечная недостаточность и другие расстройства равновесия внутренней среды организма, которые ухудшают течение основного заболевания.
В брюшной полости здорового человека всегда есть небольшое количество жидкости. Она предотвращает склеивание между собой листков брюшины. Выработанная внутрибрюшная жидкость обратно всасывается брюшиной.
При развитии онкологических заболеваний происходит нарушение нормального функционирования организма. Происходит сбой секреторной, резорбтивной и барьерной функции листков брюшины. При этом может наблюдаться либо избыточная продукция жидкости, либо нарушение процессов ее всасывания. В результате в брюшной полости накапливается большой объём экссудата. Он может достигать двадцати литров.
Основная причина поражения брюшины злокачественными клетками – её тесное соприкосновение с органами, которые поражены раковой опухолью. Асцит при наличии онкологической патологии развивается под воздействием следующих факторов:
Причиной асцита может быть химиотерапия. Скопление жидкости в брюшине происходит вследствие раковой интоксикации. Если печень поражается первичной раковой опухолью, метастазами злокачественных клеток из новообразований иной локализации, нарушается отток крови по её венозной системе, развивается портальная гипертензия – повышение давления внутри воротной вены. Просвет венозных сосудов увеличивается, из них пропотевает плазма и накапливается в брюшной полости.
Причиной асцита может быть канцероматоз брюшины. При наличии раковой опухоли органов брюшной полости на париетальном и висцеральном листах брюшины оседают атипичные клетки. Они блокируют резорбтивную функцию, в результате чего лимфатические сосуды плохо справляются с предназначенной нагрузкой, происходит нарушение оттока лимфы. Свободная жидкость постепенно накапливается в брюшной полости. Таков механизм развития канцероматозного асцита.
Стадии тяжести
Выделяют три стадии водянки брюшной полости в зависимости от количества скопившейся жидкости:
Симптомы
Основное проявление асцита – значительное увеличение размеров и патологическое вздутие живота. Признаки водянки брюшной полости могут нарастать стремительно или в течение нескольких месяцев. Асцит проявляется следующими клиническими симптомами:
Визуально у больного увеличивается живот, в горизонтальном положении он свисает и начинает «расплываться» по бокам. Пупок постепенно все более выпячивается, а на растянутых кожных покровах просматриваются кровеносные сосуды. По мере развития асцита пациенту становится тяжело наклоняться, появляется одышка.
Врачи клиники онкологии проводят оценку клинических проявлений заболевания и проводят дифференциальную диагностику рака с другими болезнями, проявлением которых является асцит.
Диагностика
Асцит врачи выявляют во время осмотра пациента. Онкологи Юсуповской больницы проводят комплексное обследование пациентов, которое позволяет выявить причину скопления жидкости в брюшной полости. Один из наиболее достоверных методов диагностики – ультразвуковое исследование. Во время процедуры врач не только чётко видит жидкость, но и высчитывает её объем.
При асците онкологи обязательно выполняют лапароцентез. После прокола передней брюшной стенки врач аспирирует жидкость из брюшной полости и отправляет в лабораторию для исследования. С помощью компьютерной томографии рентгенологии определяют наличие злокачественных новообразований в печени, которые вызывают портальную гипертензию.
Магнитно-резонансная томография дает возможность определить количество скопившейся жидкости и ее локализацию.
Лечение
Медикаментозная терапия асцита не проводится из-за низкой эффективности. Антагонисты альдостерона и диуретики нормализуют водно-солевой обмен и предотвращают избыточную секрецию перитонеальной жидкости. Онкологи Юсуповской больницы на поздних стадиях онкологического заболевания пациентам с асцитом предлагают выполнить паллиативную операцию:
Врачи клиники онкологии при асците проводят традиционную или внутриполостную химиотерапию – после удаления жидкости в брюшную полость вводят химиопрепарат. Для удаления жидкости выполняют лапароцентез. Процедуру не проводят при наличии следующих противопоказаний:
Лапароцентез назначают в случаях, когда прием диуретиков не приводит к положительному результату. Также процедура показана при резистентном асците.
Лапароцентез проводится в несколько этапов с применением местной анестезии:
Методом лапароцентеза можно вывести из организма больного до 10-ти литров жидкости. При этом может потребоваться введение альбуминов и других препаратов, чтобы предотвратить развитие почечной недостаточности.
При необходимости в брюшной полости могут быть установлены временные катетеры, по которым постепенно будет выводиться избыточная жидкость. Следует учесть, что применение катетеров может привести к снижению артериального давления и образованию спаек.
Выделяют также противопоказания к проведению лапароцентеза. Среди них:
Мочегонные средства назначают пациентам с развивающимся асцитом при раковых заболеваниях длительным курсом. Эффективность оказывают такие препараты, как «Фуросемид», «Диакарб» и «Верошпирон».
При приеме мочегонных средств в обязательном порядке назначают также препараты, содержащие калий. В противном случае высока вероятность развития нарушений водно-электролитного обмена.
Диетическое питание прежде всего подразумевает уменьшение количества потребляемой соли, задерживающей жидкость в организме. Также важно ограничить количество употребляемой жидкости. Рекомендуется включать в рацион больше продуктов, содержащих калий.
Пациентам после удаления жидкости из брюшной полости обеспечивают сбалансированное и калорийное питание. Это позволяет обеспечить потребность организма в белках, углеводах, витаминах и минералах. Потребление жиров сокращают.
Асцит неракового происхождения
Асцит – следствие различных нарушений, которые происходят в организме. Тактика лечения зависит от патологического процесса, который вызвал скопление жидкости в брюшной полости:
Для выведения жидкости из организма пациентам с асцитом назначают мочегонные препараты. Основной метод устранения асцита – удаление скопившейся жидкости посредством прокола брюшной стенки с последующей установкой дренажа. При устойчивом асците проводят реинфузию перитонеальной жидкости после её фильтрации. Перитонеовенозный шунт при асците брюшной полости обеспечивает поступление жидкости в общий кровоток. Для этого хирурги формируют конструкцию с клапаном, при помощи которой жидкость из брюшной полости во время вдоха поступает в систему верхней полой вены.
Оментогепатофренопексию при асците брюшной полости выполняют с целью снижения давления в венозной системе. Хирург подшивает сальник к диафрагме и печени. После чего во время дыхательных движений вены разгружаются от крови. В итоге уменьшается выход жидкости через стенку сосудов в брюшную полость. В результате деперитонизации (иссечения участков брюшины) создаются дополнительные пути оттока для перитонеальной жидкости.
Прогноз
Асцит при онкологическом заболевании в разы ухудшает общее самочувствие больного. Как правило, такое осложнение возникает на поздних стадиях онкологии, при которых прогноз выживаемости зависит от характера самой опухоли и ее распространенности по организму.
Продолжительность жизни при асците зависит от следующих факторов:
Развитие асцита может предотвратить опытный врач, наблюдающий пациента. Врачи Юсуповской больницы имеют огромный опыт борьбы с различного рода онкологическими заболеваниями. Квалификация медицинского персонала и новейшее оборудование позволяют провести точную диагностику и качественное, эффективное лечение согласно европейским стандартам.
Преимущества лечения асцита в Юсуповской больнице
Часто лечение асцита, вызванного раком, проводится в неспециализированных клиниках, где нет соответствующих условий и оборудования, не учитываются особенности онкологических больных.
Цель Юсуповской больницы — предоставить каждому пациенту максимально квалифицированную, эффективную помощь:
Наши усилия постоянно направлены на повышение эффективности лечения, улучшение качества жизни и прогнозов для каждого пациента.
Для того чтобы увеличить продолжительность и улучшить качество жизни пациента с асцитом, который развился вследствие онкологической патологии, обращайтесь к онкологам Юсуповской больницы. Врачи клиники онкологии проводят терапию, направленную на устранение причины накопления избыточного количества жидкости в брюшной полости, проводят симптоматическое лечение.
Отечно-асцитический синдром
Что провоцирует / Причины Отечно-асцитического синдрома:
В 6-7 % случаев у больных циррозом печени развивается правосторонний гидроторакс.
Патогенез (что происходит?) во время Отечно-асцитического синдрома:
Патогенез асцита у больных циррозом печени является многофакторным. Портальная гипертензия и связанный с ней застой в системе воротной вены являются пусковыми факторами развития асцита. Кроме того, развитию асцита способствует каскад нейрогормональных, гемодинамических и вводно-электролитных сдвигов. В настоящее время патогенез асцита рассматривается как индивидуальное сочетание многочисленных патогенетических факторов прогрессирования основного патологического процесса, которые условно разделены на местные (регионарные) и общие (системные).
К местным регионарным факторам относятся повышение печеночного сосудистого сопротивления вследствие взаимодействия комплекса органических и функциональных нарушений. По преимущественной локализации поражения при ХЗП можно выделить преси-нусоидальный, синусоидальный и постсинусоидальный уровни блока. В зависимости от обратимости изменений выделяют необратимые, или органические, поражения и потенциально обратимые, или функциональные, изменения.
Внутрипеченочный блок оттока приводит к усиленному лимфообразованию. При этом лимфа может просачиваться через лимфатические сосуды глиссоновой капсулы прямо в брюшную полость или поступать в области ворот печени в грудной лимфатический проток. В результате развивающегося лимфатического застоя происходит пропотевание жидкости в брюшную полость.
Одним из важных моментов патогенеза асцита является накопление у больных в циркулирующей крови нерасщепленных эндогенных вазодилататоров (глюкагон и др.), способствующих расширению мелких периферических артерий, а также открытию артериовенозных шунтов в органах и тканях, что помогает снижению кровенаполнения артерий, увеличению сердечного выброса, гиперволемии, повышению скорости портального кровотока и портальной гипертензии. Кроме того, следует помнить, что накопление асцитической жидкости сопровождается снижением эффективного кровотока в результате депонирования значительной части объема плазмы в сосудах брюшной полости. Эффект вазодилататоров повышается на фоне недостатка синтеза оксида азота, что способствует усилению вазоконстрикции в синусоидах и мелких разветвлениях воротной вены. Аналогичным образом действует значительная гиперпродукция эндотелинов набухшими эндотелиоцитами.
Установлено, что асцит в первую очередь формируется внутрипеченочно, внутри печеночных синусоидов. Стенки эндотелиальной выстилки синусоидов имеют относительно большие поры-финестры, необходимые для обеспечения легкого доступа плазмы к гепатоцитам в пространстве Диссе. В перипортальной области имеются выстланные эндотелием, слепо начинающиеся лимфатические капилляры, благодаря чему жидкость из пространства Диссе может попасть в лимфатические капилляры, проходя эндотелиальную стенку. При формировании блока оттока из печени возникает синусоидальная гипертензия. В соответствии с законом Старлинга, повышение синусоидального давления является фактором, усиливающим проникновение элементов плазмы через стенку синусоида в перисинусоидальное пространство Диссе, а затем в лимфатические сосуды, которые компенсируют синусоидальную гипертензию за счет возрастания оттока лимфы из печени.
К системным факторам, способствующим формированию ПГ, можно отнести гипоальбуминемию, активизацию симпатической нервной системы, повышение секреции компонентов ренин-ангиотензиналь-достероновой системы, антидиуретического гормона, предсердного натрийуретического пептида, снижение продукции простагландинов.
Наряду с вышеуказанными изменениями важную роль в формировании асцита играет гиперальдостеронизм, природа которого довольно сложна и включает в себя следующие механизмы:
Известно, что концентрация альбумина в сыворотке крови является ведущим фактором, определяющим онкотическое давление. По мере прогрессирования патологического процесса, проявляющегося на морфологическом уровне дистрофически-некротическими процессами в паренхиме и синусоидах, нарушается синтез альбуминов и, как следствие, изменяется проницаемость синусоидального эндотелия. При этом значение гипоальбуминемии и сопутствующих ей изменений онкотических градиентов возрастает.
У большинства больных хроническими гепатитами на цирротической стадии выявлены признаки активации симпатической нервной системы. Повышение уровня катехоламинов в сыворотке крови обнаружено у 60 % пациентов Считается, что снижение эффективного внутрисосудистого объема и гипоальбуминемия способствуют повышению секреции катехоламинов в целях поддержания важнейших го меостатических показателей.
Секреция ренина в почках является одной из важнейших компенсаторных реакций в условиях гиповолемии. Выброс ренина происходит вследствие как гиповолемии, так и гипонатриемии. Ренин вызывает увеличение синтеза ангиотензина, являющегося мощным вазоконстриктором, и стимулирует секрецию альдостерона. Увеличение уровня альдостерона приводит к повышению реабсорбции натрия и воды в почках
Большинство авторов сообщает о повышении уровня предсердного натрийуретического пептида при циррозе печени с асцитом. По-видимому, повышение концентрации натрийуретического пептида и увеличение задержки натрия при циррозе могут объясняться снижением чувствительности почек к данному гормону
Одним из возможных участников патогенеза асцита рассматривается простагландин Ег, синтезирующийся, в частности, в почках и обладающий вазодилататорным действием. Считается, что степень задержки натрия может быть вызвана снижением продукции этого вазодилататора. При этом простагландины оказываются патогенетически связующим звеном между изменениями гемодинамики на локальном уровне и системными гуморальными реакциями.
Следовательно, в развитии асцита при заболеваниях печени важную роль играют гемодинамические и метаболические факторы, проявляющиеся на фоне морфологической перестройки печени Появление асцита обусловлено выраженной задержкой натрия. Суточная экскреция натрия с мочой при асците не превышает 5 ммоль.
Согласно теории «недостаточного наполнения сосудистого русла», задержка натрия и воды почками вторична и обусловлена расширением сосудистого русла внутренних органов. Причиной указанных явлений считается активизация ренин-ангиотензин-альдостероновой системы, симпатической нервной системы, простагландина Ег, способствующая изменению функции почек. При этом натрийуретическому фактору отводится второстепенная роль.
Теория «избыточного наполнения сосудистого русла» предусматривает первичную задержку натрия с дальнейшим увеличением объема циркулирующей плазмы и переходом жидкости в межклеточное пространство.
Важная роль отводится активному переносу жидкости через мембрану капилляров брюшины. Кроме того, формированию асцита способствуют повышение давления внутри синусоидов, что наблюдается ПРИ циррозе, усиленное образование лимфы при обструкции синусоидов, печеночных вен.
Диагностика Отечно-асцитического синдрома:
Большое скопление жидкости в брюшной полости можно обнаружить обычными клиническими методами. При перкуссии выявляется притупление звука в боковых отделах живота. Перемещение больных на левый или правый бок вызывает смещение тупости к соответствующему фланку. При наличии осумкованной жидкости в брюшной полости, при слипчивом перитоните туберкулезной этиологии, кисте яичника перемена положения пациента тимпанит не изменяет. Асцитическую жидкость объемом менее 1,5 л определить клиническими методами не удаегся. В подобных случаях асцит можно определить с помощью УЗИ. Минимальное количество асцитической жидкости, определяемое указанным методом, составляет 200 мл. УЗИ в ряде случаев позволяет выявить заболевание, явившееся причиной развития асцита (цирроз печени, новообразование органов брюшной полости, панкреатит и др.). После клинического обнаружения асцига в неясных случаях показано проведение диагностического парацентеза с биохимическим и цитологическим исследованиями полученной жидкости. При парацентезе с помощью тонкой иглы получают 50-250 мл асцитической жидкости.
Показаниями для проведения диагностического парацентеза являются;
В асцитической жидкости определяют уровень общего белка, альбумина, глюкозы, холестерина, триглицеридов, билирубина, активности амилазы, производят подсчет количества лейкоцитов, эритроцитов, атипических клеток, окраску бактерий по Граму, посев жидкости на микрофлору с определением чувствительности к антибиотикам В. A Runyon предлагает определять в асцитической жидкости сывороточно-асцитический альбуминовый градиент (СААГ).
Лечение Отечно-асцитического синдрома:
Лечение отечно-асцитического синдрома при циррозе печени. При лечении асцита необходимо установить этиологию цирроза печени, выявить факторы, лежащие в основе его декомпенсации Выделяют базисную и диуретическую терапию.
Мероприятия, проводимые в рамках базисной терапии, включают постельный режим, уменьшение потребления поваренной соли, ограничение приема жидкости, соблюдение диеты. Для поддержания натриевого баланса целесообразно ограничить поступление хлористого натрия до 500 мг в сутки Проведение диуретической терапии предусматривает ежедневный контроль ряда параметров.
Терапия диуретиками проводится по ступенчатому принципу. Прием диуретиков можно осуществлять при отсутствии тяжелых электролитных сдвигов и нарушений функции почек. Диуретики подавляют факторы, вызывающие задержку натрия, и повышают экскрецию натрия и воды. В лечении больных асцитом чаще используют две группы диуретиков. В первую группу входят петлевые диуретики* фуросемид, буметанид, этакриновая кислота. Ко второй группе относятся спиронолактон, триамтерен, амилорид
Тактика при длительном лечении больных циррозом печени с асцитом.После ликвидации асцита возникает вопрос о длительном лечении указанной категории лиц. Больные должны придерживаться рекомендованной бессолевой диеты, проводить регулярный контроль за количеством выпитой жидкости и выделенной мочи, измерять массу тела. Доза диуретического препарата зависит от тяжести и стадии заболевания. При этом чаще используются 100-200 мг/сут спиронолактона и через день 40-80 мг/сут фуросемида в сочетании с препаратами калия. Один раз в месяц нужно исследовать содержание электролитов, азота, мочевины, проводить функциональные пробы печени, определять содержание белка в крови.
Рефрактерный (ригидный) асцит. Термин «рефрактерный к лечению асцит» используется в том случае, когда при терапии, проводимой по всем правилам, масса тела не снижается. Если диуретическая терапия, проводимая, как минимум, в течение 4 нед, оказывается неэффективной и исключаются все причины, способные вызывать мнимую рефрактерность к лечению, можно думать о рефрактерном асците.
Причинами данного синдрома чаще являютсядалеко зашедший патологический процесс в печени, большие поступления натрия в организм (с пищей, лекарственными препаратами), отсутствие ограничения приема жидкости, нарушение функции почек, не связанное с заболеванием печени, происхождение асцита (злокачественные новообразования, воспаление асцитической жидкости) и др.
Эффективным методом лечения рефрактерного асцита является парацентез, при проведении которого удаляется 5-10 л жидкости на фоне введения бессолевого альбумина: по 6 г на 1 л удаляемой жидкости. В качестве симптоматической терапии таким больным показаны методы экстракорпоральной гемокоррекции: ультрафильтрация и реинфузия асцитической жидкости, перитонеовенозное шунтирование, имплантация TIPS, трансплантация печени.
Прогноз. У 8-32 % больных с асцитом развивается спонтанный бактериальный перитонит.
К каким докторам следует обращаться если у Вас Отечно-асцитический синдром:
Патогенетические подходы к диуретической терапии асцита
(Продолжение. Начало см. в №6)
Оценка эффективности диуретической терапии у больных циррозом печени с асцитом
Показателями эффективности лечения у пациентов с асцитом являются:
Эксперты Всемирной организации гастроэнтерологов (ВОГ — OMGE) рекомендуют тактику диуретической терапии у больных циррозом печени с асцитом основывать на оценке уровня Nа и креатинина сыворотки крови [16].
Помимо вышеуказанных показателей, при длительной мочегонной терапии необходимо мониторировать уровни калия, магния, кальция, сахара, мочевины, мочевой кислоты, липидограмму, а также кислотно-щелочное равновесие крови, учитывая все возможные побочные эффекты диуретиков.
Дегидратационная терапия при асците имеет фазы активную и поддерживающую.
В активной фазе, при отсутствии отеков ног, превышение выделенной мочи над принятой жидкостью должно составлять около 1 литра в сутки со снижением веса ежедневно до 0,5–1 кг.
При наличии отеков ног положительный диурез может составлять 2–3 литра в сутки. В данном случае нет ограничений для ежедневного снижения веса. Как только отеки исчезают, но асцит остается, для профилактики азотемии (вследствие уменьшения внутрисосудистого объема) скорость потери веса не должна превышать 0,5 кг в день, так как избыточный диурез сопровождается истощением внутрисосудистого объема, что приводит к почечной недостаточности, печеночной энцефалопатии и гипонатриемии.
В поддерживающей фазе диурез должен быть сбалансированным и масса тела стабильной при регулярном (ежедневном) назначении мочегонных.
Попытка «ударного» диуреза — один раз в несколько дней является ошибочной. Никакая стремительная дегидратация не может быть оправданной и лишь приводит к гиперактивации нейрогормонов и задержке жидкости в организме.
Следует отметить, что объем уменьшения асцита у больного циррозом печени ограничен уровнем реабсорбции асцитической жидкости, который составляет 700–900 мл в сутки. Поэтому при полиурии до 3 литров в сутки теряется значительное количество неасцитической внеклеточной жидкости, что приводит к уменьшению отеков и наполнения венозного русла. Это безопасно, пока у пациента существуют отеки. Если стимуляция диуреза продолжается после исчезновения отеков и потеря жидкости превышает лимит реабсорбции асцита, то это приводит к уменьшению объема циркулирующей плазмы. При этом почечный кровоток снижается, что способствует развитию функциональной почечной недостаточности и развитию гепаторенального синдрома (ГРС), летальность при котором достигает 75%.
Рефрактерность к диуретической терапии у больных циррозом печени с асцитом. У больных циррозом печени может развиться ранняя (так называемое торможение эффекта) и поздняя рефрактерность. Ранняя рефрактерность появляется в первые часы или дни после начала активного назначения мочегонных средств, зависит от гиперактивации нейрогормонов и тем сильнее, чем активнее дегидратация (нерекомендуемый обильный диурез).
Ранняя рефрактерность преодолевается адекватным (не чрезмерным) диурезом с обязательным совместным применением иАПФ и/или спиронолактона.
Поздняя рефрактерность возникает спустя недели и месяцы постоянной диуретической терапии и связана с гипертрофией апикальных клеток почечных канальцев, где как раз и действуют диуретики.
Развитие поздней рефрактерности требует периодической (раз в 3–4 недели) смены активных диуретиков и их комбинации с иАПФ.
При этом целесообразно:
У больных циррозом печени с асцитом, длительно получающих диуретическую терапию, могут наблюдаться побочные эффекты (чаще у лиц женского пола — вследствие гиперэстогенемии), с исходными нарушениями электролитного баланса, выраженной ПКН и сниженным артериальным давлением.
Основные побочные эффекты комбинированного лечения диуретиками у больных циррозом печени с асцитом. Наиболее частыми осложнениями диуретической терапии являются:
При повышении калия и креатинина:
В ряде клинических ситуаций, вследствие развития побочных эффектов и ухудшения состояния пациентов, встает вопрос об отмене диуретической терапии.
Показания для отмены диуретических препаратов у больных циррозом печени с асцитом:
Заключение
Появление асцита — важный, поворотный этап в течении цирроза печени. Адекватное ведение асцита не только улучшает качество жизни пациента с циррозом, но и позволяет предотвратить тяжелые осложнения, такие как кровотечение, СБП и ГРС (схема 1).
Тем не менее, несмотря на уменьшение асцита и улучшение качества жизни пациентов, не повышается отдаленная выживаемость без трансплантации у большинства больных циррозом печени, поэтому при его развитии следует рассматривать вопрос о возможности пересадки печени.
Следует отметить, что специалисты, участвующие в лечении этих пациентов, постоянно сталкиваются с последовательно возникающими трудноразрешимыми задачами, нередко приводящими к неэффективному лечению и летальному исходу. По мнению авторов, важнейшим направлением в терапии асцита, помимо выведения избыточной жидкости из организма, является коррекция ПГ. Для этого рекомендуется использовать средства, воздействующие на ее функциональный компонент и механизмы системной реализации с вовлечением центральной гемодинамики. При этом препаратами, воздействующими на функциональный компонент ПГ, являются неселективные БАБ и антагонисты альдостерона в качестве нейрогуморальных модуляторов. К средствам, снижающим системные проявления ПГ, относятся иАПФ и АРА. Основываясь на патогенетических механизмах развития асцита у больных циррозом печени, авторы предприняли попытку разработать схему комплексной терапии данной категории пациентов, включающую период до развития асцита (схема 2).
В целом для эффективного лечения асцита у больных циррозом печени актуальны все описанные разделы. Это и соблюдение жесткого режима, диеты, регулярная оценка диуреза и лабораторных показателей, и знание современных подходов диуретической терапии, и правильное использование новых препаратов. Важным и необходимым при этом являются одновременный учет и ежедневная кропотливая оценка целого перечня клинических параметров, состояния ССС, почек и т. д. для принятия индивидуального терапевтического решения по поводу конкретного пациента.
Таким образом, лечение асцита — это очень тонкая «ювелирная» работа, в которой каждая мелочь значима; требует от врача дополнительных знаний, опыта и умения целостно оценивать многоуровневую систему координат под названием «цирроз печени».
По вопросам литературы обращайтесь в редакцию.
С. Н. Мехтиев, доктор медицинских наук, профессор
Ю. А. Кравчук, кандидат медицинских наук
И. В. Субботина
О. А. Мехтиева *
М. В. Шаповалов
ВМА им. С. М. Кирова, * СПб ГМА им. И. И. Мечникова, Санкт-Петербург
Схема 1
Алгоритм назначения диуретиков больным циррозом печени в зависимости от наличия и выраженности асцита
Отсутствие асцита — антагонисты альдостерона в качестве нейрогуморального модулятора (спиронолактон 25–50 мг/сут*), курсы по 3–6 месяцев с перерывом на 1–3 месяца.
Начальный (транзиторный) асцит — антагонисты альдостерона (спиронолактон до 200 мг/сут), после разрешения асцита переход на поддерживающую «нейромодуляторную» (25–50 мг/сут) дозу.
Умеренный (ненапряженный) — антагонисты альдостерона (спиронолактон до 200 мг/сут) + петлевые (фуросемид в дозе 40–160 мг/сут/торасемид 5–100 мг/сут).
Напряженный асцит — так же, как при умеренном асците: спиронолактон (100–400 мг/сут) + фуросемид (40–160 мг/сут)/торасемид (5–100 мг/сут), если максимальные дозы применяемых препаратов неэффективны в течение 5–7 дней, асцит рассматривается как резистентный.
Резистентный асцит (это понятие включает в себя неэффективность комбинированной терапии спиронолактоном и фуросемидом, поэтому изначально рекомендуется замена фуросемида торасемидом):
при сохранении неэффективности:
Поддерживающая терапия (для всех видов асцита, кроме начального):
при неэффективности возможно дополнение терапии 1–2-кратным приемом в неделю фуросемида (40–160 мг/сут) или торасемида (5–100 мг/сут) или Урегита (25–50 мг/сут).
* При побочных эффектах/противопоказаниях к антагонистам альдостерона и в качестве дополнительного мочегонного средства используются:
Схема 2
Вариант рабочей схемы комплексной терапии асцита у пациентов с циррозом печени в зависимости от его наличия и выраженности:
Отсутствие асцита (длительность терапии — постоянно):
Начальный асцит (длительность терапии — постоянно):
Умеренный (ненапряженный) асцит (длительность терапии — до разрешения асцита, затем перевод на поддерживающую терапию):
Напряженный асцит (длительность терапии — индивидуально, обычно до 4 недель, затем перевод на поддерживающую терапию):
Основная терапия
Если максимальные дозы применяемых препаратов неэффективны в течение 3–7 дней, асцит рассматривается как резистентный. Для профилактики развития резистентного асцита дополнительно рекомендуется вспомогательная терапия.
Вспомогательная терапия (препараты, улучшающие почечную фильтрацию, инотропную функцию миокарда, повышающие онкотическое давление крови):
Резистентный асцит:
Основная терапия
– спиронолактон (100–400 мг/сут) + торасемид (5–100 мг/сут) или
– спиронолактон (100–400 мг/сут) + Урегит (25–50 мг/сут) при сохранении неэффективности:
– спиронолактон (100–400 мг/сут) + фуросемид (40–160 мг/сут) + Урегит (25–50 мг/сут) или
– спиронолактон (100–400 мг/сут) + фуросемид (40–160 мг/сут) + торасемид (5–100 мг/сут) или
– спиронолактон (100–400 мг/сут) + торасемид (50–100 мг/сут) + Урегит (25–50 мг/сут).
Вспомогательная терапия (аналогична терапии при напряженном асците)
Важной терапевтической задачей на данном этапе является профилактика печеночной энцефалопатии (ПЭ), кровотечения, СБП, ГРС.
Поддерживающая терапия (для всех видов асцита, кроме начального):
При неэффективности возможно дополнение терапии 1–2-кратным приемом в неделю фуросемида (40–160 мг/сут) или торасемида (5–10 мг/сут) или Урегита (25–50 мг/сут).
* Авторская точка зрения
** При отсутствии противопоказаний