Что такое ренопривное состояние
Публикации в СМИ
Гипертензия артериальная вазоренальная
Вазоренальная артериальная гипертензия (АГ, реноваскулярная гипертония) — симптоматическая (вторичная) АГ, вызванная ишемией почки (почек) вследствие сужения почечной артерии или её ветвей, редко — двустороннего поражения. Статистические данные. Распространённость составляет 1–2% (до 4–16% по данным специализированных клиник) среди всех видов АГ.
Этиология
• Наиболее частая причина стеноза почечной артерии — атеросклероз (отмечаемый среди всех видов стеноза почечной артерии в 62%). Локализация атероматозных бляшек •• Проксимальные сегменты почечной артерии вблизи аорты (74% случаев) •• Средние сегменты почечной артерии (16% случаев) •• Вблизи бифуркации почечной артерии (5% случаев) •• Дистальные ветви почечной артерии (5% случаев).
• Реже (у 24% больных) отмечают врождённое заболевание — фибромускулярную дисплазию. Поражение локализуется в средней трети почечной артерии. Различают следующие типы процесса: •• Пролиферация внутренней оболочки ••• Первичная ••• Вторичная •• Дисплазия среднего слоя ••• Гиперплазия среднего слоя ••• Перимедиальная фиброзная дисплазия ••• Дисплазия с образованием микроаневризм ••• Расслоение среднего слоя •• Субадвентициальная фиброплазия.
• Прочие виды стенотических поражений почечных артерий наблюдают в 6% случаев •• Врождённый стеноз артерии (наиболее частая причина АГ у детей) •• Аневризма почечной артерии •• Травматический тромбоз и эмболия •• Коарктация аорты со стенозом почечной артерии •• Неспецифический аортоартериит •• Сдавление сосудистой ножки почки извне опухолью или инородным телом.
Патогенез
• Сужение почечной артерии активирует юкстагломерулярный аппарат вследствие снижения АД в постстенотическом сегменте, что приводит к выделению ренина, и снижения концентрации натрия в петле нефрона.
• Ренин превращает поступающий из печени ангиотензиноген в ангиотензин I, превращающийся под влиянием АПФ в ангиотензин II, непосредственно воздействующий на системные артериолы и резко увеличивающий периферическое сопротивление.
• Опосредованно через кору надпочечников ангиотензин II приводит к гиперальдостеронизму, задержке натрия в организме и повышению объёма внеклеточной жидкости.
• Результаты хирургического лечения во многом определяются тем, поражена одна или обе почечных артерии •• При одностороннем стенозе причина АГ — ренопрессорные механизмы ишемизированной почки. Однако со временем контрлатеральная интактная почка переключится на новый режим АД и будет поддерживать АГ даже в том случае, когда первоначальный источник АГ удалён или реваскуляризирован •• При двустороннем стенозе почечных артерий поэтапная его ликвидация приводит, как правило, к снижению АД. То же наблюдают и при реваскуляризации единственной почки.
Клинические проявления
• Стеноз почечных артерий можно заподозрить при неожиданном возникновении АГ или внезапном резком ухудшении ранее доброкачественно протекавшей АГ. Артериальная гипертензия возникает до 30 или после 50 лет, обычно при отсутствии семейного анамнеза АГ. Характерны быстрое прогрессирование АГ, высокие значения АД, быстрое поражения органов-мишеней, резистентность к лечению.
• Жалобы •• Характерные для церебральной гипертензии — головные боли, чувство тяжести в голове, приливы к голове, шум в ушах, боли в глазных яблоках, снижение памяти, плохой сон, раздражительность, мелькание «мушек» перед глазами •• Связанные с перегрузкой левых отделов сердца и относительной или истинной коронарной недостаточностью — боли в области сердца, сердцебиение, одышка, чувство тяжести за грудиной •• Обусловленные урологической патологией — чувство тяжести, либо тупые боли в поясничной области, а в случае инфаркта почки — гематурия •• Обусловленные ишемией других органов, магистральные артерии которых могут быть поражены одновременно с почечными артериями ••• Симптомы ишемии органов ЖКТ ••• Ишемия верхних или нижних конечностей ••• Признаки атеросклероза сосудов головного мозга •• Признаки воспалительной реакции (при неспецифическом аортоартериите) •• Жалобы, характерные для вторичного гиперальдостеронизма, — мышечная слабость, парестезии, приступы тетании, изогипостенурия, полидипсия, никтурия.
• Как и для любой почечной АГ характерны высокие показатели диастолического АД, достигающие в некоторых случаях 170 мм рт.ст.
• Систолический шум в правом или левом верхнем квадранте живота и по задней стенке грудной клетки. Шум обычно неинтенсивный, в отличие от шумов, выслушиваемых при артериовенозной фистуле почки или атеросклерозе брюшной аорты (грубых и продолжительных).
Лабораторные и инструментальные данные
• Гипокалиемия (на фоне избыточной секреции альдостерона).
• Определение активности ренина плазмы, особенно в сочетании с каптоприловым тестом (100% чувствительность и 95% специфичность): увеличение активности ренина плазмы после приёма каптоприла более чем на 100% от исходной величины указывает на патологически высокую секрецию ренина, и является признаком вазоренальной АГ
• Рентгеноконтрастная ангиография — «золотой стандарт» в диагностике стеноза почечных артерий. Предпочтителен трансфеморальный метод по Сельдингеру: обнаруживают стеноз почечной артерии и (дистальнее его) веретенообразное её расширение •• При нефроптозе почечная артерия натянута, она отходит от аорты под острым углом, диаметр её сужен •• При атеросклерозе почечной артерии дефект заполнения чаще всего располагается вблизи устья почечной артерии. Часто на ангиограмме выявляют признаки атеросклероза аорты •• При фибромускулярной дисплазии определяют многоочаговое сужение почечной артерии, в большинстве случаев начинающееся на расстоянии 2 см дистальнее места отхождения артерии от аорты •• При неспецифическом аортоартериите находят узурацию стенок брюшной аорты наряду с сужением почечной артерии. Часто определяют стенотические поражения и других ветвей аорты •• При тромбозе или эмболии почечной артерии определяют симптом «слепого окончания» ствола почечной артерии или одной из её основных ветвей •• При аневризме почечной артерии мешотчатое или веретенообразное её расширение располагается преимущественно в области ворот почки. Стенки аневризмы часто кальцинируются.
• Асимметрия почек при УЗИ.
• Допплеровское исследование почечных артерий — ускорение кровотока и его турбулентность.
• Почечная сцинтиграфия — уменьшение абсорбции препарата, уменьшение поступления препарата в поражённую почку, асимметрия ренографических кривых. Оптимально сочетание сцинтиграфии почек с приёмом каптоприла в дозе 25–50 мг внутрь. При приёме каптоприла уменьшается поступление изотопа в почечную ткань. Нормальная сцинтиграмма почек после приёма каптоприла исключает гемодинамически значимый стеноз почечной артерии.
• Экскреторная урография: могут быть снижены интенсивность концентрирования контрастного вещества и время его появления на урограмме, а также уменьшение в размерах почки; однако экскреторная урограмма может оставаться нормальной, поэтому окончательный диагноз требует подтверждения аортографией.
• МРТ почечных артерий — современный метод верификации вазоренальной АГ.
Дифференциальная диагностика • Первичный альдостеронизм • Феохромоцитома • Синдром Кушинга • Коарктация аорты • Заболевания паренхимы почек, приводящие, например к ХПН.
ЛЕЧЕНИЕ
Общая тактика. В первую очередь необходимо рассмотреть возможность радикального лечения — чрескожной транслюминальной почечной ангиопластики, стентирования стенозированной артерии или радикального хирургического лечения. При невозможности подобного лечения или наличии противопоказаний к нему назначают лекарственную терапию.
Лекарственная терапия — вспомогательная, т.к. снижение АД при стенозе почечной артерии нефизиологично (приводит к декомпенсации кровообращения в почке и её сморщиванию).
• Показания к длительному лечению — пожилой возраст и системное поражение артериального русла, включая коронарные артерии.
• Препараты выбора — ингибиторы АПФ, например каптоприл. Дополнительно назначают другие антигипертензивные средства (см. Гипертензия артериальная). Лечение начинают с минимальных доз ингибиторов АПФ короткого действия (например, каптоприла в дозе 6,25 мг). При отсутствии коллапса дозу каптоприла увеличивают или назначают длительно действующие ингибиторы АПФ. Необходим контроль содержания креатинина и СКФ. Ингибиторы АПФ противопоказаны при двустороннем стенозе почечных артерий.
Баллонная дилатация почечных артерий
• Мнения о её эффективности противоречивы. В любом случае, данный метод — хороший прогностический критерий последующей операции: если после адекватной дилатации происходит даже временная нормализация АД, можно говорить о прямой зависимости АГ от стеноза почечной артерии.
• Показания •• Устойчивая к терапии АГ у больных старше 60 лет с ангиографически выявленными стенозами почечных артерий •• Факторы риска (стеноз сонных, коронарных артерий, сердечная и дыхательная недостаточность) •• Почечная недостаточность, обусловленная стенозами почечных артерий •• Рестенозы почечных артерий после их реваскуляризации или трансплантации почек •• В качестве диагностической процедуры для выяснения связи стеноза почечной артерии и АГ.
Хирургическое лечение
• Органосохраняющие операции •• Резекция почечной артерии с реимплантацией в аорту •• Резекция с анастомозом «конец в конец» •• Трансаортальная эндартерэктомия •• Аутопластика почечных артерий свободными трансплантатами •• Создание спленоренального анастомоза •• Пластика почечной артерии синтетическими антитромбогенными протезами.
• Нефрэктомия — при невозможности выполнить реконструктивную операцию на артерии (доля нефрэктомий от общего числа операций — 16–20%).
• Противопоказания •• Двустороннее протяжённое поражение почечных артерий •• Сморщивание обеих почек •• Инфаркт миокарда и период до 6 мес после него •• острое нарушение мозгового кровообращения •• Терминальная стадия ХПН.
• Послеоперационные осложнения •• Внутреннее кровотечение •• Тромбоз сосудистых анастомозов •• ОПН.
• Результаты операций •• Летальность составляет 0–6% •• Положительные результаты при атеросклерозе почечной артерии отмечают у 63% больных, при фибромускулярной дисплазии — у 73% •• Период нормализации АД после операции может растягиваться до 6 мес.
• Послеоперационное ведение. Больным рекомендован диспансерный учёт. При остаточной АГ назначают антигипертензивные препараты.
Сокращение. АГ — артериальная гипертензия.
МКБ-10 • I15.0 Реноваскулярная гипертензия
Малоинвазивное лечение осложнений после лапароскопической резекции единственной почки
З.К. Эмиргаев, О.А. Богомолов, М.И. Школьник, Д.Г. Прохоров, А.С. Полехин
ФГБУ «Российский научный центр радиологии и хирургических технологий им. акад. А.М. Гранова» Минздрава России, Санкт-Петербург, Россия
Введение
Злокачественные опухоли почки занимают третье место среди злокачественных новообразований мочеполовой системы после опухолей предстательной железы и мочевого пузыря [1]. Особую сложность представляет лечение опухолей единственной почки. Методом выбора у таких больных является резекция почки, которая позволяет добиться хороших онкологических и функциональных результатов [2–4]. В качестве альтернативы резекции почки выступают радиочастотная абляция и криодеструкция опухоли, суперселективная эмболизация сосудов новообразования, а в ряде случаев — нефрэктомия, переводящая больного в ренопривное состояние [5, 6]. К наиболее частым осложнениям резекции единственной почки относятся кровотечения, мочевые свищи, острая почечная недостаточность [2]. Вероятность развития и тяжесть осложнений зависят от степени сложности резекции почки. Риск развития осложнений возрастает при удалении больших опухолей, особенно в средней трети почки [2, 7, 8].
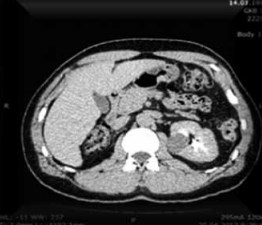
В данном сообщении описано клиническое наблюдение больного М., 53 года, оперированного по поводу опухоли единственной левой почки. Правая почка была удалена вследствие гидронефротической трансформации 32 года назад. В дальнейшем пациент находился под наблюдением амбулаторных уролога и нефролога, признаков снижения суммарной почечной функции не отмечалось. В апреле 2017 г. при плановом УЗИ выявлено образование верхней трети единственной левой почки. С целью уточнения диагноза была выполнена МСКТ, при которой было подтверждено наличие внутриорганного образования верхней трети левой почки размером 3,0 × 2,9 × 2,3 см, прилежащего к чашечно-лоханочной системе (рис. 1). По данным МСКТ и остеосцинтиграфии поражение регионарных лимфатических узлов и отдаленные метастазы отсутствовали.
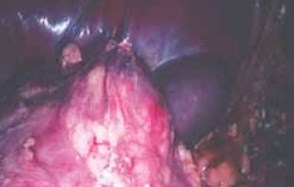
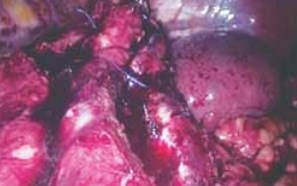
В мае 2017 г. больной был госпитализирован в ФГБУ «РНЦРХТ им. акад. А.М. Гранова» с диагнозом: «Опухоль единственной левой почки, сT1N0M0». Проведено обследование. Поясничная область не изменена, безболезненна при поколачивании, почки не пальпируются. В правой поясничной области определяется послеоперационный рубец линейной формы длиной 10 см после нефрэктомии. Патологических изменений в лабораторных анализах крови и мочи не выявлено. 24.05.2017 выполнена лапароскопическая резекция единственной левой почки. Во время операции поддерживался пневмоперитонеум 12 мм рт. ст. Первым этапом была вскрыта брюшина по линии Тольда слева. Почка мобилизована по передней, задней и латеральной поверхностям. В верхней трети левой почки визуализировано образование размером 3,1 × 3 × 2,5 см. Далее была мобилизована почечная ножка. Учитывая наличие единственной почки, было принято решение о выполнении операции без выключения кровотока и тепловой ишемии. Паранефральная клетчатка отсепарована по дистальному краю опухоли, после чего с использованием ультразвукового скальпеля выполнена резекция опухоли (рис. 2, 3). При пересечении артерии, питающей опухоль, отмечено интенсивное кровотечение, вследствие чего культя сосуда была прошита нитями пролен 3.0. Во время резекции была вскрыта верхняя группа чашечек, дефект чашечно-лоханочной системы ушит нитями викрил 2.0. С целью минимизации ишемии и некроза паренхимы почки от наложения гемостатических швов было решено отказаться. Окончательный гемостаз был достигнут с помощью гемостатической губки «Тахокомб». Операция завершена дренированием зоны операции. Гистологическое описание удаленного образования левой почки: «папиллярный рак почки 1-го типа, Grade 1, хирургический край отрицательный».
Рис. 1. МСКТ с внутривенным контрастированием больного М. Визуализируется опухоль единственной левой почки, прилегающая к чашечно-лоханочной системе
Рис. 2. Опухоль левой почки. Интраоперационная фотография
Рис. 3. Левая почка после лапароскопической резекции опухоли. Интраоперационная фотография
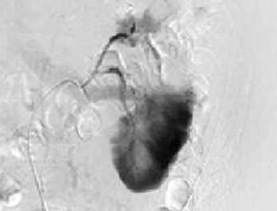
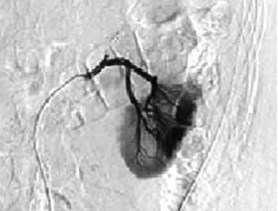
Рис. 4. Ангиография левой почечной артерии. Экстравазация контрастного вещества через культю верхней сегментарной артерии
Рис. 5. Контрольная ангиография после суперселективной эмболизации верхней сегментарной артерии. Экстравазации контрастного вещества нет
На 2-е сутки послеоперационного периода зафиксировано поступление по дренажу геморрагического отделяемого в объеме 400 мл. Пациенту экстренно выполнена ангиография левой почечной артерии. Выявлена экстравазация контрастного вещества через культю верхней сегментарной артерии почки (рис. 4). Осуществлена селективная эмболизация верхней сегментарной артерии (рис. 5). После эмболизации наблюдалось постепенное уменьшение отделяемого по дренажу до 30 мл. На 7-е сутки после операции отмечено поступление по дренажу около 500 мл светло-желтого отделяемого, при биохимическом анализе которого содержание мочевины составило 12,8 ммоль/л, креатинина 488 ммоль/л, что указывало на формирование мочевого свища. Пациенту выполнены цистоскопия и ретроградная уретеропиелография. Выявлена экстравазация контрастного вещества через верхнюю группу чашечек. Произведено стентирование левого мочеточника двухпетлевым антирефлюксным мочеточниковым стентом Колопласт Fr 6, после чего выделение мочи по дренажу прекратилось.
Дренажная трубка из забрюшинного пространства удалена на 9-е сутки после операции, и еще через 2 дня пациент выписан из стационара в удовлетворительном состоянии. Мочеточниковый стент удален через 4 недели после его установки.
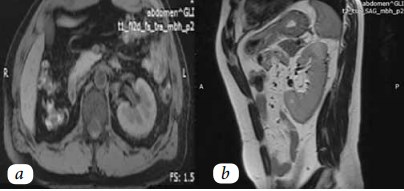
Через 6 месяцев после оперативного вмешательства (26.12.2017) пациенту выполнена МРТ брюшной полости. На фоне послеоперационных изменений признаков рецидивирования опухолевого процесса не обнаружено (рис. 6).
Рис. 6. МРТ с внутривенным контрастированием в аксиальной (а) и сагиттальной (b) плоскостях
Описанный клинический случай подтверждает, что малоинвазивная лапароскопическая операция является альтернативой открытым оперативным вмешательствам у больных с опухолью единственной почки. С целью уменьшения зоны некроза почечной паренхимы лапароскопическая резекция единственной почки должна выполняться по возможности без тепловой ишемии, без или с минимальным наложением гемостатических швов. Прилежание резецируемой опухоли к чашечно лоханочной системе сопряжено с высоким риском интраоперационных и ранних послеоперационных осложнений, таких как кровотечение и формирование мочевых свищей. Условия специализированного стационара позволяют осуществлять лечение осложнений малоинвазивными методами без выполнения повторных оперативных вмешательств.
Литература
Статья опубликована в журнале «Урологические ведомости» № 4 2018, стр. 38-40
Хроническая почечная недостаточность при урологических заболеваниях почек: взгляд нефролога
 | Евгений Михайлович Шилов Д.м.н., проф., зав. кафедрой нефрологии и гемодиализа ФППОВ ММА им. И.М. Сеченова emshilov@stream.ru |
 | Юрий Сергеевич Милованов Д.м.н., доцент кафедры нефрологии и гемодиализа ФППОВ ММА им.И.М. Сеченова yuriymilovanov@mail.ru |
В развитых странах существенное место в структуре причин хронической почечной недостаточности (ХПН) занимают урологические заболевания: воспалительные (хронический пиелонефрит – ХП), наследственные и врожденные (поликистозная болезнь, сегментарная гипоплазия, рефлюкс-нефропатия), обструктивные нефропатии (нефролитиаз, опухоли мочевой системы, гидронефроз, мочеполовой шистосомоз).
У таких больных ХПН может развиться как ренопривное состояние, возникающее в результате планового удаления почек по поводу злокачественных заболеваний, нефролитиаза. ХПН может также быть исходом острой почечной недостаточности (ОПН). Например, ОПН, развивающаяся у пожилых больных вследствие гнойного пиелонефрита, бывает труднообратимой и отличается частым присоединением ХПН с неблагоприятным прогнозом, связанным в том числе с плохой переносимостью гемодиализа. Во всех случаях после выявления почечной недостаточности важно определить, острая она или хроническая (табл. 1).
Таблица 1. Дифференциальная диагностика острой и хронической почечной недостаточности
Критерии диагноза ХПН:
Ранняя диагностика ХПН основана на данных лабораторных методов исследования. Наиболее информативным и надежным является определение максимальной относительной плотности и осмолярности мочи, величины СКФ и уровня креатинина крови. В любом случае, если в течение 3 мес и более СКФ не достигает 60 мл/мин, что означает выключение функции почек неменее чем на 50%, следует констатировать ХПН – независимо от того, имеются ли при этом другие признаки нефропатии.
Основные аспекты ведения пациентов с ХПН в настоящее время четко регламентированы. Своевременно начатая нефропротективная терапия позволяет значительно замедлить темп ухудшения функции почек и предупредить осложнения ХПН, прежде всего сердечно-сосудистые. Пациентам с хронической болезнью почек (ХБП) следует максимально ограничивать потребление поваренной соли (идеально до 0,5 г/сут). Основная цель такого ограничения – достижение целевых величин артериального давления (АД).
Профилактика прогрессирования ХПН заключается в назначении малобелковой диеты – МБД (0,6 г белка/кг/сут) или «строгой» МБД (0,3 г белка/кг/сут). При этом в диете с ограничением белка до 0,6 г/кг массы тела больного не менее 50% должен составлять белок животного происхождения (мясо, в том числе мясо цыплят, яйца, сыр, молоко) как наиболее полноценный по содержанию незаменимых аминокислот. Поддержать белковый баланс позволит добавление эссенциальных (незаменимых) аминокислот и их кетоаналогов. Чтобы МБД неприводили к катаболизму собственных белков организма, больные должны потреблять неменее 35 ккал/кг/сут.
Существенно улучшает течение ХПН рациональное использование диеты в синтезе с энтеросорбентами. Данное сочетание основано на способности энтеросорбентов связывать секретируемые в желудочно-кишечном тракте вместе с пищеварительными соками креатинин, мочевину и другие продукты азотистого обмена. Обычно их назначают при появлении тошноты, тяжести в эпигастрии. Одним из основных энтеросорбентов является лекарственный препарат Полисорб МП. Его применение ведет не только к существенному снижению уровня креатинина и мочевины крови, но и облегчает состояние пациентов за счет снижения симптомов интоксикации и уменьшения проявлений уремической гастроэнтеропатии.
Гипотензивная терапия должна быть длительной и непрерывной, ее начинают с малых доз препаратов, постепенно увеличивая их до терапевтического уровня, так как при быстром снижении АД высок риск развития артериальной гипотонии. В отсутствие противопоказаний (ишемическая болезнь сердца (ИБС), тяжелый церебральный атеросклероз) АД следует поддерживать в пределах 130/80—130/85 мм рт. ст., т. е. на уровне, при котором обеспечивается достаточный почечный кровоток и не индуцируется гиперфильтрация. На более низком уровне (125/75 мм рт. ст.) следует поддерживать АД у больных ХПН с протеинурией более 1 г/сут. Наиболее предпочтительно назначение препаратов длительного действия, метаболизируемых печенью. При недостаточном снижении АД целесообразно дополнительное назначение диуретиков. На их фоне начальные дозы лекарственных средств (ЛС) уменьшают вдвое.
Для снижения уровня гиперфосфатемии (уровень фосфора в крови не должен превышать 5мг/дл), вызывающей гиперплазию паращитовидных желез, используют ЛС, препятствующие всасыванию фосфатов в кишечнике. Препараты эритропоэтина корригируют анемию и геморрагический синдром, эффективны при эксцентрической форме гипертрофии левого желудочка, нестабильной стенокардии, ортостатической и интрадиализной гипотензии. Кпоказаниям относят уровень гематокрита менее 33%, уровень гемоглобина менее 110 г/л. Также необходимо дополнительное назначение железа, причем эффективны лишь препараты железа, вводимые внутривенно.
При ХПН у пациентов с ХП антибактериальную терапию следует проводить при наличии клинических признаков бактериальной инфекции; не стремиться к полному бактериологическому излечению, прежде всего в отношении бессимптомной бактериурии, так как это маловероятно и требует длительных курсов терапии с высоким риском лекарственной нефротоксичности. При ХПН у больных пожилого возраста и пациентов с установленным на длительное время мочевым катетером риск осложнений, вызванных терапией, существенно превышает потенциальную пользу. У больных пиелонефритом единственной почки при ХПН доза антибактериальных препаратов должна подбираться с учетом СКФ. Противопоказано назначение нефротоксичных антибиотиков. В постоянных дозах применяют антибиотики, метаболизируемые печенью.
Оценка темпов прогрессирования ХПН на додиализной стадии должна проводиться не реже 1 раза в 3 мес. Медленное прогрессирование – 15 лет и более – до достижения терминальной стадии ХПН характерно для хронического гломерулонефрита (ХГН) латентного течения, поликистоза почек, ХП, подагрической и анальгетической нефропатии; быстрое – менее 10 лет – для ХГН нефротической или смешанной формы, активного волчаночного нефрита, диабетической нефропатии, амилоидоза почек.
Показанием к началу диализного лечения служит терминальная ХПН — снижение СКФ до 10 мл/мин (повышение креатинина крови до 9–10 мг/дл). Диализное лечение начинают при более низком уровне креатинина и более высоком уровне СКФ, при появлении стойкой гиперкалиемии (более 6,5 ммоль/л), злокачественной артериальной гипертензии с признаками хронической сердечной недостаточности, тяжелой гипергидратации с риском развития отека легких или головного мозга; уремической периферической полиневропатии, декомпенсированного метаболического ацидоза.
Переход к диализным методам лечения ХБП осуществляют в плановом порядке. При достижении уровня СКФ 15 мл/мин (содержание креатинина 6–8 мг/дл) необходимо выполнить операцию формирования артериовенозной фистулы (если больной будет лечиться программным гемодиализом) или начинать обучение больного самостоятельному (на дому) проведению перитонеального диализа). Хронический перитонеальный диализ – метод выбора при трудностях создания постоянного сосудистого доступа (атеросклерозе, диабетической микроангиопатии, гипокоагуляции, у детей раннего возраста), при артериальной гипотонии, нестабильной ИБС, ишемической болезни почек (противопоказания к введению гепарина натрия).
Цель лечения диализом – достижение медицинской и социальной реабилитации больных с тяжелым нарушением функции почек. Примерно у 10—20% больных с терминальной ХПН при диализе полностью восстанавливается трудоспособность, частично – еще у 30—40% пациентов без сопутствующего сахарного диабета, хотя не все из них работают. 20% больных остаются инвалидами, способными обходиться без посторонней помощи. В последние две категории попадают в основном больные с сопутствующим сахарным диабетом, из-за которого снижается эффективность лечения и выживаемость. Смертность колеблется в зависимости от возраста и основного заболевания. Этот показатель у больных с ХПН пожилого возраста и пациентов с ренопривным состоянием на гемодиализе превышает 3% в год. В группе больных моложе 50 лет без сопутствующей патологии смертность после трансплантации почки и при гемоили перитонеальном диализе составляет менее 3—5% в год.
Трансплантация почки в настоящее время признана наиболее эффективным методом лечения поздних стадий ХПН. При подборе донора почки обязательна тканевая совместимость по антигенам системы HLA. Самые лучшие результаты наблюдаются после трансплантации почки родственника первой степени (при идентичности антигенов HLA): годичная выживаемость трансплантата составляет 95%. При частичной совместимости поHLA c живым донором (совпадении одного гаплотипа) результаты несколько лучше, чем после трансплантации трупной почки.
Однако даже при полной совместимости поHLA (например, если почка берется у родного брата или сестры) 5—10% трансплантированных почек отторгается, часто в первую неделю после операции. Реакция отторжения в этих случаях обусловлена сенсибилизацией к антигенам малых комплексов гистосовместимости. В подавляющем большинстве случаев она вызывает относительно слабый первичный иммунный ответ, который легко подавляется современными иммунодепрессантами.
При ХПН у больных пиелонефритом с частыми обострениями инфекции мочевых путей (более двух в течение 6 мес) подготовка к трансплантации почки включает устранение бактериальной инфекции. При безуспешности антибактериальной терапии и риске генерализации инфекции в посттрансплантационном периоде выполняют плановую билатериальную нефрэктомию. После пересадки почки реципиент получает активную иммуносупрессивную терапию, включающую цитостатики, глюкокортикостероиды и антилимфоцитарные антитела.
Неудачный отдаленный исход трансплантации в 40% случаев связан с необратимым отторжением трансплантата (в 24% – хроническим, в 16% – острым), в остальных случаях – смертью реципиента с функционирующим трансплантатом. Почти в 60% случаев причина смерти реципиента – сердечно-сосудистые и инфекционные осложнения. Средняя 5–летняя выживаемость трансплантата варьирует в пределах 70—80% и в первую очередь зависит от степени тканевой совместимости по антигенам системы HLA, адекватности иммуносупрессивной терапии, а также от вида трансплантации.
Соавтор – И.А. Добросмыслов, врач-нефролог