Что такое симпатическое влияние на сердце
Что такое симпатическое влияние на сердце
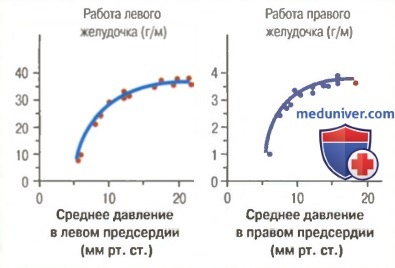
Группа кривых, которые отражают функциональную способность желудочков перекачивать кровь. На рисунке показана зависимость работы желудочков во время систолы от среднего давления в предсердиях. По мере роста давления в каждом предсердии работа желудочков увеличивается, пока не достигнет предельной величины.
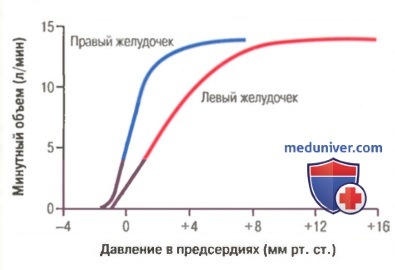
На рисунке показана зависимость минутного объема желудочков от среднего давления в предсердиях. По мере роста давления в правом и левом предсердиях минутный объем соответствующего желудочка также увеличивается.
Обратите внимание, что обе группы кривых также демонстрируют механизм Франка-Старлинга: наполнение желудочков кровью при более высоком предсердном давлении приводит к увеличению объема каждого желудочка, увеличению силы его сокращения и, следовательно, увеличению объема крови, поступающей из желудочков в артерии.
Контроль сократительной функции сердца симпатическими и парасимпатическими нервами
Стимулирующее влияние симпатических нервов на сердце. Симпатическая стимуляция может увеличить частоту сердечных сокращений у здорового молодого человека от 70 до 180-200 уд/мин, а иногда даже до 250 уд/мин. Кроме того, симпатические нервы увеличивают силу сердечных сокращений примерно в 2 раза, что приводит к увеличению ударного объема и систолического давления. Таким образом, симпатическая стимуляция способна увеличить сердечный выброс в 2-3 раза (дополнительно к изложенному механизму Франка-Старлинга).
С другой стороны, торможение симпатических нервов сердца слабо влияет на его насосную функцию. Снижение сердечного выброса происходит не более чем на 30%. Это объясняется низкой частотой постоянной тонической импульсации, идущей по симпатическим нервам к сердцу.
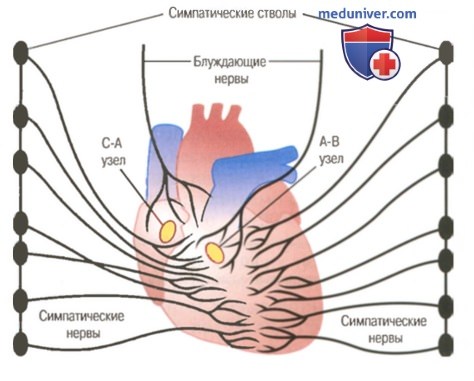
Влияние парасимпатических нервов на сердце. Стимуляция парасимпатических волокон в составе блуждающего нерва способна остановить сердцебиение на несколько минут; затем сердце «ускользает» из-под влияния блуждающих нервов и сокращается с частотой 20-40 уд/мин все время, пока продолжается стимуляция нервов. Кроме того, блуждающие нервы уменьшают силу сокращений сердца на 20-30%. Волокна блуждающего нерва в основном иннервируют предсердия, но не желудочки. Этот факт объясняет значительное влияние вагусной стимуляции на частоту сердечных сокращений и слабое ее влияние на силу сокращений. Тем не менее, суммарный эффект этих влияний выражается в снижении сердечного выброса на 50% и более.
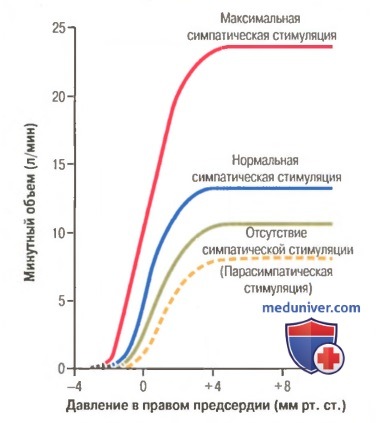
Влияние симпатических и парасимпатических нервов на кривые рабочей активности сердца. На рис.унке представлены четыре кривые, отражающие насосную функцию сердца, а не отдельного желудочка. Эти кривые показывают связь между давлением на входе в правые отделы сердца (т.е. в правом предсердии) и сердечным выбросом (из левого желудочка в аорту).
На рисунке видно, что при любом уровне давления в правом предсердии сердечный выброс увеличивается под влиянием симпатических нервов и уменьшается под влиянием парасимпатических нервов. Изменение величины сердечного выброса каждый раз происходит как за счет изменения частоты сердечных сокращений, так и за счет изменения силы сердечных сокращений.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Нарушения сердечного ритма
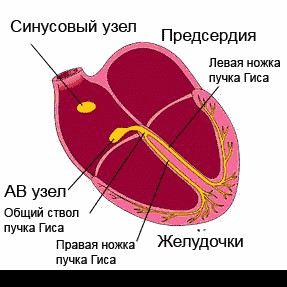
Сердце человека в нормальных условиях бьется ровно и регулярно. Частота сердцебиения в минуту при этом составляет от 60 до 90 сокращений. Данный ритм задается синусовым узлом, который называется также водитель ритма. В нем имеются пейсмекерные клетки, от которых возбуждение передается далее на другие отделы сердца, а именно на атрио-вентрикулярный узел, и на пучок Гиса непосредственно в ткани желудочков.
Данное анатомо-функциональное разделение важно с позиции типа того или иного нарушения, потому что блок для проведения импульсов или ускорение проведения импульсов могут возникнуть на любом из этих участков.
Нарушения ритма сердца и его проводимости носят название аритмий и представляют собой состояния, когда сердечный ритм становится меньше нормы (менее 60 в минуту) или больше нормы (более 90 в минуту). Также аритмией является состояние, когда ритм является нерегулярным (неправильным, или несинусовым), то есть исходит из любого участка проводящей системы, но только не из синусового узла.
Классификация
Все нарушения ритма и проводимости классифицируются следующим образом:
В первом случае, как правило, происходит ускорение сердечного ритма и/или нерегулярное сокращение сердечной мышцы. Во втором же отмечается наличие блокад различной степени с урежением ритма или без него.
В целом к первой группе относятся нарушение образования и проведения импульсов:
Причины аритмии сердца
Причины аритмии (возникновения нарушений ритма сердца) настолько многообразны, что перечислить абсолютно все является очень трудной задачей. Тем не менее, во многих случаях именно от причины аритмии зависит ее безопасность для жизни больного, дальнейшая тактика лечения.
Предложено множество различных классификаций причин аритмии, однако ни одна из них в настоящее время не является общепринятой. Наиболее приемлемой для пациента мы считаем следующую классификацию. Она основывается на признаке наличия или отсутствия у больного первичного заболевания сердца. Если имеется заболевание сердца, аритмию называют органической, а если заболевания сердца нет — неорганической. Неорганические аритмии принято также называть функциональными.
Органические аритмии
К органическим аритмиям относятся:
Функциональные аритмии
Это также достаточно большая группа, включающая:
Одинаково ли проявляются нарушения ритма сердца?
Все нарушения ритма и проводимости клинически проявляют себя по разному у разных пациентов. Часть больных никаких симптомов не ощущает и узнает о патологии только после планового проведения ЭКГ. Эта часть больных незначительна, так как в большинстве случаев пациенты отмечают явную симптоматику.
Так, для нарушений ритма, сопровождающихся учащенным сердцебиением (от 100 до 200 ударов в мин), особенно для пароксизмальных форм, характерно резкое внезапное начало и перебои в сердце, нехватка воздуха, болевой синдром в области грудины.
Некоторые нарушения проводимости, например пучковые блокады, ничем не проявляются и распознаются только на ЭКГ. Синоатриальная и атрио-вентрикулярная блокады первой степени протекают с незначительным урежением пульса (50-55 в мин), из-за чего клинически могут проявляться лишь незначительной слабостью и повышенной утомляемостью.
Блокады 2 и 3 степени проявляются выраженной брадикардией (меньше 30-40 в мин) и характеризуются кратковременными приступами потери сознания.
Кроме этого, любое из перечисленных состояний может сопровождаться общим тяжелым состоянием с холодным потом, с интенсивными болями в левой половине грудной клетки, снижением артериального давления, общей слабостью и с потерей сознания. Эти симптомы обусловлены нарушением сердечной гемодинамики и требуют пристального внимания со стороны врача.
Разновидности аритмий
Большинство людей под аритмией подразумевает беспорядочные сокращения сердечной мышцы («сердце бьется, как захочет»). Однако это не совсем так. Врач этот термин использует при любом нарушении сердечной деятельности (урежение или учащение пульса), поэтому виды аритмий можно представить следующим образом:
По частоте сердечного ритма различают 3 формы мерцательной аритмии:
На ЭКГ при МА зубец Р не регистрируется, потому что нет возбуждения предсердий, а определяются только предсердные волны f (частота 350-700 в минуту), которые отличаются нерегулярностью, различием формы и амплитуды, что придает электрокардиограмме своеобразный вид.
Причиной МА могут быть:
Частота встречаемости трепетания предсердий (ТП) в 20-30 раз ниже, чем МА. Для него также характерны сокращения отдельных волокон, но меньшая частота предсердных волн (280-300 в минуту). На ЭКГ предсердные волны имеют большую амплитуду, чем при МА.
Интересно, что на одной ЭКГ можно видеть переход мерцания в трепетание и наоборот.
Причины возникновения трепетания предсердий аналогичны причинам формирования мерцания.
Симптомы мерцания и трепетания часто отсутствуют вообще, но иногда отмечаются некоторые клинические проявления, вызванные беспорядочной деятельностью сердца или симптомы основного заболевания, В общем, яркой клинической картины такая патология не дает.
Синдром слабости синусового узла
Эта патология возраст не выбирает, однако предпочитает определенные условия:
Заподозрить синдром слабости синусового узла можно по характерным для него признакам:
Последствием синдрома дисфункции синусового узла является внезапное возникновение приступа Адамса-Морганьи-Стокса и асистолия (остановка сердечной деятельности).
Медикаментозное лечение этого синдрома сводится к применению атропина, изадрина, препаратов белладонны. Однако, учитывая, что эффект от консервативного лечения, как правило, небольшой, больным показана имплантация постоянного кардиостимулятора.
Атриовентрикулярная (АВ) блокада — нарушение проведения возбуждения в желудочки из предсердий, с задержкой или прекращением проведения импульса. Она зачастую является спутницей воспалительных и дегенеративных процессов, происходящих в сердечной мышце, инфаркта миокарда или кардиосклероза. Повышенный тонус блуждающего нерва тоже играет определенную роль в формировании атриовентрикулярной блокады.
Атриовентрикулярная блокада, являясь последствием органических поражений сердца, сама дает еще худшие осложнения, в результате которых значительно возрастает опасность летального исхода. Если атриовентрикулярная блокада 1 ст. лечится путем воздействия на основное заболевание, то АВ блокада может переходить в полную, что нарушает кровоснабжение жизненно важных органов, которое приводит к развитию сердечной недостаточности. А это уже плохое последствие, поэтому лечение откладывать нельзя, больного госпитализируют и назначают препараты, стимулирующие сердечную деятельность в инъекционных растворах с постоянным наблюдением за состоянием пациента. Если брадикардия резко выраженная, отмечается тяжелая сердечная недостаточность, больному в экстренном порядке имплантируют искусственный водитель ритма.
ВЛИЯНИЕ ВЕГЕТАТИВНОЙ НЕРВНОЙ РЕГУЛЯЦИИ НА РАЗВИТИЕ СЕРДЕЧНЫХ АРИТМИЙ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА
1 Кандидат медицинских наук, ассистент кафедры, 2 Кандидат медицинских наук, ассистент кафедры, 3 Кандидат медицинских наук, ассистент кафедры, Доктор медицинских наук, Профессор, заведующий кафедрой, Ярославский государственный медицинский университет
ВЛИЯНИЕ ВЕГЕТАТИВНОЙ НЕРВНОЙ РЕГУЛЯЦИИ НА РАЗВИТИЕ СЕРДЕЧНЫХ АРИТМИЙ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА
Аннотация
У больных сердечно-сосудистыми заболеваниями, особенно ишемической болезнью сердца (ИБС), отмечается выраженное ремоделирование миокарда, происходит перестройка вегетативной нервной системы сердца. Это ведет к нарушению как симпатических, так и парасимпатических регуляторных влияний. Рассогласования между электрофизиологическими процессами в миокарде, эфферентной импульсацией из центральных структур и состоянием афферентных связей, а также дисфункция самих центральных нервных структур могут служить причиной электрической нестабильности миокарда и способствовать возникновению фатальных нарушений сердечного ритма, приводящих к наступлению кардиальной смерти.
Ключевые слова: вегетативная нервная система, ишемическая болезнь сердца, электрическая нестабильность миокарда, нарушения ритма сердца.
Lysenkova N.O. 1 , Rumyancev M.I. 2 , Zhilina A.N. 3 , Kratnov A.E. 4
1 MD, assistant of the Department of therapy of pediatric faculty, 2 MD, assistant of the Department of therapy of pediatric faculty, 3 MD, assistant of the Department of therapy of pediatric faculty, 4 MD, Professor, Head of the Department of therapy of pediatric faculty, Yaroslavl State Medical University
THE INFLUENCE OF AUTONOMIC NERVOUS REGULATION ON THE DEVELOPMENT OF CARDIAC ARRHYTHMIAS IN PATIENTS WITH CORONARY HEART DISEASE
Abstract
In patients with cardiovascular diseases, especially coronary heart disease, there is a marked remodeling of the myocardium, there is a rearrangement of the autonomic nervous system of the heart. This leads to disruption of both sympathetic and parasympathetic regulatory influences. The mismatch between electrophysiological processes in the myocardium, with efferent impulses from the central agencies and the state of the afferent connections, and also themselves dysfunction of the central nervous structures can cause electrical instability of the myocardium and lead to fatal cardiac arrhythmias leading to cardiac death occurrence.
Keywords: autonomic nervous system, coronary heart disease, electrical instability of the myocardium, arrhythmias.
Одной из актуальных проблем современной кардиологии является своевременное определение у больных ИБС риска развития угрожающих жизни аритмий и наступления кардиальной смерти [1]. Данные клинических и морфологических исследований доказывают тесную взаимосвязь развития кардиальной смерти с наличием фатальных нарушений ритма, дисфункцией ВНС, нейрогуморальными механизмами, и сниженной ФВ левого желудочка у больных ИБС [17]. Определяющим условием для возникновения фатальных аритмий признается наличие структурной патологии сердца, которое под действием различных функциональных факторов становится электрически нестабильным [25]. Кроме того, существуют данные, согласно которым нестабильность электрофизиологических процессов в миокарде у пациентов, страдающих ИБС, в первую очередь связана с нарушением регуляции вегетативного и электролитного баланса [7, 19].
Сердце иннервируется вегетативной нервной системой (ВНС), состоящей из симпатических и парасимпатических нервов. Симпатические нервы, стимулируя β-адренорецепторы синусового узла, увеличивают частоту сердечных сокращений (ЧСС). Раздражение блуждающего нерва, в свою очередь, стимулирует М-холинорецепторы синусового узла, вследствие чего развивается брадикардия. Синусовый и атриовентрикулярный узлы находятся в основном под влиянием блуждающего нерва и, в меньшей степени, симпатического, в то время как желудочки контролируются преимущественно симпатическим нервом [28, 37]. Деятельность ВНС контролируется центральной нервной системой и рядом гуморальных влияний. В продолговатом мозге расположен сердечно-сосудистый центр, который объединяет парасимпатический, симпатический и сосудодвигательный центры. Регуляция этих центров осуществляется подкорковыми узлами и корой головного мозга. На ритмическую деятельность сердца влияют импульсы, исходящие из сердечно-аортального, синокаротидного и других сплетений. Также на сердечно-сосудистый центр действуют гуморальные нарушения, изменения в крови (парциального давления углекислого газа и кислорода, кислотно-основного состояния), хеморецепторный рефлекс [11]. В состоянии покоя доминирует тонус вагуса и изменчивость сердечной периодики в значительной степени зависит от его влияний. Вагусная и симпатическая активность находятся в постоянном взаимодействии. Поскольку синусовый узел богат холинэстеразой, действие любого вагусного импульса краткосрочно, так как ацетилхолин быстро гидролизируется. Преобладание парасимпатических влияний над симпатическими может быть объяснено двумя независимыми механизмами: холинергически индуцируемым снижением высвобождения норадреналина в ответ на симпатическую стимуляцию и холинергическим подавлением ответа на адренергический стимул. Афферентная вагусная стимуляция приводит к рефлекторному возбуждению эфферентной вагусной активности и ингибированию эфферентной симпатической активности [37]. Эффекты противоположно ориентированного рефлекса опосредуются стимуляцией афферентной симпатической активности [33]. Эфферентная вагусная активность также находится под тоническим сдерживающим влиянием афферентной кардиальной симпатической активности [16]. Эфферентная симпатическая и вагусная импульсации, направленные на синусовый узел, характеризуются разрядом, преимущественно синхронизированным с каждым сердечным циклом.
Литературные данные о роли вегетативной регуляции в аритмогенезе неоднозначны. В последнее время активно обсуждается положение о том, что повышение активности симпатического звена ВНС при ишемии миокарда приводит к возникновению нарушений ритма, тогда как активация парасимпатического звена обладает протективным эффектом [36]. Однако, при гистологическом исследовании миокарда у пациентов, погибших внезапно, было выявлено нарушение автономной регуляции, обширные очаги истощения катехоламинов в адренергических сплетениях миокарда и изменения вегетативных нервных ганглиев. Показано, что ишемические изменения в области нижней стенки левого желудочка вызывают активацию парасимпатического отдела ВНС, а в передней стенке приводят к повышению тонуса симпатических афферентных нервов [3].
Известно, что у больных ИБС, отмечается выраженное ремоделирование миокарда, происходит перестройка вегетативной нервной системы сердца. Это ведет к нарушению как симпатических, так и парасимпатических регуляторных влияний. Особого внимания заслуживает активация симпатоадреналовой системы и снижение активности парасимпатического отдела ВНС, связанные как с развитием общего адаптационного синдрома, так и со значительной структурной перестройкой миокарда, что обуславливает увеличение электрической нестабильности, склонность к возникновению фатальных нарушений сердечного ритма [2, 9, 10, 18], тем самым повышается риск кардиальной смерти.
Известно, что вагусное влияние понижает порог возникновения угрожающих жизни желудочковых аритмий и обеспечивает “антиаритмическую защиту”, возможно, путем снижения возбудимости кардиомиоцитов, а симпатическое, напротив, повышает этот порог, что приводит к более частым аритмическим осложнениям. Выявлено, что в остром периоде инфаркта миокарда (ИМ) наблюдается повышение тонуса симпатической нервной системы и снижение тонуса парасимпатической. В ряде исследований выявлено, что снижение вагусной активности или нарушение баланса влияний ВНС на синусовый ритм в пользу симпатического отдела, наблюдаемое уже в ранние сроки обострения ИБС, сопряжено с тяжестью заболевания и сохраняется не менее 6-12 месяцев [12, 15, 29]. Есть основания полагать, что этот дисбаланс связан с повышенным риском развития тяжелых осложнений и смерти: так, существуют свидетельства проаритмического эффекта уменьшения вагусных или повышения симпатическихвлияний на сердце, а также защитного действия противоположных изменений активности ВНС [10].
Исследования показали, что большинству эпизодов ишемии миокарда (61,8%) предшествовали значимые изменения тонуса ВНС (симпатической – 61,9%, парасимпатической – 38,1%). Остальные эпизоды (38,8%) возникали на фоне неизмененной активности ВНС. Установлено, что повышение активности симпатической нервной системы достоверно уменьшает продолжительность эпизодов безболевой ишемии миокарда и увеличивает длительность приступов спонтанной стенокардии [4]. Органические изменения миокарда, особенно ИМ, вносят значительные изменения в регуляторные процессы автономной нервной системы вследствие развития “вегетативной денервации” сердца. Нарушение вегетативной регуляции сердечно-сосудистой системы может быть обусловлено усилением симпато-симпатических [13, 31, 32] и симпато-вагальных рефлексов [37]. Изменение геометрических свойств пораженного миокарда приводит к усилению афферентной симпатической стимуляции вследствие механического раздражения нервных окончаний и рефлекторному ослаблению парасимпатических влияний на сердце [31]. Также снижается ответ клеток синусового узла на изменение нейрорегуляторных механизмов.
Достаточно хорошо освещен обсуждаемый в течение длительного времени вклад ВНС в генезис нарушений ритма сердца и внезапной кардиальной смерти у больных ИБС [14]. Известно, что по мере прогрессирования ИБС зоны ишемии, а также фиброза и кардиосклероза становятся более чувствительными к воздействию катехоламинов и поэтому реагируют на малейшие изменения симпатического тонуса [27]. В последние годы выявлено, что очаговые повреждения нервных волокон в желудочках сердца у больных с перенесенным ИМ могут приводить к нарушению реполяризации и, таким образом, способствовать электрической нестабильности миокарда [7, 8].Обнаружено, что при ИМ и нестабильной стенокардии нарушения симпатической иннервации сердца превышают по площади и глубине зоны нарушенной перфузии, что объясняется большей чувствительностью нейрональных окончаний к ишемии. Предполагается, что усиление адренергических влияний на кардиомиоциты у больных с ОКС происходит вследствие снижения захвата симпатическими окончаниями сердца поступающего из кровотока норадреналина [7].
Известно, что нервная регуляция стабилизирует электрическую активность сердца. Повреждения внутрисердечных нервных волокон и ганглиев могут лежать в основе серьезных нарушений образования импульсов, проведения возбуждения и нарушения процессов реполяризации миокарда. Длительные сравнительные клинические и патологоанатомические наблюдения свидетельствуют о том, что у больных с ВКС нервные волокна часто изменены вблизи проводящей системы сердца [20, 21]. Также встречаются очаговые повреждения нервных волокон в желудочках сердца, которые могут приводить к нарушению реполяризации и способствовать электрической нестабильности миокарда [42]. В литературе описаны связи между нервными волокнами и кардиомиоцитами, особенно расположенными вблизи проводящей системы, где в большом количестве проходят периферические нервы [22, 23, 43]. Не исключено, что поражение нервных сплетений в желудочках сердца, где определяется большое количество симпатических нервов [41], вызывают нарушения реполяризации из-за изменения адренергических нервных влияний. Вблизи синусового узла могут повреждаться как симпатические, так и парасимпатические нервные элементы, и естественно предположить, что поражения нервных волокон разной медиаторной природы будет вызывать противоположное действие.
Таким образом, эпидемиологические, клинические и морфологические данные убедительно доказывают, что регуляция ВНС является одним из наиболее важных механизмов, стабилизирующих электрическую активность сердца. А повреждения внутрисердечных нервных волокон и ганглиев у больных ИБС, могут лежать в основе серьезных нарушений ритма сердца.
Что такое симпатическое влияние на сердце
Влияние симпатических нервов на сердце проявлется в виде положительного хронотропного и положительного инотропного эффекта. Сведения о наличии тонических влияний симпатической нервной системы на миокард основываются в основном на хронотропных эффектах.
Электрическая стимуляция волокон, отходящих от звездчатого ганглия, вызывает увеличение ритма сердца и силы сокращений миокарда (см. рис. 9.17). Под влиянием возбуждения симпатических нервов скорость медленной диастолической деполяризации повышается, снижается критический уровень деполяризации клеток водителей ритма синоатриального узла, уменьшается величина мембранного потенциала покоя. Подобные изменения увеличивают скорость возникновения потенциала действия в клетках водителей ритма сердца, повышают его возбудимость и проводимость. Эти изменения электрической активности связаны с тем, что выделяющийся из окончаний симпатических волокон медиатор норадреналин взаимодействует с B1-адренорецепторами поверхностной мембраны клеток, что приводит к повышению проницаемости мембран для ионов натрия и кальция, а также уменьшению проницаемости для ионов калия.
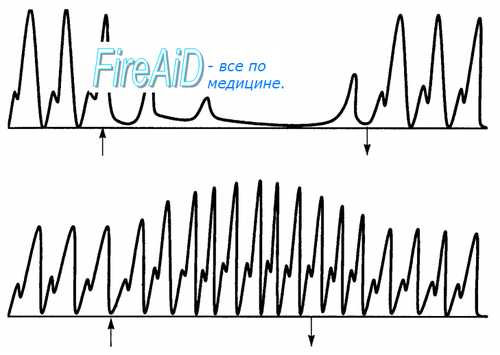
Ускорение медленной спонтанной диастолической деполяризации клеток водителей ритма, увеличение скорости проведения в предсердиях, атриовентрикулярном узле и желудочках приводит к улучшению синхронности возбуждения и сокращения мышечных волокон и к увеличению силы сокращения миокарда желудочков. Положительный инотропный эффект связан также с повышением проницаемости мембраны для ионов кальция. При увеличении входящего тока кальция возрастает степень электромеханического сопряжения, в результате чего увеличивается сократимость миокарда.
Менее изучено участие в регуляции сердечной деятельности интракардиальных ганглиозных нервных элементов. Известно, что они обеспечивают передачу возбуждения с волокон блуждающего нерва на клетки синоат-риального и атриовентрикулярного узлов, выполняя функцию парасимпатических ганглиев. Описаны инотропные, хронотропные и дромотропные эффекты, полученные при стимуляции этих образований в условиях эксперимента на изолированном сердце. Значение этих эффектов в естественных условиях остается неясным.