Что такое синдром лауна ганонга левина
Синдром преждевременного возбуждения
Синдром преждевременного возбуждения – это ускорение проведения нервного возбуждения в желудочки из предсердий по аномальным дополнительным путям. Проявляется характерными изменениями на ЭКГ-ленте и пароксизмальной тахиаритмией.
Патология является результатом врожденных нарушений в проводящей системе сердца. Синдром WPW (синдром Вольфа-Паркинсона-Уайта) встречается приблизительно у 2% населения, синдром LGL (синдром Лауна-Ганонга-Левина) в среднем у 0,6% взрослого населения. Примерно у 30% людей с тахиаритмией наблюдается наличие дополнительных проводящих путей. Патология может наблюдаться в любом возрасте.
Причины возникновения
Признаки появления синдрома
Виды синдрома преждевременного возбуждения
В эту группу аритмий входят синдром Лауна-Ганонга-Левина (синдром LGL, короткого интервала PQ), синдром Вольфа-Паркинсона-Уайта (WPW-синдром).
Соколова С.В., терапевт. Кардиология в ОН КЛИНИК: как снизить риск наступления инфаркта.
Симптоматика и постановка диагноза
Диагноз специалист может установить на основании жалоб, анамнеза, данных осмотра и ЭКГ. Заболевание имеет приступообразное течение и для него характерны следующие симптомы:
Синдром преждевременного возбуждения не имеет характерных симптомов, кроме связанных с тихиаритмией. У молодых людей симптоматика будет минимальной, даже при высокой частоте сердечных сокращений.
На основании жалоб пациента и осмотра кардиолог ОН КЛИНИК назначает проведение:
Лечение синдрома преждевременного возбуждения в ОН КЛИНИК
Из немедикаментозных методов врач назначает вагусные пробы. Они основаны на стимуляции блуждающего нерва, замедляющего ритм сердца. К вагусным пробам относят массаж каротидного синуса, надавливание на глазные яблоки, натуживание, погружение в холодную воду лица. Эти процедуры необходимо выполнять только после рекомендаций кардиолога.
Лекарственную терапию назначают после обследования. Его можно пройти в отделении кардиологии ОН КЛИНИК – быстро и с максимальным комфортом.
Медикаменты назначаются для каждого пациента с учетом индивидуальных особенностей организма и наличия сопутствующих болезней. В сложных клинических случаях решается вопрос о проведении электрической кардиоверсии.
Специалисты ОН КЛИНИК также информируют пациентов об образе жизни, рассказывают:
ОН КЛИНИК предлагает лечение, консультирование и реабилитацию в комфортных для пациентов условиях.
Не стоит ждать, пока приступ пройдет сам – заболевание опасно развитием осложнений.
Синдром преждевременного возбуждения, синдром Вольфа-Паркинсона, Лауна-Ганонга-Левина
Синдром преждевременного возбуждения — это заболевание, при котором желудочки сердца деполяризуются слишком рано, что приводит к их частичному преждевременному сокращению.
Это состояние является аномалией предсердно-желудочкового возбуждения. Данная аномалия может выражаться в следующих состояниях:
Как правило, предсердия и желудочки электрически изолированы, и электрический контакт между ними существует только в «желудочковом узле». При любом типе синдрома преждевременного возбуждения присутствует еще один проводящий путь.
С физиологической точки зрения нормальная электрическая волна задерживается на атриовентрикулярном узле, чтобы предсердия, а затем и желудочки, могли сократиться. Однако задержки волны в данном узле не происходит, и электрический импульс попадает в желудочек через желудочно-кишечный тракт быстрее, чем обычным путем — через пучок Гиса. Поэтому желудочки деполяризуются (приходят в возбужденное состояние) преждевременно.
Синдром Вольфа-Паркинсона
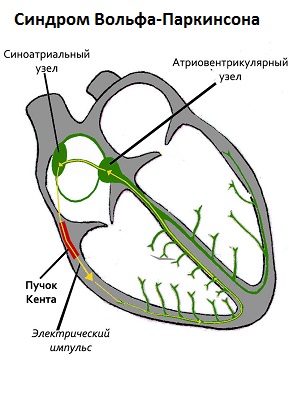
Синдром Вольфа-Паркинсона (или Вольфа-Паркинсона-Уайта, синдром WPW) был впервые описан в 1930 году. Врачи Вольф, Уайт и Паркинсон описали ряд медицинских случаев, при которых пациенты подвергались тахикардическим атакам и имели характерные отклонения на электрокардиограмме. В настоящее время синдром Вольфа-Паркинсона-Уайта определяется как врожденное заболевание. Для него характерна аномальная проводимость сердечной ткани между предсердиями и желудочками, проявляющаяся в возвратной тахикардии и суправентрикулярной тахикардии. Участок, являющийся причиной заболевания, называется пучок Кента. Он может быть расположен между двумя предсердиями и соединяется с одним любым желудочком.
Единственной причиной синдрома Вольфа-Паркинсона является врожденное наличие пучка Кента. Эта аномалия носит генетический характер. Экологических факторов, способствующих появлению данного порока, не выявлено. Четко прослеживается лишь одна закономерность — наследственная передача дефекта через поколение или в каждом поколении.
Рисунок 1. Синдром Вольфа-Паркинсона
Заболевание может проявиться в любом возрасте, и его симптомы зависят от множества факторов, в том числе и от общего состояния здоровья, возраста, веса и хронических заболеваний.
Основные клинические проявления синдрома Вольфа-Паркинсона:
Важным фактором развития заболевания является возраст. При таких сопутствующих факторах, как атеросклероз, ожирение, диабет вероятность развития синдрома Вольфа-Паркинсона сильно возрастает.
Симптомы синдрома Вольфа-Паркинсона у детей младшего возраста:
Может присутствовать интеркуррентное (случайно присоединяющееся к основному) воспалительное заболевание.
Симптомы у детей старшего возраста:
Для диагностики данного заболевания необходимы не только визуализационные исследования, но и анализ крови — биохимический, электролитный. Визуализационные методы включают телеметрию, холтеровский мониторинг, электрокардиограмму.
Стресс-тестирование является вспомогательным методом диагностики и может помочь определить тахикардию и эффективность антиаритмической лекарственной терапии.
Лечение синдрома Вольфа-Паркинсона проводится несколькими методами:
Кроме того, проводится лечение, направленное на устранение ишемических симптомов, кардиомиопатии, перикардита, электролитных нарушений, заболеваний щитовидной железы и анемии — эти заболевания нередко сопровождают аномалии предсердно-желудочкового возбуждения и осложняют лечение основного заболевания.
Лекарственные препараты, используемые для лечения синдрома Вольфа-Паркинсона:
Дозировка определяется врачом.
Хирургическое вмешательство
Катетерная радиочастотная абляция практически отменила необходимость хирургического вмешательства на открытом сердце. Однако операция всё еще проводится, в особенности таким пациентам:
Долгосрочная антиаритмическая терапия основана на использовании таких лекарственных препаратов, как флекаинид, пропафенон, амиодарон, соталол; дозировка всех средств определяется врачом.
Синдром Лауна-Ганонга-Левина
Синдром Лауна-Ганонга-Левина (LGL) — это заболевание, для которого характерны приступы тахикардии, перемещающиеся длительными периодами нормального сердцебиения. Это заболевание относится к классу аномалий предсердно-желудочкового возбуждения, как и синдром Вольфа-Паркинсона.
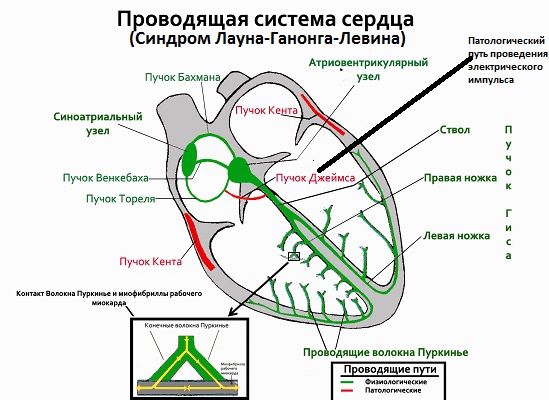
О структурных аномалиях, лежащих в основе синдрома Лауна-Ганонга-Левина известно намного меньше, чем о синдроме Вольфа-Паркинсона. Основная теория возникновения заболевания базируется на существовании интранодальных или паранодальных волокон, которые обходят весь атриовентрикулярный узел или его часть. Эти волокна получили название пучка Джеймса.
Ранее медики довольно часто приписывали наличие синдрома Лауна-Ганонга-Левина тем пациентам, у которых фиксировались короткие приступы тахикардии на фоне общей нормальной функции сердца. Однако позднее врачи пришли к выводу, что при отсутствии тахикардии в течение длительного времени пациенты могли считаться здоровыми.
PR-интервал – это промежуток, через который первичный электрический импульс Р достигает правого желудочка. Этот промежуток на ЭКГ не отображается из-за отсутствия электрической активности в процессе его осуществления.
Показатель QRS — это общая картина, которую может продемонстрировать электрокардиограмма. Благодаря этому виду диагностики врачи могут установить, нормально ли работает сердце, а также определить продолжительность задержек, то есть, PR-интервалов.
Впервые заболевание было описано в 1938 году — врачи Левин, Кларк и Критеско описали возникновение частых приступов тахикардии у пациентов с коротким интервалом PR и общим нормальным QRS. В 1952 году врачи Лаун, Ганонг и Левин, чьи фамилии фигурируют в настоящем названии синдрома, определили существование волокон, которые берут начало в нижней части предсердия и заканчиваются в нижней части атриовентрикулярного узла — это и есть пучок Джеймса.
Основным критерием синдрома Лауна-Ганонга-Левина является PR-интервал меньше или равный 0,12 (120 мс).
Рисунок 2. Синдром Лауна-Ганонга-Левина
Единственной причиной синдрома Лауна-Ганонга-Левина является врожденное наличие пучка Джеймса. Эта аномалия носит генетический характер. Экологических факторов, способствующих появлению данного порока, не выявлено. Четко прослеживается лишь одна закономерность — наследственная передача дефекта через поколение или в каждом поколении.
Лечение
Специфического и четко определенного метода лечения синдрома Лауна-Ганонга-Левина не существует. В зависимости от степени развития заболевания и симптоматической картины, а также возраста, пола, общего состояния здоровья больного, схема лечения может отличаться, как и интенсивность симптомов. Основной упор лечения делается на устранение тахикардии.
В случае гемодинамической нестабильности наличие тахикардии является причиной для госпитализации. Диетических ограничений при данном заболевании не требуется, однако необходимо исключить алкоголь, контролировать вес и уровень сахара в крови.
Почему превышение уровня витамина D опасно для жизни?
Ученые определили группу крови, при которой чаще всего развивается слабоумие
Обнаружены условия, при которых образуется супериммунитет к COVID-19
5 привычек, которые сокращают продолжительность нашей жизни
Склонность человека к мигрени развивается еще в утробе матери
Любовь к черному шоколаду и горькому кофе определяется генами
Синдром преждевременного возбуждения (I45.6)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Синдромы предвозбуждения (преждевременного возбуждения) желудочков представляют собой результат врожденных нарушений в проводящей системе сердца, связанных с наличием дополнительных аномальных проводящих путей между миокардом предсердий и желудочков, часто сопровождаются развитием пароксизмальных тахикардий.
В клинической практике наиболее часто встречаются 2 синдрома (феномена) предвозбуждения:
Клиническое значение синдромов предвозбуждения определяется тем, что при их наличии нарушения сердечного ритма (пароксизмальные тахикардии) развиваются часто, протекают тяжело, иногда с угрозой для жизни больных, требуя особых подходов к терапии.
Диагностика синдромов предвозбуждения желудочков основывается на выявлении характерных признаков ЭКГ.
Синдром CLC (Клерка — Леви — Кристеско) обусловлен наличием дополнительного аномального пути проведения электрического импульса (пучка Джеймса) между предсердиями и пучком Гиса.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Существует два типа синдрома WPW:
Этиология и патогенез
Синдромы предвозбуждения желудочков обусловлены сохранением в результате незавершенной в эмбриогенезе перестройки сердца дополнительных путей проведения импульса.
Наличие дополнительных аномальных проводящих путей при синдроме WPW (пучки, или пути, Кента) является наследственным нарушением. Описана связь синдрома с генетическим дефектом в гене PRKAG2, расположенном на длинном плече 7 хромосомы в локусе q36. Среди кровных родственников больного распространенность аномалии повышена в 4-10 раз.
Синдром WPW нередко (до 30% случаев) сочетается с врожденными пороками сердца и другими сердечными аномалиями такими как аномалия Эбштейна (представляет смещение трикуспидального клапана в сторону правого желудочка с деформацией клапанов; генетический дефект при этом предположительно локализован на длинном плече 11 хромосомы), а также стигмами эмбриогенеза (синдром дисполазии соединительной ткани). Известны семейные случаи, при которых чаще встречаются множественные дополнительные пути и повышен риск внезапной смерти. Возможны сочетания синдрома WPW с генетически детерминированной гипертрофической кардиомиопатией.
Проявлению синдрома WPW способствуют нейроциркуляторная дистония и гипертиреоз. Синдром Вольффа—Паркинсона—Уайта может проявляться также на фоне ИБС, инфаркта миокарда, миокардитах различной этиологии, ревматизме и ревматических пороках сердца.
Синдром СLC также является врожденной аномалией. Изолированное укорочение интервала PQ без пароксизмальных наджелудочковых тахикардий может развиваться при ИБС, гипертиреозе, активном ревматизме и носит доброкачественный характер.
Суть синдрома (феномена) преждевременного возбуждения желудочков состоит в аномальном распространении возбуждения от предсердий к желудочкам по так называемым дополнительным путям проведения, которые в большинстве случаев частично или полностью «шунтируют» АВ-узел.
В результате аномального распространения возбуждения часть миокарда желудочков или весь миокард начинают возбуждаться раньше, чем это наблюдается при обычном распространении возбуждения по АВ-узлу, пучку Гиса и его ветвям.
В настоящее время известны несколько дополнительных (аномальных) путей АВ-проведения:
Наличие дополнительных (аномальных) путей приводит к нарушению последовательности деполяризации желудочков.
Образовавшись в синусовом узле и вызвав деполяризацию предсердий, импульсы возбуждения распространяются к желудочкам одновременно через предсердно-желудочковый узел и добавочный проводящий путь.
В связи с отсутствием физиологической задержки проведения, свойственной АВ-узлу, в волокнах добавочного пути распространившийся по ним импульс достигает желудочков раньше, чем тот, который проводится через АВ-узел. Это обусловливает укорочение интервала PQ и деформацию комплекса QRS.
Однако основное клиническое значение дополнительных путей проведения состоит в том, что они нередко включаются в петлю кругового движения волны возбуждения (re-entry) и способствуют, таким образом, возникновению наджелудочковых пароксизмальных тахикардий.
В настоящее время предлагается преждевременное возбуждение желудочков, не сопровождающееся возникновением пароксизмальной тахикардии, называть “феноменом предвозбуждения”, а случаи, когда имеются не только ЭКГ-признаки предвозбуждения, но и развиваются пароксизмы наджелудочковой тахикардии — “синдромом предвозбуждения”, однако ряд авторов не согласны с таким разделением.
Как уже упоминалось выше, при синдроме WPW аномальный импульс возбуждения распространяется по пучку Кента, который может быть расположен справа или слева от атриовентрикулярного узла и пучка Гиса. В более редких случаях аномальный импульс возбуждения может распространяться через пучок Джеймса (соединяет предсердие с конечной частью АВ узла или с началом пучка Гиса), или пучок Махайма (проходит от начала пучка Гиса к желудочкам). При этом ЭКГ имеет ряд характерных особенностей:
Эпидемиология
Признак распространенности: Крайне редко
Распространённость синдрома WPW составляет по разным данным от 0.15 до 2%, синдром СLC выявляется приблизительно у 0.5% взрослого населения.
Наличие дополнительных путей проведения обнаруживают у 30% пациентов с суправентрикулярной тахикардией.
Чаще синдромы предвозбуждения желудочков встречаются среди мужчин. Синдромы предвозбуждения желудочков могут проявляться в любом возрасте.
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Клинически синдромы предвозбуждения желудочков не имеют специфических проявлений и сами по себе не оказывают влияния на гемодинамику.
Клинические проявления синдромов предвозбуждения могут наблюдаться в различном возрасте, спонтанно или после какого-либо заболевания; до этого момента пациент может быть асимптоматичен.
Синдром Вольффа-Паркинсона-Уайта часто сопровождается различными нарушениями сердечного ритма:
У больных с синдромом CLC также имеется повышенная склонность к возникновению пароксизмальных тахикардий.
Диагностика
Характерные особенности ЭКГ при синдроме WPW
ЭКГ при синдроме WPW (тип А):
ЭКГ при синдроме WPW (тип Б):
Синдромы CLC и WPW часто являются причиной ложноположительных результатов при проведении нагрузочных проб.
В связи с распространением в последние годы хирургических методов лечения больных с синдромом WPW (деструкция аномального пучка) постоянно совершенствуются способы точного определения его локализации. Наиболее эффективными являются методы внутрисердечного ЭФИ, в частности эндокардиальное (предопреационное) и эпикардиальное (интраоперационное) картирование.
При этом с помощью сложной методики определяют область наиболее ранней активации (предвозбуждения) миокарда желудочков, которая соответствует локализации дополнительного (аномального) пучка.
Электрофизиологическое исследование сердца (ЭФИ) используется у пациентов с синдромом WPW в следующих целях:
— С целью оценки электрофизиологических свойств (способности к проведению и рефрактерные периоды) дополнительных аномальных путей и нормальных проводящих путей.
— С целью определения количества и локализация добавочных путей, что необходимо для проведения дальнейшей высокочастотной аблации.
— С целью выяснения механизма развития сопутствующих аритмий.
— С целью оценки эффективности медикаментозной или аблационной терапии.
В последние годы с целью точного определения локализации аномального пучка применяют методику поверхностного многополюсного ЭКГ-картирования сердца, которая в 70–80% случаев также позволяет ориентировочно определить местоположение пучков Кента. Это существенно сокращает время интраоперационного выявления дополнительных (аномальных) пучков.
Дифференциальный диагноз
Осложнения
Осложнения синдромов предвозбуждения желудочков
К факторам риска внезапной смерти при WPW-синдроме относят:
— Длительность минимального интервала RR при мерцательной аритмии менее 250 мс.
— Длительность эффективного рефрактерного периода дополнительных путей менее 270 мс.
— Левосторонние дополнительные пути или несколько дополнительных путей.
— Наличие симптоматичной тахикардии в анамнезе.
— Наличие аномалии Эбштейна.
— Семейный характер синдрома.
— Рецидивирующее течение синдромов предвозбуждения желудочков.
Лечение
Синдромы предвозбуждения желудочков не требуют лечения при отсутствии пароксизмов. Однако необходимо наблюдение, так как нарушения ритма сердца могут проявиться в любом возрасте.
Купирование пароксизмов ортодромной (с узкими комплексами) реципрокной наджелудочковой тахикардии у больных с синдромом WPW проводят также, как и других наджелудочковах реципрокных тахикардий.
Антидромные (с широкими комплексами) тахикардии купируются аймалином 50 мг (1.0 мл 5% раствора); эффективность аймалина при пароксизмальных наджелудочковых тахикардиях неуточненной этиологии заставляет с большой вероятностью подозревать WPW. Может быть эффективно также введение амиодарона 300 мг, ритмилена 100 мг, новокаинамида 1000 мг.
В случаях, когда пароксизм протекает без выраженных расстройств гемодинамики и не требует экстренного купирования, вне зависимости от ширины комплексов при синдромах предвозбуждения особо показан амидарон.
Препараты IC класса, «чистые» антиаритмики III класса при WPW-тахикардиях не используются в связи с высокой опасностью свойственного им проаритмического эффекта. АТФ может успешно купировать тахикардию, но должен применяться с осторожностью, так как может спровоцировать мерцательную аритмию с высокой ЧСС. Верапамил также следует использовать с особой осторожностью (опасность нарастания ЧСС и трансформации аритмии в мерцание предсердий!) – только у пациентов с успешным опытом его применения в анамнезе.
Мерцание предсердий при участии дополнительных путей проведения представляет реальную опасность для жизни вследствие вероятности резкого учащения сокращений желудочков и развития внезапной смерти. Для купирования фибрилляции предсердий в данной экстремальной ситуации используют амиодарон (300 мг), прокаинамид (1000 мг), аймалин (50 мг) или ритмилен (150 мг). Нередко фибрилляции предсердий с высокой ЧСС сопровождается выраженными нарушениями гемодинамики, что обусловливает необходимость в неотложной электрической кардиоверсии.
Радиочастотная катетерная абляция добавочных путей является в настоящее время основным методом радикального лечения синдрома преждевременного возбуждения желудочков. Перед выполнением абляции проводятэлектрофизиологическое исследование (ЭФИ) для точного определения места нахождения добавочного пути. При этом следует иметь в виду, что таких путей может быть несколько.
Успех лечения, даже при наличии нескольких добавочных путей, достигается примерно в 95 % случаев, а частота осложнений и летальность составляют менее 1 %. Одним из наиболее тяжелых осложнений является возникновение предсердно-желудочковой блокады высокой степени при попытке абляции добавочного пути, расположенного вблизи предсердно-желудочкового узла и пучка Гиса. Риск рецидивов не превышает 5—8 %. Необходимо отметить большую экономичность катетерной абляции по сравнению с длительной медикаментозной профилактикой и операцией на открытом сердце.
Показания к проведению высокочастотной аблации:
Дилтиазем ретард 180мг 30 шт. капсулы пролонгированного действия
Товары-аналоги
Инструкция по применению Дилтиазем ретард 180мг 30 шт. капсулы пролонгированного действия
Состав, форма выпуска и упаковка
Дилтиазем 180 мг/1 капс.
Вспомогательные вещества: сахарная крупка (сахароза, патока крахмальная), сополимер метилметакрилата, триметиламмониоэтилметакрилата и этилакрилата (1:2:0.1) сополимер метилметакрилата, триметиламмониоэтилметакрилата хлорида и этилакрилата (1:2:0.2), парафин, тальк.
Состав оболочки капсулы: титана диоксид, краситель солнечный закат желтый, краситель пунцовый (Понсо 4R), краситель синий патентованный, краситель бриллиантовый черный, желатин.
Фармакотерапевтическая группа
Дилтиазем является производным бензотиазепинов; обладает антиаритмической, антиангинальной и гипотензивной активностью. Блокатор «медленных» кальциевых каналов (БМКК), снижает внутриклеточное содержание кальция в кардиомицитах и клетках гладкой мускулатуры, расширяет коронарные и периферические артерии и артериолы, снижает общее периферическое сосудистое сопротивление (ОПСС), тонус гладкой мускулатуры, усиливает коронарный, мозговой и почечный кровоток, урежает частоту сердечных сокращений (ЧСС).
Антиаритмическое действие обусловлено подавлением транспорта ионизированного кальция в тканях сердца, что приводит к увеличению эффективного рефрактерного периода и удлинению времени проведения в атриовентикулярном (AV) узле (имеет клиническое значение у больных с синдромом слабости синусового узла, пациентов пожилого возраста, у которых блокада кальциевых каналов может препятствовать генерации импульса в синусовом узле и вызывать синоатриальную (SA) блокаду. Нормальный предсердный потенциал действия или внутрижелудочковое проведение не изменяются (на нормальный синусовый ритм обычно не влияет), но при снижении амплитуды сокращения предсердий скорость деполяризации и скорость проведения уменьшаются. Антероградный эффективный рефрактерный период в дополнительных обходных пучках проведения может укорачиваться.
Антиангинальное действие обусловлено расширением периферических сосудов и снижением системного артериального давления (постнагрузки), что приводит к уменьшению напряжения стенки миокарда и его потребности в кислороде. В концентрациях, не приводящих к появлению отрицательного инотропного эффекта, вызывает релаксацию гладкой мускулатуры коронарных сосудов и дилатацию как крупных, так и мелких артерий.
Антигипертензивное действие обусловлено дилатацией резистивных сосудов и снижением ОПСС. Степень снижения артериального давления (АД) коррелирует с его исходным показателем (у пациентов с нормальным АД отмечается минимальное влияние на АД). Снижает АД как в положении «лежа», так и «стоя». Редко вызывает постуральную артериальную гииотензию и рефректорную тахикардию. Не изменяет или незначительно снижает максимальное ЧСС при нагрузке. Длительная терапия не приводит к гиперкатехоламинемии, увеличению активности ренин-ангиотензин-альдостероновой системы (РААС). Уменьшает почечные и периферические эффекты ангиотензина II. Улучшает диастолическое расслабление миокарда при артериальной гипертензии, ишемической болезни сердца, гипертрофической кардиомиопатии, снижает агрегацию тромбоцитов.
Обладает минимальным действием на гладкую мускулатуру желудочно-кишечного тракта (ЖКТ). В течение длительной (8 мес.) терапии не развивается толерантность. Не влияет на липидный профиль крови.
Максимальная выраженность гипотензивного эффекта достигается в течение 2 недель.
Фармакокинетика
После всасывания из ЖКТ активное вещество подвергается интенсивному метаболизму, вследствие эффекта «первого прохождения» преимущественно через печень. В печени метаболизируется путем деацетилирования и деметилирования (при участии изоферментов CYPЗА4, CYP3A5 и CYP3A7) с образованием активного метаболита дезацетилдилтиазема, который определяется в плазме крови в 5-10 раз меньшей концентрации, чем исходный дилтиазем, и имеет в 2-4 раза меньшую активность.
Выводится через кишечник с желчью (65%) и почками (35%, в том числе 2-4% в неизмененном виде).
Фармакокинетика дилтиазема при длительном применении не изменяется. Дилтиазем не кумулирует и не индуцирует собственный метаболизм.
У больных стенокардией и нарушенной функцией почек фармакокинетика дилтиазема не изменяется. У больных с печеночной недостаточностью увеличивается биодоступность и удлиняется T1/2. В пожилом возрасте также может быть снижен клиренс дилтиазема. Не выводится при гемодиализе и перитонеальном диализе.