Плацента неоднородная что это
Плацента является ценнейшим органом женского организма во время беременности. Главными функциями ее является доставка плоду необходимое количество питательных веществ и обеспечение его кислородом. Нормальное течение беременности, а также роды напрямую зависят от состояния развития детского места. Кроме того, эмбриональный орган выполняет защитные функции, предотвращая попадание к ребенку различных инфекций, и следит за снабжением его достаточным количеством гормонов, которые позволяют плоду расти и развиваться.
Диагностика состояния плаценты крайне важна и должна проводиться на протяжении всей беременности с помощью ультразвукового исследования (УЗИ).
Этот метод позволяет своевременно обнаружить какие-либо отклонения в развитии эмбрионального органа. И чем быстрее обнаружены патологии, тем больше шансов на успешное лечение. С помощью УЗИ доктора определяют степень зрелости плаценты, ее структуру, местоположение, толщину. В ходе такого исследования будущей матери может быть поставлен диагноз – неоднородная структура плаценты.
Причины неоднородности
В большинстве случаев неоднородная структура эмбрионального органа не должна быть поводом для беспокойства, т.к. является нормой. Окончательное формирование плаценты приходится на 16 неделю беременности, после чего вплоть до тридцатой недели ее структура должна находиться неизменной. И если в это время в структуре детского места происходят какие-либо изменения (доктор может обнаружить эхонегативные участки, или другие включения), то эти изменения могут стать поводом к серьезным нарушениям функционирования плаценты.
Основными причинами таких нарушений может стать наличие в организме роженицы какой-либо инфекции или последствия употребления спиртных напитков, анемия, курение и т.д. Неоднородная структура плаценты может спровоцировать нарушение кровотока между беременной и плодом, результатом чего станет замедление внутриутробного развития ребенка, гипоксии, тяжелые роды. Если во время УЗИ после 30 недели обнаружены изменения структуры детского места, то в этом нет ничего страшного, а беременность протекает нормально. Иногда нормой считаются изменения плаценты, которые выявлены на 27 неделе, это при условии, что ребенок продолжает развиваться в полной мере и согласно своему сроку. При исследовании ультразвуком могут быть обнаружены следующие явления, связанные с нарушением структуры детского места:
Лечение
Неоднородная структура детского места может быть связанна с гипоплазией или гиперплазией плаценты, а также ее преждевременном старении. В этом случае могут быть назначены дополнительные исследования, такие как допплер, кардиотокография.
Полное восстановление неоднородной структуры плаценты невозможно. Однако, существуют медикаментозные средства, которые нормализуют тонус матки, доставку кислорода, улучшают кровообращение. Также положительное действие оказывают отсутствие стрессовых ситуаций, всевозможных беспокойств. А залогом нормального течения беременности является своевременное проведение необходимой диагностики, правильное питание и здоровый образ жизни.
Плацентарная недостаточность
Большинство женщин знают, что плацента связывает маму и малыша во время беременности и при помощи нее к малышу поступают питательные вещества и кислород.
Бывают ли такие ситуации, когда плацента перестает правильно и полноценно выполнять свою функцию? Можно ли как то предотвратить это?
Какую функцию выполняет плацента
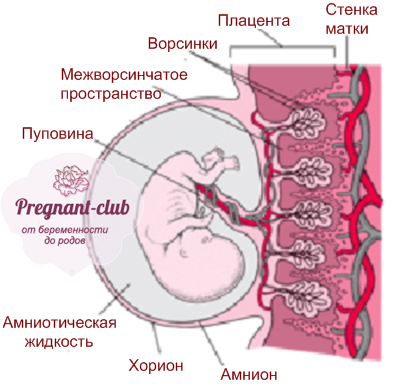
Внутри ворсин течет кровь малыша, а снаружи они омываются кровью матери. Между кровотоком мамы и малыша расположен всего один слой клеток, который и играет роль барьера между организмом матери и ребенка. Благодаря этой мембране кровь матери и плода не смешивается.
Однако в последние годы стало известно, что клетки крови плода все-таки проникают через плацентарный барьер в кровоток матери и благодаря этому стало возможным проведение генетических анализов и определение хромосомных аномалий, резуса фактора и пола плода по крови беременной женщины (неинвазивный пренатальный тест).
В плаценте происходит постоянный обмен веществ между мамой и ребенком. Из материнской крови к плоду поступает кислород и питательные вещества, от плода обратно к матери углекислый газ и продукты обмена, подлежащие выведению из организма.
Важной функцией плаценты является выработка гормонов и биологически активных веществ. В первую очередь это гормоны, важные для успешного вынашивания беременности, например хорионический гонадотропин, плацентарный лактоген, эстрогены и др.
К сожалению, не всегда все складывается вполне благополучно. В силу самых различных причин на разных сроках беременности могут происходить отклонения в развитии и функционировании плаценты. Изменения эти никогда не проходят бесследно для мамы и малыша, а зачастую имеют грозные последствия.
Если плацента перестает выполнять свои функции в полной мере, развивается так называемая плацентарная недостаточность. По сути, она заключается в ухудшении кровообращения в системе мать-плацента-плод.
Виды и причины плацентарной недостаточности
Врачи различают острую и хроническую плацентарную недостаточность:
Острая плацентарная недостаточность
Это состояние, требующее экстренного вмешательства врачей. Она характеризуется стремительным ухудшением плацентарного кровотока. Острая плацентарная недостаточность возникает в основном в результате отслойки плаценты или гибели отдельных участков ткани плаценты например при образовании тромбов в сосудах. Причиной отслойки может послужить травма живота, антифосфолипидный синдром.
Фосфолипиды – это сложные жиры, которые входят в состав оболочек всех клеток организма. В ряде случаев иммунная система организма вырабатывает большое количество антител к некоторым собственным фосфолипидам и белкам, связывающим эти липиды. Они называются антифосфолипидные антитела и при взаимодействии с клетками организма вызывают повреждение клеток и активацию свертывающей системы крови, что приводит к тромбообразованию.
Антифосфолипидный синдром является самой частой причиной тромботических осложнений при беременности, в том числе причиной отслойки плаценты и острой плацентаной недостаточности.
Вызвать отслойку плаценты может также тяжелое течение гестоза – грозного осложнения второй половины беременности, проявляющееся отеками, повышением давления и появлением белка в моче.
Острая плацентарная недостаточность развивается при отслойке более 2/3 поверхности плаценты.
В случае развития острой плацентарной недостаточности необходимо максимально быстро провести операцию кесарева сечения для сохранения жизни малыша и мамы.
Хроническая плацентарная недостаточность
Значительно чаще у беременных женщин встречается хроническая плацентарная недостаточность. В этом случае происходит нарушение формирования и созревания плаценты, уменьшается маточно-плацентарный и плодово-плацентарный кровотоки, ограничивается газообмен и обмен веществ в плаценте, снижается синтез плацентарных гормонов. Все эти изменения определяют недостаточное поступление кислорода и питательных веществ малышу, вызывают задержку роста и развития плода.
Причинами плацентарной недостаточности чаще всего являются перенесенные аборты, особенно хирургический аборт при первой беременности, курение, при этом количество и крепость выкуриваемых сигарет значения не имеют, поскольку на формировании неполноценных сосудов плаценты негативное действие оказывает табачный дым, а не никотин.
В группу риска по развитию плацентарной недостаточности входят также женщины с хроническими заболеваниями, такими как артериальная гипертензия, железодефицитная анемия, пиелонефрит, сахарный диабет, заболевания щитовидной железы.
В последние годы наблюдается значительный рост плацентарной недостаточности, вызванной бактериями, вирусами, грибами. Причиной этого может быть как острая инфекция, перенесенная будущей мамой во время беременности, так и активация хронического инфекционного процесса в организме беременной женщины.
Немаловажное значение в формировании хронической плацентарной недостаточности играет патология матки: эндометриоз, пороки развития матки (седловидная, двурогая). Фактором риска врачи считают также миому матки. Безусловно, целый ряд лекарственных средств оказывает неблагоприятное влияние на формирование плаценты и развитие плода. В настоящее время определен список препаратов, не разрешенных к применению во время беременности.
В некоторых случаях плацентарная недостаточность может быть обусловлена наличием хромосомных нарушений у плода, в частности при синдромах Дауна (наличие дополнительной 21 хромосомы у плода) или синдроме Эдвардса (дополнительная 18 хромосома у плода) уже в ранние сроки беременности диагностируется нарушение функции плаценты.
Следует отметить, что среди осложнений беременности, наиболее часто приводящих к развитию хронической плацентарной недостаточности, существенным фактором является преэклампсия (или поздний гестоз) – это осложнения второй половины беременности, проявляющееся отеками, повышением давления и появлением белка в моче.
Независимо от факторов, способствующих развитию плацентарной недостаточности, в основе ее лежат нарушения кровообращения в маточно-плацентарном комплексе, приводящие к нарушению всех функций плаценты. Следовательно, симптомы хронической плацентарной недостаточности будут обусловлены недостатком поступления кислорода и питательных веществ к плоду.
Это прежде всего, задержка внутриутробного развития плода – отставание размеров плода и замедление темпов его роста. Часто имеют место изменение двигательной активности плода. Сначала может быть некоторое усиление движений, а затем уменьшение. Нарушение защитной функции плаценты приводит к внутриутробному инфицированию плода под действием проникающих через плаценту патогенных (болезнетворных) микроорганизмов. Плод, развитие которого происходит в условиях плацентарной недостаточности, в значительно большей степени подвержен риску травматизации в родах, у них отмечается нарушение адаптации к внеутробной жизни, повышенная заболеваемость в первый год жизни.
По времени возникновения врачи разделяют плацентарную недостаточность на раннюю и позднюю.
Ранняя (или первичная) плацентарная недостаточность
Развивается до 16 недель беременности. Она возникает уже на этапе формирования плаценты и связана с заболеваниями беременной женщины, имеющимися до беременности, к примеру с патологией матки, хронической артериальной гипертензией, эндокринологическими заболеваниями. При этом происходит формированием неполноценных сосудов в плаценте.
Поздняя (или вторичная) плацентарная недостаточность
Возникает после 16 недель беременности и чаще всего связана с заболеваниями, возникшими уже во время беременности. Чаще всего это железодефицитная анемия (то есть снижение концентрации гемоглобина и железа в крови), гестационный сахарный диабет (то есть нарушение усвоения организмом глюкозы, возникшее на фоне беременности), перенесенные вирусные и бактериальные инфекции.
Важным является подразделение плацентарной недостаточности на компенсированную и декомпенсированные формы.
Компенсированная плацентарная недостаточность
Развивается, к примеру, при угрозе прерывания беременности и нетяжелых формах позднего гестоза, в случае, если эти осложнения успешно поддаются медикаментозной коррекции.
Декомпенсированная плацентарная недостаточность
Вызывает развитие задержки развития плода, хронической внутриутробной гипоксии, вплоть до гибели плода.
Диагностика плацентарной недостаточности
Лечить уже развившуюся плацентарную недостаточность практически невозможно, поэтому врачи активно стремятся выявлять беременных женщин, угрожаемых в отношении формирования нарушений функции плаценты. Если плацентарная недостаточность выявляется в 3 триместре беременности, эффективного лечения, к сожалению, не существует. Поэтому очень активно в настоящее время применяются все способы выявления в ранние сроки беременности тех женщин, в формировании плаценты которых произошли нарушения.
В первую очередь, при постановке на учет по беременности выявляют максимально значимые факторы риска – курение, перенесенные аборты, отягощенную наследственность (низкий вес при рождении, склонность к тромбозам), наличие хронических заболеваний сердца, сосудов, сахарного диабета.
Профилактические мероприятия против развития плацентарной недостаточности особенно актуальны и необходимы до 16-17 недель беременности, когда происходит формирование структур плаценты.
Значимую помощь в оценке риска развития плацентарной недостаточности оказывает пренатальный скрининг, который проводится в 11-14 недель беременности. Он проводится для выявления синдромов Дауна, Эдвардса и др. хромосомных болезней у плода. В настоящее время самым актуальным является проведение комплексного ранний скрининг беременной на прогнозирование риска развития плацентарной недостаточности, преэклампсии и внутриутробной задержки развития плода. Поскольку данный вид диагностики относится к самым современным и передовым, к сожалению, он пока не включен в перечень услуг, предоставляемых в женской консультации в рамках ОМС, но доступен всем желающим в центрах пренатальной диагностики.
Определение белков, вырабатываемых плацентой
В первую очередь проводят определение белка РАРР-А, он является также маркером хромосомных аномалий плода. Снижение концентрации РАРР-А в крови в 11-14 недель беременности встречается у беременных женщин, имеющих высокий риск плацентарной недостаточности и задержки развития плода.
Второй гормон плаценты, который помогает в оценке рисков плацентарной недостаточности – PIGF (плацентарный фактор роста). Его концентрация в крови снижается задолго до первых проявлений плацентарной недостаточности. Его определение применяют не настолько широко, как PAPP-A, но тем не менее многие лаборатории уже включили данный белок в пренатальный скрининг 1 триместра. Крайне важное значение при проведении скрининга 1 триместра имеет измерение кровотоков в сосудах матки. Однозначно доказано, что сужение сосудов матки, определяемое при исследовании, свидетельствует о неполноценности формирования плаценты, которое будет ухудшаться с увеличением срока беременности и приведет к снижению питания малыша и снабжения его кислородов, то есть к развитию плацентарной недостаточности и задержки развития плода. При нормальных размерах маточных сосудов в 11-14 недель беременности риск тяжелой плацентарной недостаточности ничтожно мал.
Следующее обязательное скрининговое ультразвуковое исследование проводится в 20-21 неделю беременности. При этом обязательно проводят измерения плода, чтобы оценить, нет ли отставания в росте. Ведь при кислородном голодании замедляются темпы роста плода и размеры его начинают отставать от нормы для каждого срока беременности. Кроме того врач обязательно оценивает состояние и зрелость плаценты. Во время УЗИ проводится также допплерометрия сосудов матки для выявления ранних изменений, предшествующих клиническим проявлениям плацентарной недостаточности.
У пациенток, относящихся к группе высокого риска кроме УЗИ и допплерометрии проводят также суточное мониторирование колебаний артериального давления, определение количества белка в анализе мочи, собранном за сутки, оценивают показатели системы свертывания крови.
Третье УЗИ проводится всем будущим мамам в 30–34 недели беременности. Врач измеряет окружность головы и живота крохи, длину костей его ручек и ножек, и вычисляет предполагаемый вес плода. Эти измерения позволяют доктору убедиться в том, что малыш развивается нормально. Также имеет значение строение плаценты, наличие в ней признаков старения, вследствие чего она обычно перестает полноценно снабжать малыша кровью, а, значит, ему перестает хватать кислорода и питательных веществ и развитие ребенка нарушается. Во время УЗИ оценивается количество и вид околоплодных вод, которые также могут изменяться при внутриутробном страдании плода.
Допплерометрия
Допплерометрия сосудов плаценты и пуповины (метод исследования скоростей кровотоков в этих сосудах) так же позволяет оценить самочувствие малыша. Доктор исследует кровоток в артериях матки, пуповины, сердца и мозга ребенка. Это исследование позволяет определить, хорошо ли работает плацента, нет ли признаков нехватки кислорода у малыша, или развития гестоза у мамы. При снижении скорости кровотока в каком-либо сосуде можно говорить о нарушениях питания плода различной степени тяжести.
Вовремя проведенное обследование позволяет выявить начальные стадии дефицита кровоснабжения. В таких случаях лечение сможет предотвратить грозные осложнения, такие как гипоксия и внутриутробная задержка развития малыша. Допперометрию проводят в 20–21 неделю и в 30-32 недели беременности, при наличии изменений, контроль осуществляют минимум каждые две недели.
Кардиотокография
Это важный метод оценки состояния плода. Проводится КТГ при сроке беременности 33 недели и более, поскольку только на этом этапе внутриутробного развития малыша устанавливается полноценная регуляция деятельности сердечно-сосудистой системы плода центрами спинного и головного мозга. Запись сердцебиений плода проводят в течение 20–40 минут, а при необходимости исследование может быть продлено до 1,5 часов.
Аппарат регистрирует и записывает частоту сердцебиений малыша. Врач акушер-гинеколог оценивает кривую записи сердцебиений, эпизоды урежения и резкого учащения частоты сердечных сокращений плода и на основании этих данных делает заключение о том, насколько комфортно малыш чувствует себя в животе у мамы. К примеру, при снижении концентрации кислорода в крови плода, уменьшается и его поступление к клеткам нервной системы, что в свою очередь отражается на частоте сердечных сокращений. При нормальном течении беременности КТГ проводят после 33 недели 1 раз в 10–14 дней, иногда чаще. В некоторых клиниках в настоящее время предлагается услуга постоянного КТГ-мониторирования, что приобретает актуальность при наличии признаков плацентарной недостаточности. Беременной женщине выдается мониторчик, который регистрирует изменения сердечной деятельности малыша и эти данные по интернету передаются лечащему врачу.
Лечение плацентарной недостаточности
Специфических способов лечения плацентарной недостаточности в настоящее время не существует, поскольку нет лекарственных препаратов, которые избирательно улучшают маточно-плацентарный кровоток. Именно поэтому все меры борьбы с плацентарной недостаточностью направлены на профилактику. Если пациентка относится к группе высокого риска по развитию плацентарной недостаточности, с раннего срока беременности ей назначают лекарственные препараты, эффективность которых хорошо доказана и которые предупреждают раннее развитие выраженных нарушений функции плаценты.
Если во время проведения дополнительных методов оценки состояния плода выявляются начальные нарушения поступления кислорода к малышу, проводится медикаментозное лечение, направленное на увеличение притока крови и кислорода через плаценту и обязательные контрольные обследования на фоне проводимой терапии. Если изменения серьезные и малыш испытывает выраженный дефицит кислорода и питательных веществ, состояние его страдает, то в таких случаях проводится экстренное родоразрешение.
Плацента неоднородная что это
Плацента — это орган, объединяющий мать и плод. От функционирования плаценты зависит развитие и состояние плода. Существует множество методов исследования функции плаценты. Тем не менее самым информативным остается осмотр последа после его рождения. Такой осмотр помогает в оценке состояния новорожденного, а также в выборе тактики ведения послеродового периода. Плаценту осматривают сразу после родов — в первую очередь для того, чтобы оценить ее целостность. Затем более тщательно изучают весь послед. Пуповинную кровь для анализа берут сразу после пересечения пуповины, еще до рождения последа. Послед необходимо осматривать во всех без исключения случаях.
Исследование плаценты и пуповины
I. Размеры и вес плаценты
А. Вес плаценты при доношенной беременности составляет 1/6—1/7 веса плода. Зрелая плацента имеет вид диска диаметром 15—20 см и толщиной 2—3 см. Вес ее в среднем составляет 400—600 г.
Б. Гиперплазия плаценты. Вес плаценты при этом составляет 1/3—1/2 веса плода. Гиперплазия плаценты встречается при гемолитической болезни новорожденных, врожденном сифилисе и сахарном диабете классов A—C по классификации П. Уайт (см. гл. 9, п. I.В.1). Умеренная гиперплазия плаценты встречается у заядлых курильщиц.
В. Гипоплазия плаценты наблюдается у женщин, страдающих гипертонической болезнью и артериальной гипертонией беременных. Гипоплазия плаценты часто сочетается с внутриутробной задержкой развития.
II. Пуповина имеет длину 50—70 см. При осмотре обращают внимание на наличие узлов и прикрепление пуповины (к плаценте или плодным оболочкам), отмечают число сосудов пуповины. Если длина пуповины меньше 40 см, говорят об абсолютной короткости пуповины. Это состояние может сопровождаться серьезными осложнениями во время родов через естественные родовые пути.
А. Истинные узлы пуповины встречаются в 1% родов. Перинатальная смертность при этом достигает 6%. Истинные узлы пуповины образуются при чрезмерно длинной пуповине, когда плод вследствие значительной подвижности проскальзывает через ее виток. В родах эта патология проявляется брадикардией у плода. Ложные узлы пуповины представляют собой утолщения отдельных участков пуповины вследствие резкого закручивания пупочных артерий или варикозного расширения пупочной вены. Ложные узлы пуповины не представляют опасности для плода.
Б. Обвитие пуповины вокруг шеи плода встречается в 20—24% родов, обычно при пуповине длиной более 70 см. Обвитие пуповины, как правило, не представляет опасности для плода. На КТГ во время родов могут появиться децелерации.
В. Прикрепляется пуповина обычно к центральной части плаценты.
1. В большинстве случаев краевого прикрепления пуповины (см. рис. 29.1) роды проходят без осложнений. Однако попытка выделения последа путем потягивания за пуповину может привести к ее отрыву.
2. Оболочечное прикрепление пуповины
а. При этом пуповина прикрепляется не к самой плаценте, а к плодным оболочкам на некотором расстоянии от края плаценты. Сосуды направляются от корня пуповины по оболочкам к плаценте (см. рис. 29.2). Если участок оболочек с проходящими по нему сосудами располагается над внутренним зевом ниже предлежащей части плода, говорят о предлежании сосудов. Эту патологию можно заподозрить, когда излитие околоплодных вод сопровождается кровотечением. Диагноз подтверждают при обнаружении эритроцитов плода в мазке содержимого заднего свода влагалища, окрашенном по Клейхауэр—Бетке, или с помощью экспресс-анализов. Лечение заключается в экстренном родоразрешении. В отдельных случаях при рождении ребенка в состоянии выраженной анемии и гипоксии ему непосредственно после родов производят переливание препаратов крови. При многоплодной беременности оболочечное прикрепление пуповины может осложниться кровопотерей у одного или обоих плодов.
б. Риск оболочечного прикрепления пуповины при одноплодной беременности составляет 1%. При двойне и, особенно, при тройне он значительно выше.
Г. Агенезия одной из пупочных артерий
1. Распространенность этой патологии при одноплодной беременности составляет 0,2—1,1%. К факторам риска относят сахарный диабет и трисомии у матери. В 25—50% случаев заболевание сочетается с другими пороками развития — расщелиной неба, пороками сердца, почек, мочевых путей, половых органов и опорно-двигательного аппарата. Дети чаще рождаются маловесными. Пороки развития, как правило, множественные, и ребенок зачастую нежизнеспособен. При выявлении агенезии одной из пупочных артерий проводят тщательное обследование новорожденного.
2. При двойне эта патология наблюдается у одного из близнецов в 7% случаев. Однако риск врожденных пороков при этом значительно ниже, чем при одноплодной беременности.
III. Материнская поверхность плаценты
А. Кровотечение в послеродовом периоде
1. Задержка в матке фрагмента плаценты — частая причина послеродового кровотечения. Диагноз ставят при осмотре материнской поверхности плаценты. На задержку дольки или части дольки указывает дефект ткани плаценты. Показано немедленное ручное или инструментальное обследование стенок полости матки под общей анестезией.
2. Задержка в матке добавочной дольки плаценты — см. гл. 29, п. IV.Е.
Б. Ретроплацентарные сгустки крови и гематомы
1. Наиболее частые причины появления сгустков крови на материнской поверхности плаценты перечислены ниже.
а. Разрыв краевого синуса — наиболее вероятная причина кровотечения из половых путей в III триместре беременности (в отсутствие предлежания и преждевременной отслойки плаценты). При осмотре сгустки крови обнаруживают у одного из краев плаценты.
б. Преждевременная отслойка плаценты. При осмотре плаценты на материнской поверхности обнаруживают плотно прикрепленный к ней сгусток крови, размеры которого соответствуют площади отслойки. Внешний вид и консистенция сгустка зависят от того, сколько времени прошло после отслойки. Застарелая гематома обычно плотная, при отделении ее на плаценте остается тарелкообразное углубление. Сгустки крови на материнской поверхности плаценты могут обнаруживаться и при преэклампсии (клиническая картина преждевременной отслойки плаценты при этом часто отсутствует).
2. Лечение заключается в родоразрешении. Диагноз подтверждают после осмотра плаценты.
В. Отложение фибрина в межворсинчатом пространстве наблюдается при физиологическом созревании плаценты и особенно выражено при переношенной беременности. Отложение фибрина имеет вид множественных белесоватых очажков на материнской поверхности плаценты. Они плотные на ощупь, особенно если произошло обызвествление.
Г. Инфаркты плаценты выглядят как четко отграниченные очаги плотной консистенции (см. рис. 29.3). Инфаркты чаще располагаются в толще плаценты, реже — на ее материнской поверхности. На срезе очага можно определить давность инфаркта (свежий — с кровоизлияниями или старый — с признаками организации).
1. Небольшие краевые инфаркты наблюдаются в норме при физиологическом старении плаценты в результате ее атрофии. Чаще инфаркты плаценты встречаются при гипертонической болезни или преэклампсии.
2. Свежий инфаркт имеет темно-багровый цвет, нечеткие контуры, его основание граничит с децидуальной оболочкой. По мере старения он уплотняется, приобретает беловатый или бледно-желтый цвет и становится хорошо отграниченным от окружающих тканей.
3. Инфаркты развиваются вследствие микротромбозов или длительного спазма спиральных артерий эндометрия. К инфарктам плаценты также предрасполагают атеросклеротические изменения более крупных артерий на фоне артериальной гипертонии. Осложнения инфарктов плаценты — внутриутробная гипоксия и внутриутробная задержка развития. Инфаркты нередко обнаруживают при преждевременной отслойке плаценты.
IV. Плодовая поверхность плаценты
А. Оболочки, покрывающие плодовую поверхность плаценты, тонкие, прозрачные, синевато-стального цвета.
1. Окрашивание оболочек меконием наблюдается в 20% родов, обычно при переношенной беременности. Оболочки при этом приобретают буровато-зеленоватый цвет. В этой группе новорожденных повышена ранняя детская смертность. Ее причины — аспирация мекония и другие осложнения переношенности, а также внутриутробная задержка развития.
2. Хориоамнионит. Оболочки утолщены, белесоватые, непрозрачные, иногда с резким неприятным запахом.
Б. Субхориальное отложение фибрина встречается в норме и считается признаком зрелости плаценты. На плодовой поверхности определяются серо-белые наложения плотной консистенции и различного диаметра, располагающиеся одиночно или группами.
В. Субхориальные кисты — тонкостенные полости диаметром 4—5 см, заполненные серозным или слизистым содержимым, иногда с примесью крови. Расположены на плодовой поверхности плаценты. Встречаются в норме.
1. Определение. На поверхности амниона обнаруживают серовато-желтые наложения диаметром 2—3 мм, особенно многочисленные в области прикрепления пуповины (см. рис. 29.4). Наложения состоят из слущенного эпидермиса плода и легко удаляются.
2. Обследование. Узловатый амнион встречается при маловодии и обычно сочетается с пороками развития почек и мочевых путей (двусторонняя агенезия почек, поликистоз почек, обструкция мочевых путей). В связи с этим об обнаружении узловатого амниона обязательно сообщают неонатологу.
Д. Амниотические бляшки. На плодовой поверхности плаценты определяются зоны метаплазии цилиндрического эпителия амниона в многослойный плоский в виде мелких сероватых бляшек с зернистой поверхностью. В отличие от узловатого амниона, бляшки удаляются с трудом. Амниотические бляшки обычно наблюдаются при доношенной беременности. Они представляют собой результат физиологических изменений ткани плаценты.
1. Определение. Добавочные дольки формируются из ткани трофобласта, не подвергшейся атрофии, и могут располагаться на некотором расстоянии от плаценты. При этом добавочные дольки соединяются с плацентой оболочками, по которым проходят сосуды (см. рис. 29.5). Задержка добавочной дольки в матке после рождения последа может вызвать кровотечение.
2. Диагностика и лечение. Оборванные сосуды на краях плаценты свидетельствуют о том, что имеется добавочная долька плаценты, оставшаяся в матке. Для удаления добавочной дольки проводят ручное или инструментальное обследование стенок полости матки под общей анестезией.
Ж. Плацента, окруженная валиком (placenta circumvallata), формируется в результате отслойки и скручивания краев плаценты в ранние сроки беременности. При этом гладкий хорион располагается в виде валика вокруг хориальной пластинки (см. рис. 29.6). Если отслойка и скручивание произошли по самому краю плаценты, формируется плацента, окруженная ободком (placenta marginata).
1. Клиническая картина. В большинстве случаев проявления отсутствуют и плаценту, окруженную валиком, обнаруживают случайно при осмотре последа. Могут наблюдаться кровотечения и подтекание околоплодных вод в течение беременности, преждевременные роды, пороки развития и перинатальная гибель плода.
2. Диагностика и лечение. Клинические проявления — повышение тонуса матки, подтекание околоплодных вод и кровотечение — появляются в конце II или начале III триместра беременности. Этиотропного лечения не существует. Беременность может закончиться преждевременными родами.
Послед при многоплодной беременности
А. Бихориальные биамниотические близнецы. Каждый близнец имеет собственные хорион и амнион. Перегородка между полостями, в которых находятся плоды, состоит из двух амнионов (тонких прозрачных оболочек) и двух гладких хорионов, лежащих между ними. Для уточнения диагноза показано гистологическое исследование перегородки.
Б. Монохориальные биамниотические близнецы. Оба амниона заключены в один общий для обоих близнецов хорион. Перегородка между плодами состоит из оболочек двух амнионов. Диагноз подтверждают с помощью гистологического исследования перегородки.
В. Монохориальные моноамниотические близнецы. Амниотическая полость общая для обоих близнецов, перегородки нет. Пуповины обоих плодов прикрепляются к плаценте очень близко друг от друга, вследствие чего возможно их перекручивание и гибель плодов.
Г. Прогноз. Перинатальная смертность среди монохориальных близнецов выше, чем среди бихориальных. Причина заключается в том, что в общей плаценте формируются анастомозы между сосудами кровеносных систем близнецов. В зависимости от вида анастомозов (артериоартериальные, артериовенозные или веновенозные) и диаметра формирующих их сосудов возможны следующие исходы.
1. Развитие двух нормальных плодов.
2. Фето-фетальная трансфузия, которая проявляется выраженным многоводием одного плода и задержкой развития другого.
3. Нормальное развитие одного плода и тяжелая патология у другого (врожденное отсутствие сердца, мумификация).
VI. Однояйцовые и двуяйцовые близнецы
А. Однояйцовые близнецы. Тип плацентации зависит от того, в какой период формирования плаценты произошло разделение единого эмбрионального зачатка. Возможны все три типа плацентации, описанные выше, но чаще формируется общая плацента. Отдельные плаценты развиваются в 30% случаев.
Б. Двуяйцовые близнецы. При одновременном развитии двух оплодотворенных яйцеклеток всегда формируются отдельные плаценты. Плаценты нередко тесно примыкают друг к другу.
А. Оболочечное прикрепление пуповины наблюдается чаще, чем при одноплодной беременности.
Б. Агенезия одной из пупочных артерий наблюдается в 7% случаев (чаще при одноплодной беременности).
К наиболее распространенным новообразованиям плаценты относят хориоангиому и трофобластическую болезнь.
VIII. Хориоангиома — доброкачественная опухоль, развивающаяся из капилляров плода, входящих в состав ворсин хориона. Размеры опухоли от нескольких миллиметров до 7—8 см в диаметре. При хориоангиоме, особенно больших размеров, возможны многоводие, преэклампсия, преждевременная отслойка плаценты и сердечная недостаточность у матери. Могут встречаться пороки развития плода. В большинстве случаев хориоангиома протекает бессимптомно. Ее обнаруживают случайно при осмотре последа.
IX. Трофобластическая болезнь. Изначально классификация трофобластической болезни была основана на гистологических критериях. В дальнейшем была предложена клиническая классификация, которая учитывает характер течения той или иной формы заболевания. Гистологически различают пузырный занос, деструирующий пузырный занос, хориокарциному и трофобластическую опухоль плацентарной площадки. Клинически выделяют пузырный занос (полный или частичный), злокачественные опухоли трофобласта (деструирующий пузырный занос, хориокарциному) и трофобластическую опухоль плацентарной площадки.
1. Этиология и распространенность. При пузырном заносе ворсины хориона резко увеличены в размерах, отечны. Они представляют собой конгломерат кист, напоминающий грозди винограда (см. рис. 29.7). При микроскопическом исследовании обнаруживают резкое уменьшение количества, вплоть до исчезновения, кровеносных сосудов в строме ворсин хориона и выраженную пролиферацию эпителия ворсин. Выделяют полный и частичный пузырный занос. При частичном пузырном заносе в матке находят элементы плода. Это заболевание обусловлено хромосомными аномалиями, чаще триплоидией, и редко трансформируется в злокачественные опухоли трофобласта. При исследовании ткани полного пузырного заноса (при котором элементы плода отсутствуют) обнаруживают хромосомный набор 46,ХХ, где обе X-хромосомы имеют отцовское происхождение. Причиной могут быть оплодотворение яйцеклетки одновременно двумя сперматозоидами или удвоение хромосом сперматозоида в отсутствие (либо вследствие неполноценности) материнской X-хромосомы. Примерно в 20% случаев полный пузырный занос трансформируется в злокачественные опухоли трофобласта. Распространенность пузырного заноса в Северной Америке и Европе составляет 1 на 1000—1700 беременностей, в Азии и Центральной Америке — несколько выше. В США пузырный занос наблюдается в 1 из 600 случаев искусственного аборта.
а. Возраст. Пузырный занос чаще наблюдается у женщин старше 40 либо моложе 20 лет и не зависит от количества предшествовавших родов.
б. Общие проявления обычно развиваются в течение первых 18 нед беременности и включают следующее.
1) Кровотечение из половых путей встречается практически всегда и может приводить к анемии. Иногда в матке скапливается значительное количество крови.
2) Неукротимая рвота беременных наблюдается в 20—30% случаев. При этом требуется парентеральное введение жидкостей, электролитов и противорвотных средств.
3) Артериальная гипертония развивается в 10—30% случаев. При появлении артериальной гипертонии в ранние сроки беременности в первую очередь исключают пузырный занос.
4) Тиреотоксикоз наблюдается нечасто. При физикальном исследовании отмечаются тахикардия и тремор. Кожа теплая, влажная. Щитовидная железа диффузно увеличена. Хирургическое вмешательство и преэклампсия могут спровоцировать тиреотоксический криз.
5) Эмболия ветвей легочной артерии клетками трофобласта наблюдается в 2—3% случаев. При этом внезапно развиваются кашель, одышка и цианоз.
1) В 50% случаев величина матки опережает срок беременности вследствие пролиферации хориального эпителия, с одной стороны, и скопления крови в полости матки — с другой.
2) Текалютеиновые кисты яичников наблюдаются в 20—40% случаев. Характерно двустороннее увеличение яичников (до 8 см и более). Возможен перекрут ножки кисты.
3. Диагностика. Пузырный занос следует заподозрить при неукротимой рвоте беременных и повышении АД до 24-й недели беременности, а также при обнаружении других характерных проявлений заболевания (см. гл. 29, пп. IX.А.1—2). Выделение из матки отечных, кистозно измененных ворсин хориона — абсолютный признак пузырного заноса, позволяющий сразу поставить диагноз и назначить лечение. Если обнаружить ворсины не удается, используют следующие методы исследования.
б. Уровень ХГ в моче. Пузырный занос исключают, если после 12-й недели беременности суточная экскреция ХГ превышает 500 000 МЕ. Дифференциальную диагностику проводят с многоплодной беременностью. Следует помнить, что при пузырном заносе суточная экскреция ХГ может быть в пределах и даже ниже нормы. Таким образом, этот показатель не может быть основой для постановки диагноза и имеет ориентировочное значение.
в. В последние годы вместо содержания ХГ в моче чаще определяют другой показатель — содержание бета-субъединицы ХГ в сыворотке. В норме он достигает максимума на 12—14-й неделе беременности и обычно не превышает 100 000 МЕ/л. Если уровень бета-субъединицы ХГ в сыворотке более 100 000 МЕ/л, исключают пузырный занос.
а. Вакуум-аспирация — метод выбора для удаления пузырного заноса, особенно если женщина желает в дальнейшем иметь детей. Для расширения канала шейки матки используют палочки ламинарии. Операцию проводят под общей анестезией, используют насадку наибольшего размера. Во время операции вводят окситоцин, 10—20 ед в/в капельно в 1000 мл 5% глюкозы. После вакуум-аспирации производят выскабливание полости матки острой кюреткой. Материал, полученный при вакуум-аспирации и выскабливании, не смешивают и отдельно посылают на гистологическое исследование.
б. Экстирпация матки показана женщинам, не планирующим в дальнейшем иметь детей. Текалютеиновые кисты яичников исчезают самостоятельно после удаления пузырного заноса и снижения уровня бета-субъединицы ХГ в сыворотке.
а. Исход. Выздоровление после удаления полного пузырного заноса наблюдается в 80% случаев. Поскольку у остальных женщин развивается деструирующий пузырный занос или хориокарцинома, огромное значение имеет тщательное наблюдение больных.
1) Рентгенографию грудной клетки проводят перед удалением пузырного заноса, а также через 4 и 8 нед после операции.
2) Бимануальное исследование проводят через 2—4 нед после удаления пузырного заноса, а затем — ежемесячно.
3) Содержание бета-субъединицы ХГ в сыворотке определяют еженедельно до получения трех отрицательных результатов подряд. Несмотря на то что трехкратное обнаружение нормального титра бета-субъединицы ХГ свидетельствует о выздоровлении, после этого исследование проводят ежемесячно в течение полугода, а затем — каждые 2 мес еще в течение полугода. Титр бета-субъединицы ХГ в сыворотке возвращается к норме в среднем через 14 нед после удаления пузырного заноса.
в. Контрацепция. При беременности содержание бета-субъединицы ХГ в сыворотке возрастает и может быть ошибочно расценено как признак рецидива заболевания. В связи с этим в течение всего периода наблюдения женщине рекомендуют воздерживаться от беременности. Назначают пероральные контрацептивы.
а. Рецидив пузырного заноса
1) Распространенность составляет 1 на 50—150 случаев заболевания.
2) При рецидиве пузырного заноса повышается риск деструирующего пузырного заноса и хориокарциномы.
б. Злокачественные опухоли трофобласта. Половина злокачественных опухолей трофобласта развивается в исходе пузырного заноса, 25% — после нормальной беременности, еще 25% — после аборта и внематочной беременности.
1) Предварительный диагноз ставят на основании следующих данных.
а) Титр бета-субъединицы ХГ в сыворотке повышается в 2 и более раз каждые 2 нед.
б) Содержание бета-субъединицы ХГ в сыворотке сохраняется на одном и том же уровне, не снижаясь, на протяжении трех недель. Для оценки динамики снижения уровня бета-субъединицы ХГ в сыворотке после удаления пузырного заноса был предложен график, отражающий средние темпы снижения этого показателя (см. рис. 29.8). Сравнение полученных результатов с графиком позволяет своевременно поставить диагноз даже по неполным данным и избежать гипердиагностики.
в) Содержание бета-субъединицы ХГ в сыворотке через 60 сут после удаления пузырного заноса превышает 500 МЕ/л.
г) Матка увеличена, сохраняются кровянистые выделения из половых путей и текалютеиновые кисты яичников.
д) Округлые тени в легких на рентгенограмме грудной клетки.
е) Метастазы в шейке матки или во влагалище.
ж) Неврологические нарушения (указывают на метастазы в головной мозг).
а) Гинекологическое исследование. Обращают внимание на скорость уменьшения матки, текалютеиновых кист яичников и наличие объемных образований во влагалище.
б) Рентгенография грудной клетки.
в) Исследование крови. Определяют следующие показатели.
i) Уровень гемоглобина, гематокрит, количество эритроцитов и тромбоцитов, лейкоцитарная формула.
iv) Биохимические показатели функции печени.
г) КТ или МРТ печени и головного мозга.
е) УЗИ малого таза для исключения беременности и врастания ворсин хориона в миометрий.
ж) Содержание бета-субъединицы ХГ в сыворотке.
3) Окончательный диагноз. В зависимости от результатов обследования ставят диагноз хориокарциномы или деструирующего пузырного заноса.
Б. Деструирующий пузырный занос
1. Определение. Главный признак деструирующего пузырного заноса — инвазивный рост. Измененные ворсины хориона врастают глубоко в миометрий, иногда прорастая всю стенку матки. Поскольку в процесс вовлекаются вены матки и малого таза, возможно массивное внутрибрюшное кровотечение. Метастазы в легкие, влагалище и наружные половые органы наблюдаются редко.
а. В 75% случаев деструирующий пузырный занос развивается в исходе пузырного заноса, реже — после нормальной беременности, аборта и внематочной беременности.
б. При гистологическом исследовании обнаруживают кистозно измененные ворсины хориона с резко выраженной пролиферацией клеток трофобласта. Кровеносные сосуды в строме ворсин отсутствуют.
а. Назначают метотрексат, 0,3—0,4 мг/кг/сут в/м или в/в в течение 5 сут, или дактиномицин, 0,01—0,012 мг/кг/сут в/в в течение 5 сут.
1) Исчезновение интоксикации, лейко- и тромбоцитопении обычно происходит в течение 5—10 сут после завершения курса химиотерапии. Курс лечения повторяют каждые 2 нед (в отсутствие выраженного побочного действия препаратов, при количестве лейкоцитов выше 1500 мкл –1 и тромбоцитов — выше 100 000 мкл –1 ).
2) Перед каждым курсом химиотерапии определяют биохимические показатели функции печени, АМК и уровень креатинина в сыворотке, повторяют общий анализ крови и бимануальное исследование.
3) После нормализации уровня бета-субъединицы ХГ в сыворотке проводят еще 1—2 курса лечения. После этого уровень бета-субъединицы ХГ определяют ежемесячно в течение года Нормальное содержание бета-субъединицы ХГ в сыворотке свидетельствует о ремиссии.
б. Назначение высоких доз метотрексата в сочетании с фолинатом кальция имеет ряд преимуществ: менее выражено побочное действие, быстрее наступает ремиссия, требуется меньше курсов химиотерапии.
2) После каждого курса химиотерапии трижды в неделю на протяжении двух недель производят общий анализ крови, определяют количество тромбоцитов и биохимические показатели функции печени (в первую очередь активность АсАТ ).
1) Титр бета-субъединицы ХГ в сыворотке определяют еженедельно.
2) Повторный курс лечения показан, если титр бета-субъединицы ХГ в сыворотке повышается или остается неизменным на протяжении 2 нед, а также при выявлении рецидивов или метастазов.
3) Если после первого курса лечения уровень бета-субъединицы ХГ в сыворотке снизился, лечение продолжают в тех же дозах. Если уровень бета-субъединицы ХГ в сыворотке не снижается, дозу метотрексата увеличивают на 0,5 мг/кг, а дозу фолината кальция — на 0,05 мг/кг.
4) При лекарственной устойчивости меняют схему химиотерапии или производят экстирпацию матки (см. гл. 29, п. IX.Б.2.г). Признаки лекарственной устойчивости приведены ниже.
а) Титр бета-субъединицы ХГ в сыворотке повышается.
б) Титр бета-субъединицы ХГ в сыворотке не снижается после двух курсов химиотерапии.
в) Титр бета-субъединицы ХГ в сыворотке не возвращается к норме после четырех курсов химиотерапии.
г. Экстирпация матки. Если больная не собирается больше иметь детей, показана экстирпация матки. Операцию производят на третий день пятидневного курса химиотерапии метотрексатом или дактиномицином. Матку направляют на гистологическое исследование. Больной многократно определяют уровень бета-субъединицы ХГ в сыворотке и, при необходимости, назначают химиотерапию (см. гл. 29, п. IX.Б.2).
д. Осложнения лечения могут возникнуть внезапно и потребовать госпитализации больной.
2) Очаговые некрозы печени, значительное повышение уровня АМК и активности печеночных ферментов.
3) Поражение ЖКТ — стоматит, понос, изъязвление и перфорация.
е. Наблюдение во время ремиссии включает регулярное определение уровня бета-субъединицы ХГ в сыворотке, рентгенографию грудной клетки и бимануальное исследование (см. гл. 29, п. IX.А.5).
ж. Исход последующих беременностей. Лечение деструирующего пузырного заноса не влияет на риск пороков развития и гибели плода.
1. Определение. Хориокарцинома — злокачественная опухоль, которая метастазирует преимущественно гематогенным путем. Метастазы обнаруживают в легких, во влагалище, головном мозге и печени. Окончательный диагноз ставят после гистологического исследования.
а. При гистологическом исследовании обнаруживают, что ткань опухоли не содержит ворсин хориона и представлена скоплениями атипичных эпителиальных и синцитиальных клеток. Строма отсутствует. В опухоли часто наблюдаются вторичные изменения — некрозы и кровоизлияния.
б. В 50% случаев хориокарцинома развивается в исходе пузырного заноса, в остальных — после аборта и нормальных родов.
в. Поскольку строма в опухоли отсутствует, для хориокарциномы характерны атипичные сосуды, построенные из опухолевых клеток. Такие сосуды быстро разрушаются, вызывая кровоизлияния и массивные кровотечения.
г. Заболевание обычно развивается через несколько месяцев после родов или аборта.
2. Обследование (см. гл. 29, пп. IX.А.5—6). Проводят следующие лабораторные и инструментальные исследования.
б. Люмбальная пункция с одновременным определением содержания ХГ в СМЖ и сыворотке (для диагностики метастазов в головной мозг и оценки эффективности лечения).
3. Относительно прогноза монохимиотерапии больных делят на две группы — с низким и с высоким риском лекарственной устойчивости.
а. Критерии низкого риска
1) Суточная экскреция ХГ (до лечения) составляет менее 100 000 МЕ, содержание бета-субъединицы ХГ в сыворотке — ниже 40 000 МЕ/л.
2) Продолжительность заболевания менее четырех месяцев (считая с момента родов, аборта, диагностики пузырного заноса или первых клинических проявлений заболевания).
3) Отсутствие метастазов в печени и головном мозге. Наличие метастазов только в легких или малом тазу.
4) Отсутствие предыдущей химиотерапии.
б. Критерии высокого риска
1) Суточная экскреция ХГ составляет выше 100 000 МЕ, содержание бета-субъединицы ХГ в сыворотке — более 40 000 МЕ/л.
2) Продолжительность заболевания более четырех месяцев.
3) Наличие метастазов в головном мозге или печени.
4) Неэффективность предшествующей химиотерапии.
5) Возникновение заболевания после родов.
4. Лечение в группе низкого риска
а. Лечение такое же, как и при деструирующем пузырном заносе (см. гл. 29, пп. IX.Б.2.а—б).
б. Наблюдение такое же, как и при деструирующем пузырном заносе (см. гл. 29, п. IX.Б.2.в и п. IX.Б.2.е).
в. При неэффективности лечения (появление новых метастазов, отсутствие снижения уровня бета-субъединицы ХГ в сыворотке) показана полихимиотерапия (см. гл. 29, п. IX.В.5), а также пересмотр показаний к экстирпации матки.
5. Лечение в группе высокого риска включает полихимиотерапию в комбинации с лучевой терапией или хирургическим лечением.
а. Основные принципы ведения больных в группе высокого риска — непрерывное лечение и наблюдение, длительная поддерживающая терапия.
1) При использовании обеих схем лечения возможны тяжелые осложнения. Могут развиться лейкопения, тромбоцитопения, сепсис и кровотечение (в брюшную или плевральную полости, а также кровоизлияние в печень, головной или спинной мозг).
2) При одиночных метастазах, особенно в легких, показано хирургическое вмешательство.
в. При снижении уровня бета-субъединицы ХГ в сыворотке до нормы (после получения трех схожих результатов подряд) проводят еще два курса химиотерапии.
г. По окончании лечения уровень бета-субъединицы ХГ в сыворотке определяют каждые 2 нед в течение первых 3 мес, затем — каждые 2 мес в течение следующих 6 мес, а после этого — каждые полгода.
6. Лечение метастазов в головной мозг начинают с лучевой терапии. Затем переходят к полихимиотерапии.
1. У больных деструирующим пузырным заносом и хориокарциномой (группы низкого риска лекарственной устойчивости) 5-летняя выживаемость составляет почти 100%.
2. При хориокарциноме в группе больных с высоким риском лекарственной устойчивости 5-летняя выживаемость составляет лишь 50—80%.
а. При метастазах во влагалище или легкие прогноз лучше, чем при метастазах в головной мозг и печень.
б. При метастазах в головной мозг 5-летняя выживаемость составляет только 50%, при метастазах в печень — еще ниже.
в. Прогноз в значительной степени зависит от количества метастазов и эффективности предыдущих курсов химиотерапии.
Д. Трофобластическая опухоль плацентарной площадки
1. Определение. Трофобластическая опухоль плацентарной площадки — самая редкая из опухолей трофобласта. Она характеризуется достаточно глубоким проникновением хориального эпителия, преимущественно цитотрофобласта, в толщу миометрия. В отличие от хориокарциномы, при трофобластической опухоли плацентарной площадки раздельные пролифераты цито- и синцитиотрофобласта отсутствуют, нет клеточного полиморфизма и атипизма. Ворсины хориона встречаются редко. Клетки опухоли проникают в сосуды и выстилают их изнутри, вытесняя эндотелий, — как при нормальном развитии плаценты.
2. Клиническая картина. Наблюдаются увеличение матки, аменорея или маточные кровотечения. Отмечается умеренное повышение уровня бета-субъединицы ХГ в сыворотке. Больную считают беременной, а отсутствие динамики увеличения матки принимают за несостоявшийся аборт. При прорастании опухолью стенки матки возможно внутрибрюшное кровотечение. Эта опухоль характеризуется выраженным инвазивным ростом и редким метастазированием.
а. С помощью иммуногистохимического исследования в клетках опухоли обнаруживают высокое содержание плацентарного лактогена и незначительное содержание бета-субъединицы ХГ в сыворотке.
б. Поскольку при трофобластической опухоли плацентарной площадки уровень бета-субъединицы ХГ в сыворотке повышается незначительно, для оценки эффективности лечения определяют сывороточный уровень плацентарного лактогена.
4. Лечение включает выскабливание полости матки, а в случае рецидива — экстирпацию матки. Опухоль часто устойчива к проводимой химиотерапии. Летальность при наличии метастазов достигает 15—20%.
Многоводие и маловодие
А. Общая характеристика. Распространенность составляет 0,5—1,5%. На 30—37-й неделе беременности количество околоплодных вод не должно превышать 1700 мл. О многоводии говорят, когда при доношенной беременности количество околоплодных вод превышает 2000 мл. Клинические проявления обычно возникают, если объем околоплодных вод превышает 3000 мл.
1. При хроническом многоводии количество вод нарастает медленно. Ниже приведены самые частые причины хронического многоводия.
2) Атрезия пищевода или двенадцатиперстной кишки.
б. У матери. Сахарный диабет, гемолитическая анемия, многоплодная беременность.
в. Особенности сосудов плаценты и пуповины (при однояйцовой многоплодной беременности, хориоангиоме).
2. Острое многоводие встречается значительно реже хронического. Количество околоплодных вод при этом резко увеличивается в течение нескольких часов или суток. Состояние требует активного лечения. Как правило, возникают преждевременные роды. Ребенок обычно погибает вследствие недоношенности.
1. Наблюдается значительное увеличение размеров матки (обычно на 21—37-й неделе беременности).
2. В некоторых случаях появляются боль в животе, одышка и выраженные отеки. Состояние беременной может ухудшиться настолько, что требуется неотложная помощь.
4. Для диагностики пороков развития ЦНС определяют содержание альфа-фетопротеина в околоплодных водах.
5. Определяют содержание пролактина в околоплодных водах. Его снижение относительно нормы для данного срока беременности указывает на многоводие.
1. При удовлетворительном состоянии беременной и отсутствии пороков развития плода показано амбулаторное лечение.
2. При остром многоводии и ухудшении состояния беременной показаны госпитализация и постельный режим. Ограничение потребления поваренной соли и диуретики неэффективны.
3. При выраженной одышке и боли в животе показан абдоминальный амниоцентез. Жидкость выпускают медленно, со скоростью 500 мл/ч. Быстрое выведение даже незначительного количества околоплодных вод может осложниться преждевременной отслойкой плаценты и преждевременными родами. Преждевременные роды могут развиться даже при медленном выведении околоплодных вод. Амниоцентез повышает риск внутриутробной инфекции.
4. Объем околоплодных вод быстро нарастает вновь, поэтому амниоцентез обычно приходится выполнять повторно. При многоводии, особенно остром, высок риск преждевременных родов.
Г. Осложнения в родах
1. Нарушения положения и предлежания плода (особенно часто — тазовое предлежание).
3. Кровотечение в родах и послеродовом периоде.
Д. Осложнения у плода
1. Прогноз для плода неблагоприятный. Перинатальная смертность достигает 50%. Основные причины смерти — пороки развития и недоношенность.
2. Грубые пороки развития наблюдаются в 20—30% случаев многоводия.
3. Новорожденного тщательно обследуют. В первую очередь исключают атрезию пищевода или двенадцатиперстной кишки.
4. В 60% случаев многоводие не связано с заболеваниями матери или плода.
Е. Осложнения у матери. В связи с перерастяжением матки возможны дискоординация и слабость родовой деятельности. Для профилактики послеродового кровотечения после рождения ребенка вводят окситоцин, 10—20 ед в/в капельно в 1000 мл 5% глюкозы.
А. Определение. О маловодии говорят, если объем околоплодных вод не превышает 60 мл, индекс объема околоплодных вод в этом случае ниже 5 см. При выраженном маловодии беременность обычно прерывается на ранних сроках. Маловодие может развиваться на разных сроках беременности и нередко остается нераспознанным. При доношенной беременности, осложненной маловодием, часто наблюдаются пороки развития плода и внутриутробная задержка развития.
Б. Состояние плода. Маловодие чаще всего вызвано заболеваниями, сопровождающимися ограничением или полным прекращением поступления мочи плода в амниотическую полость. К ним относятся пороки развития почек и мочевых путей плода: двусторонняя агенезия почек, поликистоз почек, стеноз мочеиспускательного канала. При обнаружении после родов узловатого амниона, одного из признаков маловодия, показано тщательное обследование мочевых путей новорожденного (см. гл. 29, п. IV.Г.2). Маловодие в большинстве случаев сопровождается внутриутробной гипоксией. Оно часто встречается при переношенной беременности и внутриутробной задержке развития.
В. Лечение в первую очередь направлено на профилактику и устранение патологии плода.
1. Benirschke K., Kaufman P. Pathology of the Human Placenta (2nd ed.). New York: Springer-Verlag, 1990.
2. Fox H. Pathology of the Placenta. Philadelphia: Saunders, 1978.
3. Kaplan C. G. Color Atlas of Gross Placental Pathology. New York: Igaku-Shoin, 1994.
4. Hammond C. B. et al. Treatment of metastatic trophoblastic disease: Good and poor prognosis. Am. J. Obstet. Gynecol. 115:451, 1973.
5. Miller D. S., Lurain J. R. Classification and staging of gestational trophoblastic tumors. Obstet. Gynecol. Clin. North Am. 15:477, 1988.
6. Schlaerth J. B. et al. Prognostic characteristics of serum human chorionic gonadotropin titer regression following molar pregnancy. Obstet. Gynecol. 587:478, 1981.
7. Young R. H., Scully R. E. Placental site trophoblastic tumor. Current status. Clin. Obstet. Gynecol. 27:248, 1984.
8. Phelan J. P. et al. Amniotic fluid volume assessment with the four-quadrant technique at 36—42 weeks’ gestation. J. Reprod. Med. 32:540, 1987.
9. Queenan J. T. Polyhydramnios and oligohydramnios. Contemp. Obstet. Gynecol. 36:60, 1991.
10. Shenker L. et al. Significance of oligohydramnios complicating pregnancy. Am. J. Obstet. Gynecol. 164:1597, 1991.