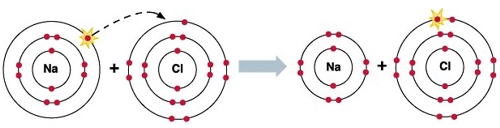
Плюсы и минусы в химии что означают
Валентность и степень окисления
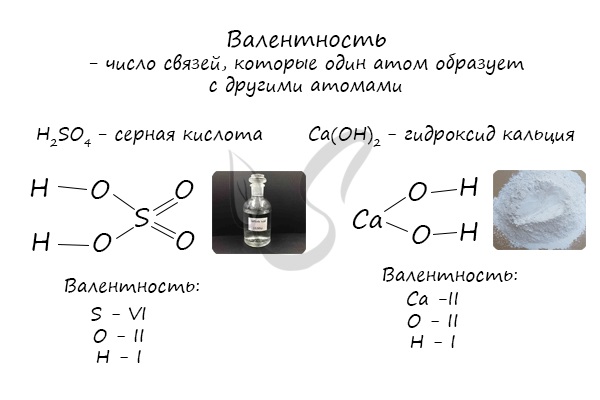
Валентность
Определяют валентность по числу связей, которые один атом образует с другими. Для примера рассмотрим две молекулы
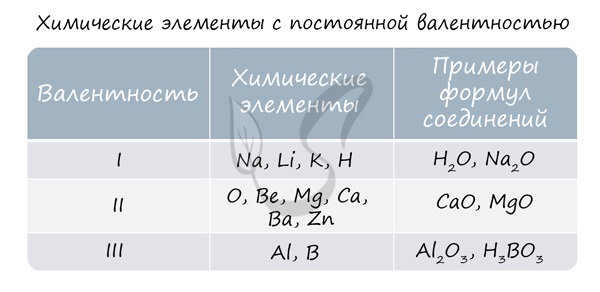
Для определения валентности нужно хорошо представлять графические формулы веществ. В этой статье вы увидите множество формул. Сообщаю вам также о химических элементах с постоянной валентностью, знать которые весьма полезно.
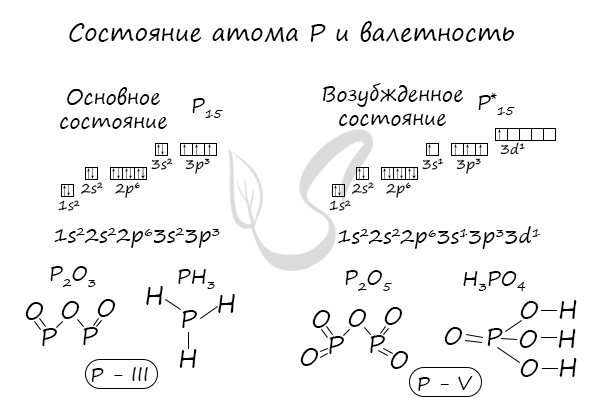
В электронной теории считается, что валентность связи определяется числом неспаренных (валентных) электронов в основном или возбужденном состоянии. Мы касались с вами темы валентных электронов и возбужденного состояния атома. На примере фосфора объединим эти две темы для полного понимания.
Подавляющее большинство химических элементов обладает непостоянным значением валентности. Переменная валентность характерна для меди, железа, фосфора, хрома, серы.
Степень окисления
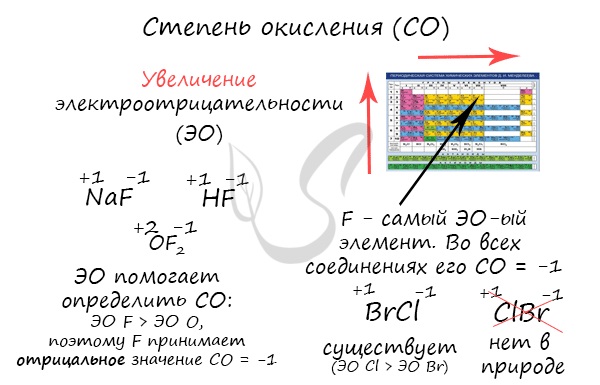
Численно степень окисления равна условному заряду, который можно приписать атому, руководствуясь предположением, что все электроны, образующие связи, перешли к более электроотрицательному элементу.
Зная изменения электроотрицательности в периодах и группах периодической таблицы Д.И. Менделеева, можно сделать вывод о том какой элемент принимает «+», а какой минус. Помогают в этом вопросе и элементы с постоянной степенью окисления.
Самостоятельно определите степени окисления атомов в следующих веществах: RbOH, NaCl, BaO, NaClO3, SO2Cl2, KMnO4, Li2SO3, O2, NaH2PO4. Ниже вы найдете решение этой задачи.
Сравнивайте значение электроотрицательности по таблице Менделеева, и, конечно, пользуйтесь интуицией 🙂 Однако по мере изучения химии, точное знание степеней окисления должно заменить даже самую развитую интуицию 😉
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Валентность и степень окисления
Плюсы и минусы в химии что означают
Когда химические вещества вступают во взаимодействие, химические связи между их атомами разрушаются и образуются новые, уже в других сочетаниях. В результате одни вещества превращаются в другие.
Рассмотрим реакцию горения метана, происходящую в конфорке газовой плиты:
Молекула метана (CH₄) и две молекулы кислорода (2O₂) вступают в реакцию, образуя молекулу углекислого газа (CO₂) и две молекулы воды (2H₂O). Связи между атомами углерода (С) и водорода (H) в метане, а также между атомами кислорода (O) разрываются, и образуются новые связи между атомами углерода и кислорода в молекуле углекислого газа (CO₂) и между атомами водорода и кислорода в молекуле воды (H₂O).
Картинка даёт наглядное представление о том, что произошло в ходе реакции. Но зарисовывать сложные химические процессы такими схемами неудобно. Вместо этого учёные используют уравнения химических реакций.
Химическое уравнение — это условная запись химической реакции с помощью формул и символов.
Их записывают в виде схемы, в которой отражён процесс превращения. В левой части располагаются формулы реагентов — веществ, вступающих в реакцию. Завершается уравнение продуктами реакции — веществом или веществами, которые получились в результате.
Новые вещества образуются потому, что изменяются связи между атомами, но сами атомы не возникают из ниоткуда и не исчезают в никуда. На рисунке видно, что атом углерода из состава метана перешёл в состав углекислого газа, атом водорода — в состав воды, а атомы кислорода распределились между молекулами углекислого газа и воды. Число атомов не изменилось.
Согласно закону сохранения массы, общая масса реагентов всегда равна общей массе продуктов реакции. Именно поэтому запись химической реакции называют уравнением.
Виды химических реакций
Вещества вступают в реакции по-разному, можно выделить четыре наиболее частых варианта:
Сложное вещество негашёная известь соединяется с водой, и образуется новое сложное вещество — гашёная известь:
Стрелка вверх означает, что образовался газ. Он улетучивается и больше не участвует в реакции.
В примере атомы цинка замещают атомы водорода в составе хлороводорода, и образуется хлорид цинка:
Стрелка вниз означает, что вещество выпало в осадок, поскольку оно нерастворимо.
Коэффициенты в уравнениях химических реакций
Чтобы составить уравнение химической реакции, важно правильно подобрать коэффициенты перед формулами веществ.
Коэффициент в химических уравнениях означает число молекул (формульных единиц) вещества, необходимое для реакции. Он обозначается числом перед формулой (например, 2NaCl в последнем примере).
Коэффициент не следует путать с индексом (числом под символом химического элемента, например, О₂). Индекс обозначает количество атомов этого элемента в молекуле (формульной единице).
Чтобы узнать общее число атомов элемента в формуле, нужно умножить его индекс на коэффициент вещества. В примере на картинке (2H₂O) — четыре атома водорода и два кислорода.
Подобрать коэффициент — значит определить, сколько молекул данного вещества должно участвовать в реакции, чтобы она произошла. Далее мы расскажем, как это сделать.
Алгоритм составления уравнений химических реакций
Для начала составим схему химической реакции. Например, образование оксида магния (MgO) в процессе горения магния (Mg) в кислороде (O₂). Обозначим реагенты и продукт реакции:
Чтобы схема стала уравнением, нужно расставить коэффициенты. В левой части схемы два атома кислорода, а в правой — один. Уравняем их, увеличив число молекул продукта:
Теперь число атомов кислорода до и после реакции одинаковое, а число атомов магния — нет. Чтобы уравнять их, добавим ещё одну молекулу магния. Когда количество атомов каждого из химических элементов в составе веществ уравнено, вместо стрелки можно ставить равно:
Уравнение химической реакции составлено.
Рассмотрим реакцию разложения. Нитрат калия (KNO₃) разлагается на нитрит калия (KNO₂) и кислород (О₂):
В обеих частях схемы по одному атому калия и азота, а атомов кислорода до реакции 3, а после — 4. Необходимо их уравнять.
Для начала удвоим коэффициент перед реагентом:
Теперь в левой части схемы шесть атомов кислорода, два атома калия и два атома азота. В левой по-прежнему по одному атому калия и азота и четыре атома кислорода. Чтобы уравнять их, в правой части схемы нужно удвоить коэффициент перед нитритом калия.
Снова посчитаем число атомов каждого химического элемента в составе веществ до и после реакции: два атома калия, два атома азота и шесть атомов кислорода. Равенство достигнуто.
Химические уравнения не только позволяют предсказать, что произойдёт при взаимодействии тех или иных веществ, но и помогают рассчитать их количественное соотношение, необходимое для реакции.
Учите химию вместе с домашней онлайн-школой «Фоксфорда»! По промокоду CHEMISTRY892021 вы получите бесплатный недельный доступ к курсам химии за 8 класс и 9 класс.
У нас вы сможете учиться в удобном темпе, делать упор на любимые предметы и общаться со сверстниками по всему миру.

Интересное по рубрике
Найдите необходимую статью по тегам
Подпишитесь на нашу рассылку
Мы в инстаграм
Домашняя онлайн-школа
Помогаем ученикам 5–11 классов получать качественные знания в любой точке мира, совмещать учёбу со спортом и творчеством

Рекомендуем прочитать
Реальный опыт семейного обучения
Звонок по России бесплатный
Посмотреть на карте
Если вы не нашли ответ на свой вопрос на нашем сайте, включая раздел «Вопросы и ответы», закажите обратный звонок. Мы скоро свяжемся с вами.
Степень окисления для «чайников»
Степень окисления или окислительное число дает количественную характеристику состояния атома в соединении.
| Степень окисления — условный заряд атома в соединении, если предположить, что соединение состоит только из ионов |
Исходя из вышесказанного, в окислительно-восстановительных реакциях вычисляют неизвестную степень окисления элементов, исходя из двух моментов:
Составляем и решаем уравнение:
| Высшая степень окисления — наибольшее положительное ее значение |
Высшая степень окисления является очень важной количественной характеристикой элемента, чаще всего, она равна номеру группы элемента в Периодической таблице:
| Низшая степень окисления — наименьшее возможное ее значение для данного элемента |
Если элемент имеет три и более возможных степеней окисления, то все остальные степени окисления, лежащие между высшей и низшей, называются промежуточными или средними.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Плюсы и минусы химической промышленности
Реакции проходят не только в лабораторных условиях. В промышленных масштабах производится химическая продукция, важнейшая для повседневной жизни людей. В «десятку» лидеров по объему входят следующие вещества: серная кислота, азот, аммиак, этилен и другие. Компоненты пищи также получают при помощи химической промышленности. Фраза «100%-ый натуральный продукт» означает, что в нем отсутствуют синтетические добавки. Но при его производстве могут быть использованы технологии.
Отрасль народного хозяйства
Получение химической продукции основано на переработке природного сырья, материалов. В основе лежат различные технологии, экономичные методы. Химпроизводство является многоотраслевым. В его организацию заложены научные принципы:
Помимо природных ресурсов, которые используют для химической продукции, задействуется вторичное сырье (отходы, отработанные изделия).
К вспомогательным материалам относят топливо, растворители, воду, катализаторы. К минеральному сырью – руды и другие ископаемые (поваренная соль, глины, песок). К органическому – нефть, уголь, торф, природный газ.
Химические предприятия необходимо располагать в непосредственной близи с источником воды. Параллельно решаются задачи:
Горячей водой или паром подогревают реагирующие вещества. При этом расход вспомогательного материала огромен. Так, требуется 1,5 тыс. кубических метров воды для получения 1 тонны аммиака, 250 м3 – такого же количества бумаги.
Положительные стороны работы химпрома
Отрицательные моменты
Вывод
Классические слова о «глубоко простирающих руках химии в дела человеческие», сейчас стоит воспринимать с особой осторожностью. Потребители товаров, созданных при помощи современных технологий, должны внимательно изучать инструкции о составе, применении веществ. Надзорные органы – следить за расходом, утилизацией в промышленном масштабе.
Абсолютно исключать химикаты из бытовой сферы неразумно и нереально. Огонь, к примеру, тоже может уничтожить все вокруг. Но при умелом обращении люди согреваются, готовят пищу и осуществляют процессы жизнедеятельности с его помощью.
Плюсы и минусы химии в жизни человека
Какова роль химии в жизни современного человека, какие плюсы и минусы химии, Вы узнаете из этой статьи.
Сложно представить какой бы была наша жизнь без химии и продукции, которую она производит. Сегодня мы поговорим о том, какая отрицательная и положительная роль химии в жизни человека.
Плюсы и минусы химии в жизни человека
Вред химии в жизни человека
Химия в роли негативного фактора в человеческой жизни появляется постоянно. Чаще всего это проявляется в здоровье населения и в экологической сфере. Изобилие чужеродных материалов на нашей планете приводит к засорению воды и почвы. К тому же они не подвергаются естественным процессам гниения. Но когда они все же разлагаются или сгорают, то выделяют огромное количество токсичных веществ, которые дополнительно отравляют окружающую среду. То же самое касается отходов с промышленных предприятий, которые практически не перерабатываются, отравляя человека и окружающую среду.
Еще одна отрицательная роль химии в жизни человека, это производство искусственной пищи. С одной стороны это как бы решает продовольственную проблему, но генетическое изменение продуктов питания приводит к накоплению в них негативных веществ, которые пагубно влияют на здоровье человека. Большое количество консервантов в пище в некоторых странах стало настоящей проблемой. Тело людей, питающихся подобными веществами, после смерти не сгнивает, а годами лежит под землей, так как естественные процессы гниения в них сильно затормаживаются.
Окружающая нас в быту химия часто вызывает аллергические реакции и отравления в организме. Также средства от вредителей для обработки растений и минеральные удобрения опасны для человека и природы. Они постепенно приводят к разрушению.
Плюсы химии в жизни человека
Задумываясь о том, какие плюсы химии в жизни человека, вспомните о тех ее достижениях, которые сделали мир вокруг нас более комфортным. Из продукции химической промышленности изготавливают и производят медицинские препараты, удобрения, материалы с уникальными свойствами, источники пищи и энергии, косметические средства.
Надеемся, что из этой статьи Вы узнали о том, какие плюсы и минусы химии в жизни человека.





.jpg)
.jpg)
.jpg)
.jpg)


.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)