Повышен хромогранин а и гастрин что это значит
Биохимическое тестирование нейроэндокринных опухолей
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
На уровень этих веществ влияет как наличие опухоли, так и другие факторы, например, некоторые лекарственные препараты, продукты питания и напитки. Биомаркеры используют для диагностики, но одних их недостаточно для точной постановки диагноза, обнаружения первичной опухоли и определения ее типа. Несмотря на это, определение нескольких биомаркеров обязательно для диагностики и последующего наблюдения пациентов с нейроэндокринными опухолями.
Хромогранин А (CgA)
Это белок, содержащийся в секреторных гранулах нормальных и опухолевых нейроэндокринных клеток. Он высвобождается вместе с пептидными гормонами и биогенными аминами, а также сам по себе является предшественником функциональных нейроэндокринных пептидов.
В современных рекомендациях измерение хромогранина А является обязательным у пациентов с нейроэндокринными опухолями желудочно-кишечного тракта. Исходный и последующие уровни хромогранина А отражают ответ на противоопухолевое лечение и прогноз по заболеванию. Кроме того, рост уровня хромогранина А часто отражает местное прогрессирование у пациентов с поражением печени.
Однако, высокий уровень хромогранина А наблюдается только у 60–80% пациентов с НЭО и имеет ограниченную чувствительность (60–83%) и относительно низкую специфичность (72–85%). Доказано, что прием ингибиторов протонной помпы (Омез, Нексиум и т.п.), атрофический гастрит и нарушение функции почек вызывают повышение уровня CgA у людей без нейроэндокринных опухолей. Поэтому важно сочетать определение уровня хромогранина А с другими методами диагностики. Так, комбинация со сцинтиграфией соматостатиновых рецепторов повышает чувствительность (93%) и специфичность (81%). Чувствительность теста на хромогранин А зависит также от локализации первичной опухоли, наличия эндокринологических синдромов, стадии заболевания и наличия метастатического поражения печени.
Важно отметить, что в зависимости от лаборатории, показатели нормального уровня хромогранина А могут сильно варьировать, поэтому рекомендуется выполнять повторные тесты в той же лаборатории, где выполнялся первый тест (до начала лечения).
Нейронспецифическая энолаза (NSE)
Особый фермент, в норме встречающийся в клетках центральной нервной системы. Считается, что повышение уровня NSE отражает процесс гибели клеток с нейроэндокринной дифференцировкой. В основном NSE является опухолевым маркером в диагностике, в прогнозировании и наблюдении мелкоклеточного рака легкого. Однако, NSE повышается у 38–40% пациентов с нейроэндокринными опухолями желудочно-кишечного тракта. NSE имеет сходную с хромогранином А специфичность, но ее чувствительность ниже. Уровни NSE напрямую связаны с дифференцировкой, агрессивностью и размером опухоли. Несмотря на свою ограниченную чувствительность, NSE обратно коррелирует с общей выживаемостью при нейроэндокринных опухолях IV стадии.
«Серотониновая группа»
Рис. Схема метаболизма серотонина в организме человека
Повышенный уровень серотонина, вырабатываемого многими нейроэндокринными опухолями желудочно-кишечного тракта, напрямую связан с диареей и приливами при карциноидном синдроме. В процессе метаболизма серотонина в организме образуется 5-гидроксииндолуксусная кислота (5-HIAA), которая выводится с мочой. Традиционно в комплексе диагностики определяются уровни всех метаболитов «серотониновой группы» (см. схему). Суточный уровень 5-HIAA в моче используется в качестве маркера при диагностике и наблюдении НЭО. Специфичность 5-HIAA у пациентов с НЭО близка к 90%, но чувствительность составляет 35–68%. Когда все эти метаболиты измеряются вместе, чувствительность увеличивается до 84%.
Перечисленные маркеры являются основными практически для всех НЭО, вне зависимости от локализации. В каждом конкретном случае перечень необходимых маркеров может расширяться, что диктуется локализацией опухоли.
Среди дополнительных маркеров встречаются:
Хромогранин А
Описание
Хромогранин А является важнейшим универсальным маркёром нейроэндокринной ткани и различных нейроэндокринных опухолей.
Хромогранин А — гликопротеин, который относится к семейству хромогранинов, являющихся основным компонентом содержимого крупных оптически плотных гранул большинства нейроэндокринных клеток. При специфической стимуляции таких клеток, хромогранины секретируются вместе с пептидными гормонами и нейропептидами.
Хромогранины (из которых хромогранин А является наиболее изученным) играют важную роль в процессах образования, созревания, внутриклеточной транспортировки и экзоцитоза секреторных гранул в нейроэндокринных клетках и нейронах. Кроме того, в результате ферментативного расщепления хромогранинов образуется ряд более мелких пептидов, обладающих различной биологической активностью.
В качестве специфичных маркёров нейроэндокринных опухолей разного происхождения, в рамках комплексной диагностики, обычно используют их специфические продукты (катехоламины и их метаболиты — при подозрении на феохромоцитому, серотонин и его метаболит 5-ОИУК — при подозрении на карциноид, гипофизарные гормоны — при подозрении на опухоли гипофиза и т. п.).
Чувствительность хромогранина в качестве опухолевого маркёра нейроэндокринных опухолей варьирует от 10 до 100% в зависимости от типа опухоли и стадии заболевания. Исследование хромогранина А в сыворотке крови находит клиническое применение, прежде всего, в комплексной диагностике карциноидных опухолей (несекретирующие серотонин опухоли могут сохранять способность продуцировать хромогранин А). Определение уровня хромогранина А может быть полезно в комплексной диагностике феохромоцитомы, нейробластомы, медуллярного рака щитовидной железы, опухолей, происходящих из островкового аппарата поджелудочной железы, и др.
Повышение уровня хромогранина А в сыворотке коррелирует с размером, распространённостью, гистопатологическими характеристиками нейроэндокринных опухолей. Оно ярче выражено при больших, хорошо дифференцированных и метастатических опухолях.
Повышенный уровень хромогранина
Причиной повышения уровня хромогранина А, помимо нейроэндокринных опухолей, могут быть атрофический гастрит, гастриты, связанные с инфекцией Helicobacter pylori (параллельно с повышением секреции гастрина), почечная недостаточность, патология печени (цирроз, хронические гепатиты), доброкачественная гиперплазия и карцинома простаты.
Небольшое повышение хромогранина А отмечали при язвенных колитах и болезни Крона, болезни Паркинсона, ревматоидном артрите, гиперпаратиреоидизме, гипертиреоидизме, сердечной недостаточности, у части пациентов с опухолями, не относящимися к нейроэндокринным (груди, лёгких, желудочно-кишечного тракта и пр.). Следует учитывать, что две группы лекарственных препаратов оказывают значительное влияние на концентрацию хромогранина: ингибиторы протонной помпы и блокаторы H2-рецепторов гистамина.
Показания
В комплексной диагностике и обследованиях пациентов с характерными признаками и симптомами нейроэндокринных опухолей.
Подготовка
Кровь рекомендуется сдавать утром, в период с 8 до 12 часов. Взятие крови производится натощак или спустя 8–14 часов голодания, допустимо днём через 4 часа после лёгкого приёма пищи. Допускается употребление воды без газа и сахара. Накануне сдачи исследования следует избегать пищевых перегрузок.
В случае приёма лекарственных препаратов (наиболее значимы препараты из групп ингибиторов протонной помпы и блокаторов Н2-рецепторов гистамина), следует обсудить с врачом возможность их временной отмены (не менее 3-х периодов полувыведения для ингибиторов протонной помпы). Возможно влияние глюкокортикоидов на результат исследования.
Повышен хромогранин а и гастрин что это значит
Хромогранин А – лабораторный тест, направленный на определение концентрации в сыворотке крови белка, являющегося специфичным маркером нейроэндокринных опухолей.
Chromogranin A, CgA, Serum Chromogranin A.
Иммуноферментный анализ (ИФА).
Мкг/л (микрограмм на литр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Нейроэндокринные опухоли – это разнородная группа новообразований, происходящих из клеток так называемой APUD-системы. Эта система представлена рассеянными в различных частях организма человека эндокринными клетками, которые способны вырабатывать биологически активные вещества (например, гормоны и гормоноподобные молекулы). Нейроэндокринные опухоли могут возникать в любых органах, где в норме присутствуют нейроэндокринные клетки: желудочно-кишечный тракт, легкие, вилочковая железа, почки, яичники, простата, щитовидная и молочные железы. Клиническая картина нейроэндокринных опухолей во многом определяется вырабатываемыми ими биологически активными веществами, определение концентрации которых в крови широко используется в диагностике таких новообразований.
Хромогранин А – это белок, вырабатываемый нейроэндокринными клетками и принимающий участие в продукции этими клетками биологически активных соединений. Важно отметить, что не все опухолевые клетки активно вырабатывают гормоны и подобные им вещества, однако сывороточный уровень хромогранина А повышается независимо от этого.
Концентрация хромогранина А в крови человека определяется методом иммуноферментного анализа (ИФА). Принцип ИФА основан на взаимодействии специфичного антитела к хромогранину А, фиксированного на поверхности планшета с хромогранином А, содержащимся в исследуемой сыворотке пациента. При формировании комплекса хромогранин-антитело специальный фермент, добавленный в реакционную смесь, изменяет её окраску. При этом интенсивность цвета пропорциональна концентрации хромогранина А в исследуемой сыворотке. Интенсивность окраски измеряется специальным прибором, который переводит параметры световой волны в цифры, соответствующие концентрации хромогранина А.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
По разным данным, чувствительность и специфичность хромогранина А как маркера нейроэндокринных опухолей составляет от 45 до 95 %. Человек с нормальным уровнем хромогранина А, наиболее вероятно, не будет иметь нейроэндокринную опухоль. Тем не менее на основании нормального результата только этого теста абсолютно исключить заболевание нельзя. Результат определения концентрации хромогранина А должен оцениваться в комплексе с исследованием уровня других опухолевых маркеров, клинической картиной, а также данными визуальных методов обследования.
Повышенный уровень хромогранина А у человека с клиническими проявлениями может указывать на наличие опухоли, но он не специфичен для локализации и морфологического типа опухоли – в группу нейроэндокринных опухолей входят различные по клеточному субстрату и локализации опухоли, хромогранин является общим маркером для них всех. Кроме того, не все нейроэндокринные опухоли вырабатывают биологически активные вещества, соответственно, не всегда повышение хромогранина А будет сопровождаться симптомами карциноидного синдрома. Это ещё раз доказывает, что при выявлении повышенного уровня хромогранина А диагностический поиск должен быть продолжен в целях обнаружения опухоли (определение её локализации при помощи визуализирующих методов диагностики) и проведения биопсии с последующим иммуногистохимическим анализом для установления морфологического типа.
Ниже приведены некоторые опухоли, при которых выявляется повышение сывороточного уровня хромогранина А:
гастроинтестинальные опухоли – гастринома, инсулинома, глюкагонома, ВИПома, соматостатинома и др.;
опухоли щитовидной (медуллярный рак) и паращитовидных желез;
опухоли нервной системы – параганглиома, нейробластома, опухоли гипофиза;
опухоли надпочечников – феохромоцитома;
опухоли легких – мелкоклеточный рак легких.
Кроме того, повышение хромогранина А может наблюдаться и при других опухолях, которые не входят в группу нейроэндокринных: рак молочной, поджелудочной и предстательной желез, рак яичников.
При интерпретации результатов теста необходимо помнить, что повышение концентрации сывороточного хромогранина А может быть и при других состояниях, не связанных с опухолями (смотрите раздел «Что может влиять на результат?»).
Ряд научных исследований выявил корреляцию уровня хромогранина А с размером и гистологическим типом нейроэндокринных опухолей. Наиболее высокие уровни отмечались при больших и хорошо дифференцированных опухолях (например, феохромоцитома, медуллярный рак щитовидной железы), также значительно повышенный хромогранин А всегда обнаруживается при гастриноме (хроническое повышение уровня гастрина вызывает гиперплазию нейроэндокринных клеток желудка, которые способны секретировать хромогранин A).
В процессе мониторинга концентрации хромогранина А его снижение на фоне лечения говорит, вероятнее всего, об эффективности терапии. Если же сниженный в процессе лечения уровень хромогранина А начинает расти, скорее всего, имеет место рецидив опухоли.
Что может влиять на результат?
Важно помнить, что уровень хромогранина А в сыворотке крови может изменяться под воздействием различных факторов или патологических состояний, не связанных с нейроэндокринными опухолями. Среди факторов, вызывающих увеличение концентрации хромогранина А в крови, можно выделить:
Стоит заметить, что хотя при этих состояниях уровень хромогранина А и повышен, все же он значительно меньше того, который наблюдается при нейроэндокринных новообразованиях.
В настоящее время не существует стандартизированных тестовых систем для определения концентрации хромогранина А. Это значит, что сопоставлять результаты тестов, выполненных диагностическими системами разных производителей, нельзя. При мониторинге пациента с течением времени тесты на хромогранин А желательно выполнять с использованием тестовой системы одного производителя, чтобы можно было сравнивать значения. При переходе на другую тест-систему пациентам должны устанавливаться новые базальные уровни.
Кто назначает исследование?
Онколог, нейрохирург, эндокринолог, андролог, терапевт, врач общей практики.
Согласование результатов определения уровня хромогранина А различными тест-системами
Журнал «Экспериментальная и клиническая урология» Выпуск №1 за 2015 год
Сивков А.В., Кешишев Н.Г., Кривенко М.П., Ковченко Г.А., Рабинович Э.З., Никонова Л.М., Ромих Ф.Д.
Хромогранин (Хг) представляет собой кислый гликопротеин, состоящий из 439 аминокислот. Данный гликопротеин присутствует в ядрах большинства нейроэндокринных клеток [1]. Семейство хромогранинов состоит из трех различных водорастворимых кислых гликопротеинов – хромогранин А (ХгА), хромогранин B (ХгB), секретогранин II или хромогранин C (ХгС). По всей длине молекулы Хг распределены основные аминокислотные остатки, особенно ими богат С-конец молекулы. По этим аминокислотным остаткам происходит расщепление молекулы, в результате чего образуются вазостатин и хромостатин. ХгВ сходен по химической структуре с ХгА, но распространен менее широко [2, 3].
ХгА широко используется в качестве иммуногистохимического маркера нейроэндокринной дифференцировки (НЭД). При наличии стимулирующих факторов происходит высвобождение ХгА, других пептидных гормонов и нейропептидов. В панели маркеров НЭД ХгА обладает наибольшей диагностической ценностью.
ХгА экспрессируется опухолями, имеющими нейроэндокринное происхождение, из различных эмбриональных отделов первичной кишки – верхнего (foregut), из которого дифференцируются бронхи, легкие, желудок, проксимальный отдел двенадцатиперстной кишки, поджелудочная железа; среднего (midgut), предшественника дистального отдела двенадцатиперстной кишки, тощей, подвздошной, слепой и восходящей ободочной кишки, а также аппендикса; нижнего (hindgut), из которого развиваются дистальные отделы толстой кишки и прямая кишка [4, 5].
ХгА может повышаться при гастро-энтеро-панкреатических опухолях, нейроэндокринных опухолях (НЭО) поджелудочной железы, синдроме множественной эндокринной неоплазии 1 типа, опухолях мозгового слоя надпочечников, опухоли паращитовидных желез, феохромоцитомах, нейробластомах, некоторых гипофизарных опухолях и др. [6].
Специфичность ХгА в диагностике НЭО зависит от природы и локализации образования, в некоторых случаях она достигает 100%, например, при метастатическом раке истинно нейроэндокринных опухолей [7, 8, 9, 10].
В соответствии с рекомендациями Европейского общества по нейроэндокринным опухолям ХгА является обязательным маркером биохимического обследования для диагностики, мониторинга и прогноза НЭО [11]. ХгА характеризуется высокой диагностической чувствительностью при НЭО желудка (95%), подвздошной кишки (80%), бронхолегочной системы (70%), синдроме множественных эндокринных неоплазий (78%). При этом, в различных исследованиях была выявлена зависимость ХгА от распространенности процесса [4].
Среди факторов, вызывающих ложноположительное повышение ХгА крови, можно выделить:
Чувствительность и специфичность определения плазматических уровней ХгА при различных нейроэндокринных заболеваниях варьирует от 70% до 95%. Наиболее высокие показатели ХгА наблюдают в случае опухолей с выраженной секреторной активностью [18].
Не существует единого международного стандартизированного подхода к определению ХгА. Коммерческие наборы для определения ХгА отличаются типом используемых антител (моноклональное и поликлональные), а также методом анализа (иммуноферментный и радиоиммунный). Подобные различия в методах неизбежно приводят к неоднородности результатов [19, 20].
В России официально зарегистрированы две тест-системы определения ХгА: тест-система компании DAKO (Дания) и компании Euro-Diagnostica (ED Швеция).
Оба метода проводятся путем иммуноферментного анализа, представляют собой количественное определение ХгА крови. В наборах DAKO и ED используются плазма крови (сыворотка крови), этилендиаминтетрауксусная кислота (ЭДТА) или гепариновая плазма. Для определения ХгА в наборах ED и DAKO применяются разные единицы измерения: нмоль/л и Ед/л соответственно. Согласно данным компаний производителей референсные значения для ED и DAKO составляют 0-3 нмоль/л и 2-18 Ед/л соответственно [21, 22].
Референсные значения для ED рассчитывались на основе 97,5 процентиля для образцов, собранных у 120 доноров крови (60 мужчин и 60 женщин в возрасте 20-65 лет). Ожидаемый диапазон референсных значений ХгА составил 0-3 нмоль/л. Расчеты были выполнены в соответствии с правилами Consensus Standards for Medical Testing: NCCLS EP17 – A [23]. К сожалению, мы не смогли получить данные о методиках расчета референсных диапазонов для ХгА компании DAKO.
В урологии ХгА применяется для определения НЭД, главным образом, при раке предстательной железы (РПЖ). Повышенные значения данного маркера могут свидетельствовать о присутствии нейроэндокринных клеток в ткани ПЖ [24, 25]. Обнаружение НЭД диктует необходимость назначения патогенетической терапии, включая аналоги соматостатина [26]. В ходе наших предыдущих исследований возникла проблема интерпретации (согласования) значений ХгА, определенных разными тест-системами, что вело к диагностическим ошибкам. [27]. Поэтому, целью нашей работы стало сравнение показателей ХгА, определенных тест-системами DAKO и ED при различных заболеваниях предстательной железы.
МАТЕРИАЛЫ И МЕТОДЫ
Всего в исследование было включено 304 мужчин с доброкачественной гиперплазией предстательной железы (ДГПЖ), хроническим простатитом, простатической интраэпителиальной неоплазией (ПИН) низкой степени, ПИН высокой степени, локализованным РПЖ (ЛРПЖ), местнорапрострененным РПЖ (МРРПЖ), кастрационно-резистентным РПЖ (КРРПЖ). Также была набрана контрольная группа здоровых мужчин. У 113 пациентов мы смогли определить ХгА двумя тест-системами. Кроме того, всем пациентам были выполнены клинический и биохимический анализы крови для выявления сопутствующих патологических процессов, а также определен уровень простатспецифического антигена (ПСА) сыворотки крови. С учетом анамнеза у пациентов исключали заболевания желудочно-кишечного тракта, эндокринной системы, онкологические процессы, неконтролируемую артериальную гипертензию, предшествующие хирургические манипуляции на органах мочевой системы. При обнаружении указанных заболеваний пациенты в исследование не включались.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
По результатам исследования мы получили явно завышенные показатели при различных заболеваниях ПЖ при использовании тестсистемы DAKO по сравнению с ED (табл. 1).
В группе больных, где уровень ХгА определялся с помощью ED, повышенный ХгА (ХгА≥ 3 нмоль/л) был выявлен у 5 пациентов КРРПЖ и у 1 – с ЛРПЖ, тогда как в группе, где использовалась тест-система DAKO превышение верхней границы нормы (18 Ед/л) было определено 34 пациента, в том числе у 6 мужчин контрольной группы.
С чем связанно такое несоответствие? Первый возможный ответ – это погрешности технологий определения ХгА. Второй причиной может быть несоответствие референсных значений той или иной тест-системы. Таким образом, мы столкнулись со сложностями интерпретации значений сывороточного ХгА, определенного тест-системами DAKO и Euro-Diagnostica.
Таблица 1. Число больных с повышенным уровнем ХгА, определенного тест-системами DAKO и Euro-Diagnostica при заболеваниях предстательной железы
| Заболевание | n | Превышение референсных значений | |
|---|---|---|---|
| ED: >3 нмоль/л | DAKO: >18 Ед/л | ||
| Контрольная группа | 29 | 0 | 6 |
| ДГПЖ | 3 | 0 | 0 |
| Хронический простатит | 8 | 0 | 1 |
| ПИН низкой степени | 9 | 0 | 1 |
| ПИН высокой степени | 5 | 0 | 1 |
| ЛРПЖ | 24 | 1 | 9 |
| МРРПЖ | 7 | 0 | 3 |
| КРРПЖ | 28 | 5 | 13 |
| ВСЕГО пациентов | 113 | ||
Для определения диагностической ценности двух тест-систем нами был проведен сравнительный многофакторный математический анализ показателей ХгА при различных заболеваниях ПЖ. Были приняты следующие обозначения: ХгА D – для измерений в тест-системе компании DAKO, ХгА E – для EuroDiagnostica. Все пациенты были разделены на следующие группы: контрольную, в которую вошли здоровые мужчины и еще 7 групп с различными заболеваниями ПЖ. Всего были проанализированы данные 113 мужчин, из которых 29 – составили контрольную группу.
С целью формирования статистических моделей для имеющихся данных был проведен их предварительный анализ. В первую очередь это касалось контрольной группы, которую можно рассматривать как однородную совокупность наблюдений. В таблице 2 представлены оценки первых моментов (среднего μ и стандарта σ) и коэффициента вариации σ/μ, а также результаты проверки гипотезы о том, что для имеющихся данных применимо нормальное распределение. В последнем случае использовались критерий асимметрии (равенство нулю нормированного 3-го центрального момента) и критерий эксцесса (равенство определенному значению нормированного 4-го центрального момента) и 1% значение уровня значимости.
Из этого можно сделать вывод о том, что:
1. Измерения маркеров XгA E и XгA D осуществляются в пропорциональных единицах (похожие значения коэффициента вариации σ/μ), т.е. ни одно из этих измерений не имеет явных преимуществ с точки зрения точности.
2. Для измерений XгA E и XгA D нет предпосылок принять гипотезу о нормальном распределении, поэтому требуется осторожность при использовании методов, ориентированных на эту модель данных.
Несмотря на то, что в обеих тест-системах анализируется одна и та же характеристика, сомнения относительно согласованности формируемых измерений привели к желанию исследовать статистическую зависимость значений ХгА. В соответствии со сделанным замечанием об осторожности использования нормального распределения для исследования зависимости использовался критерий хи-квадрат для таблицы сопряженности 5×5 [26]. Получившиеся статистические значения приведены в таблице 3, где для 1% уровня значимости указан результат принятия гипотезы о независимости измерений XгA E и XгA D.
Из данной таблицы следует, что между маркерами XгA E и XгA D есть ярко выраженная связь и она не маскируется ошибками измерений. Интересно, что аналогичный анализ для ПСА и XгA E, а также для ПСА и XгA D показал, что гипотеза о независимости может быть принята (табл. 3), что свидетельствует о том, что XгA E и XгA D являются иными, специфическими характеристиками процессов, протекающих в организме пациентов, нежели чем ПСА.
Таблица 2. Статистический анализ (μ, σ, σ/μ) значений ХгА мужчин контрольной группы
| Маркер | μ | σ | σ/μ | Гипотеза о нормальности распределения | |
|---|---|---|---|---|---|
| Критерий асимметрии | Критерий эксцесса | ||||
| XгA E | 1,31 | 0,59 | 45% | Отвергается | Принимается |
| XгA D | 14,70 | 7,12 | 48% | Отвергается | Отвергается |
Таблица 3. Статистическая зависимость значений ХгА (DAKO и Euro-Diagnostica) и ПСА
| Пара маркеров | χ2 16 | Гипотеза о независимости |
|---|---|---|
| XгA E, ПСА | 21,90 | Принимается |
| XгA D, ПСА | 21,30 | Принимается |
| XгA E, XгA D | 125,67 | Отвергается |
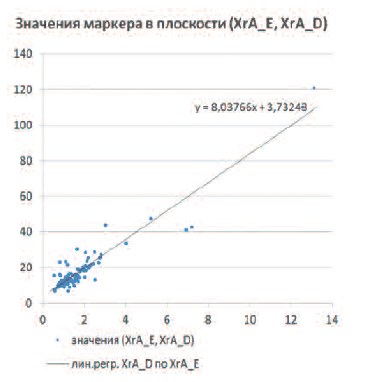
Рис. 1. Линейная зависимость значений XrA (DAKO и Euro-Diagnostica)
Для нашего исследования более важным, чем установление наличия зависимости, является описание закона этой зависимости. Визуальный анализ рисунка 1 позволяет выдвинуть предположение о том, что связь значений измерений маркеров, как для контрольной группы, так и в остальных случаях можно описать как линейную.
Таким образом, приходим к задаче линейного регрессионного анализа [28], решение которой дает следующую модель зависимости:
XгA D=3,73243 + 8,03766•XгA E + εD. (уравнение 1).
Понятно, что совершенно аналогично можно построить регрессию XгA E по XгA D, а именно:
XгA E= – 0,25827 + 0,11287•XгA D + εE. (уравнение 2).
Оценки для квадратичного отклонения ошибки ε принимают соответственно значения 4,66641 для εD и 0,55298 для εE. О степени адекватности построенных регрессионных моделей можно судить по значению так называемого коэффициента детерминации R2 – доли дисперсии прогнозируемой переменной (например, в уравнении 1 – это ХгА D), объясняемой рассматриваемой моделью зависимости (в уравнении 1 – это формула 3,73243+8,03766•ХгА E). Значения R2 обычно представляются в процентах и считается, что для подходящих, хорошо подобранных моделей R2 >50%. Оценка R2 строится с помощью выборочной дисперсии прогнозируемой переменной (в уравнении 1 – это ХгА D) и выборочной дисперсии ошибки представления (в уравнении 1 – это оценка дисперсии εD). При анализе зависимости результатов измерений различными тест-системами получаем значение R2=91%, что говорит о приемлемости выбранной модели линейной зависимости. Заметим, что для рассматриваемой линейной регрессии коэффициент детерминации равен квадрату обычного коэффициента корреляции ρ для ХгА E и ХгА D, т.е. ϱ=√R2=0.95.
Воспользуемся установленной связью между двумя способами измерения ХгА и согласуем результаты по референсным значениям. Имеющаяся контрольная выборка позволяет оценить процентили распределения значений маркера. Соответствующие значения даны в таблице 4.
Строки таблицы привязаны к элементам вариационного ряда для контрольной выборки, по этой причине значения процентов не кратны 10 и имеют не совсем привычный вид. Значение ХгА E =2,99 для 97% (в последней строке таблицы) не противоречит референсным значениям 0-3, поэтому может быть принято за базовое.
Таблица 4. Пороговые значения ХгА для тест-систем DAKO и Euro-Diagnostica
| Частота правильного диагностирования «здоровых» | Пороговое значение для XгA E | Пороговое значение для XгA D |
|---|---|---|
| 41% | 1,03 | 12,60 |
| 52% | 1,18 | 12,94 |
| 59% | 1,20 | 13,20 |
| 69% | 1,40 | 14,49 |
| 79% | 1,86 | 18,20 |
| 90% | 2,48 | 22,85 |
| 97% | 2,99 | 44,00 |
Таблица 5. Число больных с повышенным уровнем ХгА, определенного тест-системами DAKO и Euro-Diagnostica согласно регламентным и согласованным значениям
| Заболевание | n | Регламентные референсные значения | Согласованные референсные значения | |
|---|---|---|---|---|
| ED: >3 нмоль/л | DAKO: >18 Ед/л | DAKO: >28 Ед/л | ||
| Контрольная группа | 29 | 0 | 6 | 2 |
| ДГПЖ | 3 | 0 | 0 | 0 |
| Хронический простатит | 8 | 0 | 1 | 0 |
| ПИН низкой степени | 9 | 0 | 1 | 0 |
| ПИН высокой степени | 5 | 0 | 1 | 0 |
| ЛРПЖ | 24 | 1 | 9 | 3 |
| МРРПЖ | 7 | 0 | 3 | 0 |
| КРРПЖ | 28 | 5 | 13 | 5 |
| ВСЕГО пациентов | 113 | 6 | 34 | 10 |
На основании соотношений в уравнениях 1 и 2 получаем, что средние значения ХгА D и ХгА E при заданных параметрах ХгА E и ХгА D можно вычислить по следующим формулам:
XгA D=3,73243 + 8,03766•XгA E, ХгA E= – 0,25827 + 0,11287•XrA D, из которых видно, что значению ХгA E=3,00 соответствует ХгА D=27.84≈28, а не регламентированное значение 18. Обратно, если бы мы взяли ХгА D=18, то должны были получить ХгA E=1,77.
При согласовании референсных значений (0-3 нмоль/л – для ХгA E и 0-28 Ед/л – для ХгA D) получаем данные, представленные в таблице 5.
Сравнение пары столбцов (ED: 0-3) и (DAKO:2-18) с парой (ED:0-3) и (DAKO:0-28) в этой таблице показывает, что несогласованность значений ХгА, определенных с помощью тест-систем DAKO и EuroDiagnostica, практически исчезла.
ВЫВОДЫ
Исходя из полученных данных, следует отметить: