Повышенная эхогенность предстательной железы что это такое
О чем говорят эхопризнаки диффузных изменений предстательной железы?
Предстательную железу называют «вторым сердцем» мужчины. К сожалению, рано или поздно каждый представитель сильного пола может столкнуться с нарушением функционирования органа. Диффузные изменения в клетках возникают из-за:
Обнаружить эхопризнаки диффузных изменений предстательной железы поможет УЗИ. Исследование обладает высокой информативностью и позволяет поставить максимально точный диагноз без использования инвазивных методик.
В норме простата имеет размеры 3х3х5 см и однородную гомогенную структуру. Контуры органа четкие и ровные, без признаков утолщения или истончения. Пузырьки семени хорошо визуализируются. Если хотя бы один параметр не соответствует нормальным значениям, врач имеет основание подозревать патологические процессы.
Чтобы вовремя обнаружить проблему и пройти лечение, мужчинам старше 40 лет важно выполнять профилактическое обследование предстательной железы для раннего выявления диффузных изменений. Чем быстрее будет поставлен точный диагноз, тем выше вероятность скорого выздоровления.
Что покажет УЗИ?
Во время трансректального ультразвукового исследования датчик максимально приближается к простате, что дает возможность точно оценить состояние органа. Врач-диагност определяет и фиксирует:
По характеру и расположению очагов диффузных изменений в предстательной железе удается диагностировать многие заболевания. Эхопризнаки могут указывать на:
Диагностику заболеваний предстательной железы, лечение эректильной дисфункции в Москве и терапию других патологий проводят опытные специалисты нашей клиники андрологии. Предварительная запись — по телефонам, указанным на сайте.
Повышенная эхогенность предстательной железы что это такое
Ультразвуковая диагностика заболеваний предстательной железы.
Лаврова С. А., Ткаченко П. М.
Минский диагностический центр.
C ростом сети УЗ-службы все большее количество врачей проводят скрининг-диагностику заболеваний предстательной железы и мочевого пузыря. Данный материал преследует цель помочь разобраться в особенностях морфологических изменений, происходящих в предстательной железе при ее патологии и соотнести с УЗ-картиной. Адресован прежде всего специалистам кабинетов УЗИ поликлиник и неурологических стационаров.
На западе рак предстательной железы составляет 20% от общего числа раковых заболеваний, а как причина смерти уступает только опухолям легких. По секционным данным с гистологическим исследованием предстательной железы у 12-47% мужчин старше 50 лет имеются очаги рака. Клинически рак диагностируется реже, так как большой процент от данного числа составляют «малые формы» рака, обладающие малой инвазивностью и при которых пациент умирает от другой патологии.
Для повышения качества диагностики заболеваний предстательной железы важно знать особенности топографической и зональной анатомии данного органа.
Предстательная железа располагается в малом тазу между мочевым пузырем и передней брюшной стенкой, передней стенкой прямой кишки, мочеполовой диафрагмой. Железа имеет форму каштана и плотно охватывает шейку мочевого пузыря и простатическую уретру. Основание железы плотно спаяно с мочевым пузырем. Передняя поверхность направлена к симфизу, а задняя — к ампуле прямой кишки. По задней поверхности расположена выраженная бороздка, из-за которой железу традиционно делят на левую и правую доли. Кроме того, выделяется конусообразная средняя доля, ограниченная спереди простатической уретрой, а сзади — семявыбрасывающими протоками.
Согласно теории зональной анатомии в предстательной железе выделяют 4 железистые зоны (Cхема). От знания их топики во многом зависит правильность интерпретации УЗ-данных. Центральной зоне (ЦЗ) соответствует 20% железистой ткани. Периферическая зона (ПЗ) занимает 75%. Переходным (транзиторным) зонам (ТЗ) принадлежит 5% от общего количества железистой ткани.
Небольшой объем ткани занимают периуретральные железы (ПУЖ), но как раз эта часть железы очень важна для объяснения изменений при доброкачественных гиперплазиях.
Кроме железистой части различают 4 фибромышечные зоны (см. Схему выше):
1) Передняя фибромускулярная строма (ПФС),
2) Гладкомышечные волокна уретры (ГВУ),
3) Препростатический сфинктер (ППС), являющийся продолжением мускулатуры нижней части мочеточника и препятствующий обратной эякуляции,
4) Постпростатический сфинктер (ПОПС), отвечающий за удержание мочи в мочевом пузыре и блокирующий произвольное мочеиспускание.
Исходя из нормальной УЗ-картины при трансабдоминальном поперечном сканировании железу условно делят на 2 части:
-наружную, состоящую из ЦЗ, ПЗ, ТЗ;
-внутреннюю, включающую ПФС, ППС, ПОПС.
Наружная часть выглядит как структура нормальной эхо-плотности, а внутренняя — гипоэхогенная. Наружная и внутренняя части разделены фибромускулярным слоем, т.н. «хирургической капсулой», по ходу которой при оперативных вмешательствах производится разрез, а также идет отложение солей кальция (кальциевая инкрустация железы). Данные образования хорошо видных при УЗИ как гиперэхогенные структуры различного размера, часто дающие эхо-тень.
При обнаружении одного из видов патологических изменений рекомендуем:
— измерение размеров,
— уточнение их локализации,
— проведение гистографии патологического участка и участка ткани с нормальной эхогенностью. Это будет полезно при динамическом наблюдении за пациентом.
Нормальная железа выглядит при трансабдоминальном поперечном сканировании в виде овального образования, при продольном — в виде треугольника с четкими, ровными контурами. Симметричная, с сохраненной во всех отделах капсулой, с более гипоэхогенной внутренней фибромускулярной частью и однородной, средней эхогенности, наружной.
При доброкачественной гиперплазии УЗИ позволяет выявить направление преимущественного роста. При гипертрофии транзиторных зон железа растет по направлению к внутренней части. Образуются «латеральные доли», железа становится шаровидной, увеличенной в размерах, объеме, но сохраняет четкость контура, нормальную эхо-плотность. При трансабдоминальном доступе узлы четко визуализируются не всегда. Трансректальное УЗИ предоставляет наиболее детальную и достоверную информацию и проводится в специализированных стационарах.
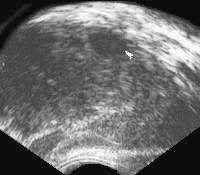
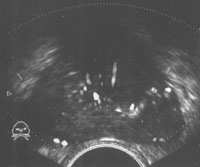
Разросшиеся латеральные доли сдавливают ПЗ и ЦЗ и ведут к их атрофии. При росте парауретральных зон происходит ограничение их гиперплазии мощным фибромускулярным слоем ППС, поэтому при данном виде патологии железа растет по ходу уретры с формированием «средней доли», оттесняющей стенку мочевого пузыря (Рис. 1). Данная патология хорошо визуализируется при продольном трансабдоминальном сканировании (выбухание контура железы в мочевой пузырь со сдавлением его шейки). В начале роста происходит нарушение соотношения внутренней и наружной железистых частей. Кроме различий в зонах преимущественного роста будет отличаться и клиника. При варианте с образованием шаровидной железы (рост ТЗ) железа заметно увеличена, а дизурические явления минимальные, тогда как при образовании «среднекй доли» железа увеличена незначительно, а дизурия — выражена. При декомпенсации сфинктеров развивается недержание мочи, дилятация верхних мочевых путей с последующей атрофией коркового слоя почек, которые постепенно присоединяются к учащенному мочеиспусканию, никтурии, ослаблению напора мочи и замедленному мочеиспусканию, возникающим на начальных стадиях заболевания.

| Рис. 1. Аденоматозные узлы, оттесняющие стенку мочевого пузыря. |
При сдавлении шейки мочевого пузыря можно визуализировать признаки инфравезикальной обструкции, следствиями которой являются морфологические и функциональные изменения в нижних и верхних мочевых путях. В частности, в мочевом пузыре, на начальных стадиях доброкачественной гиперплазии, определяется утолщение стенки с сохранением ее слоистого строения. Утолщение идет за счет компенсаторной гипертрофии детрузора. Затем на сонограммах можно зафиксировать трабекулярность стенки пузыря, а в конечной стадии от перерастяжения происходит ее истончение и уплотнение.
В зависимости от степени выраженности изменений различают 3 стадии доброкачественной гиперплазии предстательной железы:
1. Увеличение железы без наличия остаточной мочи,
2. Наличие остаточной мочи,
3. Присоединение к вышеописанному дилятации верхних мочевых путей и истончение коркового слоя почек.
Кроме этого, необходимо помнить, что в норме у взрослого остаточный объем может быть до 20 ml, а у детей — не превышать 10ml.
Картина острого простатита неспецифична (диффузное увеличение ткани железы, снижение ее эхоплотности с сохранением четкости контура, симметрии, нарушение дифференцировки железы на фибромышечные и железистые зоны) поэтому диагностика должна проводиться в сочетании с пальцевым ректальным исследованием (болезненность при пальпации) и учетом клинико-лабораторных данных.
В случае абсцедирования на фоне общего снижения эхогенности виден еще более гипоэхогенный или анэхогенный фокус с четкими или нечеткими контурами в зависимости от стадии процесса. Участки анэхогенной плотности соответствуют некротическим изменениям. При формировании стенки абсцесса видим снижение инфильтрации ткани вокруг полости и постепенную, при динамическом наблюдении, нормализацию плотности всей ткани. Поствоспалительная киста при адекватной терапии может регрессировать.
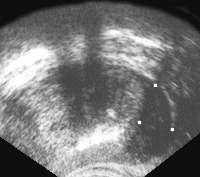
При онкопатологии трансабдоминальный доступ помогает локализовать процесс, оценить целостность капсулы, степень распространенности и вовлечения смежных органов. Минимальный размер опухоли, которую можно определить при трансабдоминальном доступе, составляет приблизительно 8-10 мм., тогда как при трансректальном УЗИ он составит 4-6 мм. 60% опухолевых узлов представлены гипоэхогенными структурами, до 38-40% — изооэхогенными (Рис. 3). Лишь 1% составляют гиперэхогенные опухоли, хотя многими исследователями опухолевый генез данных образований отрицается. Они приводят данные гистологического обследования доказывающие, что участки фиброза и кальцинаты были оценены как опухоли (при трансабдоминальном обследовании кальцинаты малых размеров не всегда дают тень).
 | Рис. 3. Рак предстательной железы. |
1.Трансабдоминальная сонография позволяет диагностировать большинство заболеваний предстательной железы, имеющих макроскопические структурные изменения и, являясь методом скрининг-диагностики, должна дополняться при обнаружении патологических изменений трансректальным исследованием с биопсией.
2. Окончательный диагноз выставляется только с учетом клинико-лабораторных данных, результатов ректального пальцевого исследования в сочетании с трансректальным УЗИ и биопсией.
Неоднородная предстательная железа по результатам УЗИ: основные причины
Предстательная железа — один из самых уязвимых органов в организме мужчины. Она может повреждаться в результате снижения выработки половых гормонов, нездорового образа жизни, инфицирования, переохлаждения. Самые распространенные заболевания простаты — доброкачественная гиперплазия, простатит, опухоли.
С возрастом вероятность возникновения изменений в строении предстательной железы постоянно повышается. Поэтому мужчинам старше 40 лет необходимо регулярно обследоваться у уролога-андролога и ежегодно делать УЗИ. Срочно пройти диагностику необходимо, если Вас беспокоят:
В таких случаях обязательно нужно обратиться к специалисту.
Эхопризнаки неоднородности простаты
Неоднородная предстательная железа может быть диагностирована с помощью УЗИ. На патологию указывают следующие результаты:
Неоднородность структуры предстательной железы и патологические изменения в тканях органа наблюдаются при следующих заболеваниях.
Методы лечения выявленных патологий
Неоднородная структура предстательной железы по результатам УЗИ — повод провести расширенную диагностику: МРТ, КТ. По итогам обследования врач уточняет диагноз и назначает лечение.
В 87% случаев причиной неоднородности простаты является простатит. Для устранения его симптомов предусмотрены противовоспалительная и физиотерапия. Кисты и опухоли подлежат хирургическому лечению.
Диагностика простатита и прочих заболеваний предстательной железы проводится специалистами нашей клиники андрологии в Москве. По результатам обследования специалист подберет эффективную методику терапии, при необходимости направит на операцию. Справки и предварительная запись на консультации — по телефонам.
Диагностика рака предстательной железы
Глава 4. Диагностика рака предстательной железы
Тщательно собранный анамнез помогает установить некоторые особенности заболевания. Симптомы рака предстательной железы, особенно дизурия, развиваются быстро. Иногда постепенно ухудшается общее состояние, больной жалуется на слабость, похудание. Внешний вид пациента изменяется только при далеко зашедшем опухолевом процессе. Истощение и выраженная бледность кожи наблюдаются редко. При осмотре следует обращать внимание на состояние лимфатических узлов, печени, почек, мочевого пузыря, определять количество остаточной мочи. При возникновении подозрения на рак предстательной железы в первую очередь принято проводить три необходимых исследования:
1. Ассиметричная предстательная железа.
2. Плотной или деревянистой консистенции части предстательной железы. Плотность может определяться в виде отдельных узлов, либо различной величины инфильтратов, вплоть до перехода их на стенки таза.
3. Неподвижность железы вследствие сращения ее с окружающими тканями.
4. Пальпируемые семенные пузырьки.
Данные, полученные при пальпации, не всегда легко интерпретировать, так как ложно положительный диагноз рака предстательной железы возможно поставить при следующих обстоятельствах:
1. Доброкачественная гиперплазия предстательной железы.
2. Камни предстательной железы.
4. Флеболиты стенки прямой кишки.
5. Полипы или рак прямой кишки.
6. Аномалии семенных пузырьков.
Результаты пальпации безусловно очень трудно дифференцировать от перечисленных заболеваний, но зато они являются вескими основаниями для дальнейшего обследования больного. В среднем только у одной трети случаев пальпируемых узлов предстательной железы впоследствии гистологически верифицируют рак простаты.
Определение уровня простато-специфического антигена (ПСА). Поскольку простато-специфический антиген имеет большое значение не только для диагностики, но и для лечения и прогноза рака предстательной железы, более подробно остановимся на этом маркере.
В скрининговых программах традиционно используют пороговый уровень в 4 нг/мл для всех возрастных групп. Использование предложенного уровня снижает количество ложно-положительных определений при гиперплазии предстательной железы.
При сравнении предоперационных уровней ПСА с результатами, полученными после простатэктомии, многие авторы отмечают высокую чувствительность и четкую корреляцию со стадией заболевания. Так из ряда работ (Stamey et аl., 1987, 1989), создается впечатление, что концентрация ПСА в сыворотке нелеченных больных пропорциональна объему опухоли в ткани простаты. Несмотря на определенную вариабильность предоперационных уровней ПСА у больных с клиническими стадиями А и В, показано, что его уровни ниже 15 нг/мл и выше 40 нг/мл являются достаточно четкими признаками отсутствия или наличия пенетрации капсулы, инвазии в семенные пузырьки и метастазов в тазовые лимфоузлы, хотя и при уровнях ПСА 15 нг/мл иногда возможна инвазия в капсулу железы.
Увеличение уровня ПСА до больших значений (около 20 нг/мл и выше) является высокоспецифичным даже при нормальных показателях ректального пальцевого исследования простаты. Поэтому при высоких цифрах ПСА биопсия предстательной железы должна проводится обязательно. Уровень ПСА более 50 нг/мл указывает на экстракапсулярную инвазию в 80% случаев и поражение регионарных лимфатических узлов у 66% больных (Stanley et аl., 1990). Исследования Rana et аl. (1992) показали, что результаты ПСА более 100 нг/мл указывают на 100% метастазирование (регионарное или отдаленное).
Наибольшие трудности возникают при интерпретации значений ПСА в диапазоне от 4 нг/мл до 20 нг/мл. Проведенные исследования свидетельствуют о том, что частота рака простаты у пациентов с концентрацией общего ПСА от 4 до 15 нг/мл и нормальными данными при пальцевом ректальном исследовании простаты достигает по разным данным от 27 до 37%.
Помимо первичной диагностики рака простаты, определение ПСА широко применятся в следующих случаях:
1. После радикальной простатэктомии через несколько недель ПСА перестает определяться. Регулярные контрольные исследования (каждые 3 месяца) позволяют своевременно выявить рецидив заболевания в случае повышения ПСА. Если же показатели ПСА нормальны и нет клинических симптомов болезни, то исключаются другие исследования.
2. У больных, получавших лучевую терапию, отмечается значительное снижение уровня ПСА в сыворотке крови, что свидетельствует об эффективном лечении. В то же время, повышение ПСА говорит о малой чувствительности опухоли к проводимому лечению, либо о рецидиве заболевания. Следует отметить, что снижение ПСА до нормальных цифр коррелирует с уровнем антигена до лечения. Пациенты с показателями ПСА до лечения неболее 20 нг/мл имели нормальные показатели ПСА после лечения в 82% случаев. В то же время, у больных с более высокими цифрами ПСА до лечения этот процент составлял лишь 30%. Большинство пациентов со стабильным снижением ПСА оставались в ремиссии в течение последующих 3-5 лет.
3. Целесообразно определять ПСА у больных, получающих терапию антиандрогенами. Повышение уровня ПСА говорит о прогрессировании заболевания и о необходимости сменить характер лечения.
При антиандрогенном лечении уровень ПСА в сыворотке крови является точным индикатором успеха или неуспеха терапии. После начала терапии уровень ПСА быстро снижается у 50% больных (от 85 до 2.1 нг/мл), в то время как в отсутствие ответа величина ПСА не изменяется (Hudson et аl., 1989). Прогрессирование болезни наблюдалось в 50% случаев, когда уровень ПСА не снижался ниже 10 нг/мл. Это означает, что уровень ПСА не играет прогностического значения до начала терапии, в то время как в процессе лечения ПСА является хорошим индикатором эффективности терапии и хорошо коррелируется, как с выживаемостью, так и с длительностью ремиссии. Согласно Stainey (1989), повышение уровня ПСА через 6 месяцев после начала терапии может служить в качестве оценки чувствительности к проводимой терапии.
Простата окружена перипростатической жировой клетчаткой и фасцией, которые формируют гиперэхогенный пограничный слой, который часто описывается как капсула железы. Истинная капсула простаты, если ее удается визуализировать, определяется в виде очень тонкой гипоэхогенной прерывистой линии по поверхности железы.
Семенные пузырьки визуализируются в виде симметричных гипоэхогенных тяжей, расположенных между простатой и мочевым пузырем размерами 2 х 7 см.
Как уже отмечалось выше, рак чаще всего развивается в периферической зоне простаты. Учитывая эту особенность, проще проводить дифференциальную диагностику с другими заболеваниями. Выявляемые структурные изменения, локализирующиеся в пределах центральной зоны, с большей вероятностью могут быть отнесены к проявлению доброкачественного процесса, в то время как обнаружение структурной перестройки, локализующейся в периферической зоне, чаще соответствует злокачественной опухоли.
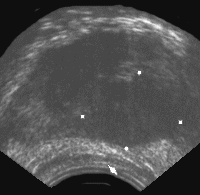
Наиболее характерными признаками рака простаты, локализующегося в периферической зоне, является наличие одного или нескольких узлов неправильной формы и пониженной эхогенности (рис. 4).
Рис. 4. Трансректальное исследование предстательной железы (продольная плоскость на границе периферической и переходной зоны), опухолевый узел (указан стрелкой) не выходящий за пределы органа. Признаков пенетрации капсулы нет.
Диагноз: рак предстательной железы.
Нередко узел окружен гиперэхогенным ободком, что объясняется фиброзной реакцией соединительной ткани предстательной железы, окружающей опухолевый очаг. По мере роста опухоли появляются бугристые контуры железы с признаками пенетрации пограничного слоя (рис. 5 и рис. 6).
Рис. 5. Рак предстательной железы. Опухолевый узел в периферической зоне левой доли, инфильтрирует заднебоковую поверхность железы и перипростатической клетчатки.
Рис. 6. Трансректальное исследование предстательной железы (поперечная плоскость). Опухолевый узел в периферической зоне левой доли. Отмечается деформация наружного контура железы, признаки пенетрации собственной капсулы. (Т3) Диагноз: рак предстательной железы.
Особенно большое значение имеет выявление инфильтрации по передне-боковой поверхности железы, которая недоступна пальцевому исследованию.
Наиболее сложными для диагностики являются опухоли, которые локализуются в центральной и переходной зонах железы. Зачастую, развиваясь на фоне доброкачественной гиперплазии, рак по эхогенности практически не отличается от окружающих тканей, в связи с чем нередко возникают диагностические ошибки, а диагноз устанавливается при гистологическом исследовании удаленного материала во время операции.
По мере увеличения опухолевой инфильтрации стромы железы меняется ее ультразвуковая структура. Ткань железы становится неоднородной, с беспорядочными отражениями низкой интенсивности. Ультразвуковая томография позволяет выявить инфильтрацию капсулы простаты, семенных пузырьков мочевого пузыря, стенки прямой кишки, лимфатических узлов, что, естественно, позволяет уточнить стадию заболевания.
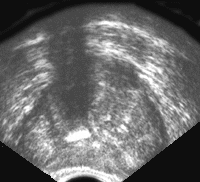
В отличие от рака, гиперплазия предстательной железы обычно развивается в переходной зоне по направлению к внутренней части железы. При этом переходная зона начинает сдавливать центральную и периферическую зону, вызывая их постепенную атрофию. Из центральной и периферической зон и фибромышечных слоев формируется «хирургическая капсула», по которой происходит «вылущивание» гиперплазированных узлов при операции. По мере роста доброкачественной гиперплазии железа приобретает шаровидную форму; при преимущественном росте периуретральных желез отмечается выбухание контура железы в просвет мочевого пузыря и формируется средняя доля, которая растет, оттесняя кпереди и деформируя заднюю стенку мочевого пузыря, сдавливая в значительной степени простатическую уретру и шейку мочевого пузыря. Поскольку доброкачественная гиперплазия предстательной железы не характеризуется инфильтративным ростом, то капсула железы обычно четко прослеживается по периферии среза. Частыми находками при доброкачественной гиперплазии являются мелкие ретенционные кисты и кальцинаты, генез которых связан со сдавлением протоков железы гиперплазированной тканью; располагаются они чаще всего по т.н. хирургической капсуле. При ультразвуковом исследовании простаты порой возникает необходимость проводить дифференциальную диагностику с простатитом. Это вызвано тем, что пальпация предстательной железы при простатите иногда дает результаты, очень похожие на рак. Ультразвуковое исследование в стадии отека и инфильтрации железы выявляет: увеличение железы (рис. 7 и рис. 8), изменение ее формы (чаще шаровидная) и структуры. Снижается эхогенность железы, теряется эхографическая дифференциация железистых и фибромышечных зон.
Рис. 7. Трансректальное исследование предстательной железы (поперечная плоскость). Хронический простатит с участками кальцификации в железе.
Рис. 8. Хронический простатит; усиление кровотока в ткани железы (режим энергетического Доплера).
Описанные три основных метода диагностики в дальнейшем требуют обязательного морфологического подтверждения заболевания. С этой целью выполняется пункционная биопсия, которая наиболее достоверна при выполнении ее под контролем ультразвука. Особенно это касается обследования больных с малыми образованиями.
Биопсию предстательной железы можно производить через промежность, трансректально или трансуретральным доступом. Открытая биопсия применяется крайне редко. Трансуретральная резекция предстательной железы не только позволяет уточнить диагноз, но и обеспечивает восстановление мочеиспускания.
В диагностике рака предстательной железы частота ложноотрицательных результатов гистологического анализа кусочков ткани при промежностном и трансректальном доступе не превышает 20%.
Осложнения пункционной биопсии встречаются крайне редко и могут быть связаны с повреждением мочевого пузыря и мочеиспускательного канала. Возможна гематурия, гематоспермия, промежностная и позадилобковая гематома. Для профилактики инфекционных осложнений, которые составляют около 2%, за сутки до биопсии и после нее назначают антибиотики.
В некоторых сложных случаях дифференциальной диагностики с успехом применяют цитологическую диагностику рака предстательной железы. Для цитологического исследования используют аспират из предстательной железы.
Из методов диагностики рака предстательной железы заслуживает внимания рентгеновская компьютерная и магнитно-резонансная томография. Получаемая при этом информация соответствует таковой при ультразвуковом исследовании. На томограммах также видны структура предстательной железы, опухолевые узлы, их величина, степень прорастания капсулы, инфильтрация мочевого пузыря, семенных пузырьков, окружающей клетчатки. Эти методы, однако, оказались не более точными, чем трансректальное УЗИ при определении стадии ограниченного местного роста рака предстательной железы, и, более того, есть данные, что трансректальное ультразвуковое исследование дает более надежные результаты при оценке стадии заболевания.
Экскреторная урография позволяет оценить функцию почек и уродинамику верхних мочевых путей. Уретероэктазия и уретерогидронефроз являются следствием сдавления тазовых отделов мочеточников опухолью. Такие изменения часто бывают односторонними. При полной обструкции мочеточника происходит выключение почки, при этом тень рентгеноконтрастного вещества на стороне сдавления отсутствует.
Определение стадии заболевания. За установлением диагноза рака предстательной железы одновременно встает вопрос об установлении стадии заболевания, что в конце концов определяет характер будущего лечения. Кратко остановимся на возможностях применяемых методов исследования в установлении стадии заболевания.
Пальцевое исследование прямой кишки. Точность диагностики рака предстательной железы при пальцевом исследовании прямой кишки составляет 30-50%. Часто наблюдается недооценка стадии, поскольку небольшие, расположенные в передних отделах железы опухоли, как правило, не пальпируются; ложноположительные результаты наблюдаются у больных с гиперплазией предстательной железы и простатитом. Этот метод однако позволяет выявить рак предстательной железы, когда уровни ПСА остаются в пределах нормы, и предоставляют хотя не точные, но полезные данные о стадии заболевания. Пальпируемый неподвижный опухолевый инфильтрат или прорастание в кишку говорят о далеко зашедшем опухолевом процессе (Т4).
Определение простатического специфического антигена. При оценке отмечается достаточно четкая корреляция между уровнями ПСА и гистологической (и в меньшей степени клинической) стадией рака предстательной железы. У каждого конкретного больного корреляция не столь сильна из-за значительного перекрывания пределов различных возрастных норм. Уровни 10-20 нг/мл часто являются показателем опухоли, прорастающей за пределы капсулы предстательной железы, уровни выше 40 нг/мл свидетельствуют о наличии метастазов.
Хотя сывороточные уровни ПСА сами по себе не являются надежным показателем стадии заболевания, их можно использовать, чтобы избежать некоторых исследований. Выдвинуто предположение, что больным с вновь выявленным раком предстательной железы без симптомов поражения костей и при уровнях ПСА не выше 10 нг/мл не требуется проводить сцинтиграфию костей для определения стадии. У таких больных вероятность метастазов в костях приближается к нулю, хотя многие практические врачи считают этот метод исследования основным, так как при его помощи можно диагностировать «горячие точки», как например, остеоартроз позвоночника, который позже может создать путаницу в оценке симптомов. По данным Walsh et Partin (1994) при предоперационном ПСА 20нг/мл рецидива не было только у 45%.
Казалось бы приведенные цифры убедительно показывают значимость ПСА для прогноза заболевания, но тем не менее надо принимать во внимание и другие исследования. По данным Элиса (1994) у 21% больных с ПСА 3 ;
4) у 37% больных с дооперационной стадией T1c найден распространенный рак (пенетрация капсулы), или опухоль по краю резекции, или инвазия семенных пузырьков, или наличие метастазов в регионарные лимфатические узлы).
Таблица 15. Ошибки клинического стадирования 3170 больных, подвергнутых радикальной простатэктомии по поводу клинически локализованного РПЖ (стадии Т2с и меньше) (Zincke et аl., 1994).
| Клиническая стадия | Число больных (%) | Паталогоанатомическая стадия | |||
| Ограничена предстательной железой | рТ3 | PN+ | Опухоль по линии резекции | ||
| Т1а | 49 (1.5%) | 44 (88%) | 4 (8%) | 1 (2%) | 2 (4%) |
| T1b | 177 (5,6%) | 120 (68%) | 46 (16%) | 11 (6%) | 35 (20%) |
| Т2а | 897 (28%) | 512 (57%) | 330 (37%) | 55 (6%) | 140 (16%) |
| T2b,с | 2047 (65%) | 82 (40%) | 959 (47%) | 267 (13%) | 593 (29%) |
| Всего: | 3170 (100%) | 1497 (47%) | 1339 (42%) | 334 (11%) | 770 (24%) |
Остановимся на значении степени дифференцировки опухоли и показателя Глисона. Каково их значение для решения вопроса о выборе метода лечения больного. Понятно, что целесообразность простатэктомии определяется:
1) наличие или отсутствие пенетрации опухолью капсулы простаты;
2) наличие опухоли по краю разреза;
3) по объему опухоли;
4) инвазия семенных пузырьков;
5) метастазы в лимфатических узлах.
При просмотре этих показателей у больных после простатэктомии в зависимости от показателей Глисона выяснилась прямая закономерность: чем меньше показатель Глисона, тем меньше вероятность большого распространения опухоли. И наоборот, чем больше показатель Глисона, тем больше вероятность распространения опухоли за пределы капсулы, тем больше вероятность рецидива опухоли (таб. 16).
Таблица 16. Корреляция между показателями Gleason и гистологическими данными простатэктомии.
| Гистологические данные | Gleason | |||
| 5 | 6 | 7 | 8-10 | |
| Пенетрация капсулы | 16% | 24% | 62% | 85% |
| Опухоль по краю разреза | 20% | 29% | 48% | 59% |
| Инвазия семенных пузырьков | 1% | 4% | 17% | 48% |
| Метастазы в лимфоузлы | 1% | 2% | 12% | 24% |
| Средний объем опухоли (см 3 ) | 2.2 | 2.7 | 5.1 | 4 |
Так при показателе Глисона 8-10 пенетрация капсулы встречается чаще в 4 раза, чем при показателе 5, опухоль по краю разреза в 3 раза, объем опухоли больше в 2 раза, инвазия семенных пузырьков в 48 раз и метастазы в лимфатических узлах в 24 раза.
Исходя из приведенных данных можно сделать следующие выводы:
1. У больных с показателями Глисона 8-10 и метастазами в лимфатические узлы операция не целесообразна. Тем не менее, если больной все же оперируется с показателем Глисона 8-10 необходимо перед простатэктомией произвести срочное гистологическое исследование всех лимфатических узлов удаляемых во время тазовой лимфаденэктомии. При подтверждении метастазов простатэктомия не выполняется.
2. При показателе Глисона менее 8 лимфатические узлы можно исследовать в плановом порядке.
3. При показателе Глисона 7 больного следует оперировать.
4. При показателе Глисона менее 7 в зависимости от возраста, общего состояния больного можно наблюдать.