ущемленная вентральная грыжа код по мкб 10 у взрослых
Грыжа передней брюшной стенки с непроходимостью без гангрены (K43.0)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Этиология и патогенез
Эпидемиология
Возраст: преимущественно молодой и зрелый
Признак распространенности: Редко
Соотношение полов(м/ж): 1.5
Факторы и группы риска
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Местные симптомы кишечной непроходимости:
— невправимость грыжи;
— появление или усиление боли или изменение ее характера в области грыжи;
— напряженность грыжевого мешка;
— изменение цвета кожи над ним и появление локального отека (редко).
Диагностика
Лабораторная диагностика
2. Общий анализ мочи:
— повышение удельного веса, цвета;
— снижение темпа диуреза;
— возможно умеренное повышение уровня индикана (редко).
3. Биохимия:
— нарушения электролитного состава (гипохлоремия, гипокалиемия) и гипопротеинемия могут отчасти маскироваться гемоконцентрацией;
— возможна небольшая гиперазотемия (редко);
— повышение уровня С-реактивного белка;
— повышение уровня молочной кислоты (гиперлактатемия, лактатацидоз) свидетельствует об ишемии стенки кишечника, при этом снижение уровня лактата в динамике (в том числе и после оперативного лечения) не означает отсутствия ишемии стенки кишечника.
Дифференциальный диагноз
Осложнения
Лечение
Оперативное вмешательство не должно откладываться на значительный срок для проведения предоперационной подготовки, за исключением редких случаев:
— острого нарушения мозгового кровообращения;
— острого инфаркта миокарда;
— острых значительных нарушений гемодинамики, дыхания, свертывающей системы крови.
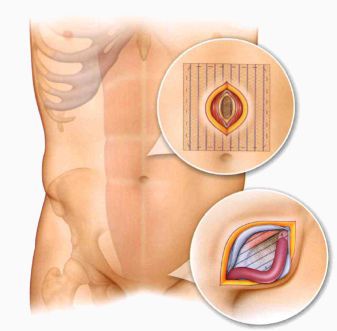
Методически операция не отличается от таковой при прочих ущемленных грыжах, за исключением доступа. В ходе операции выделяется и вскрывается грыжевой мешок, производится рассечение грыжевого кольца, оценивается жизнеспособность ущемленных участков кишечника, с целью предотвращения распространения инфекции отграничивается операционное поле. Пластика производится либо местными тканями, либо ненатяжными методиками с использованием сетчатого трансплантата.
При аллергии на лактамы альтернативным подходом является назначение комбинаций:
— клиндамицин+гентамицин или азтреонам или фторхинолоны;
— метронидазол+гентамицин или фторхинолоны (ципрофлоксацин или левофлоксацин).
АБП должна проводиться в срок за 60 минут до начала операции, за исключением фторхинолонов, которые требуют более длительного времени для парентерального введения (начало введения за 2-3 часа до операции).
Что такое грыжа послеоперационная вентральная? Причины возникновения, диагностику и методы лечения разберем в статье доктора Хитарьян А. Г., флеболога со стажем в 31 год.
Определение болезни. Причины заболевания
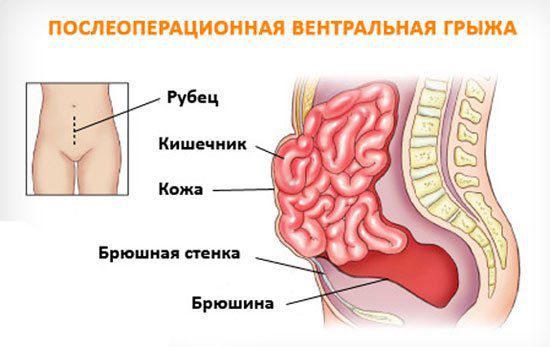
Вентральная грыжа — это распространенное заболевание, при котором наблюдается пролабирование внутренних органов, покрытых париетальной брюшиной, или их частей через естественные или искусственные отверстия в мышечно-апоневротическом каркасе. [3]
Послеоперационными вентральными грыжами (ПВГ) называют грыжи, возникшие после выполнения операции по поводу любого хирургического заболевания, кроме грыж брюшной стенки. [8] [9]
Термин «вентральная грыжа» ввел ученый и врач Клавдий Голен в 129-199 гг. н. э. Будучи анатомом, хирургом и основателем экспериментальной физиологии, он занимался так же лечебной деятельностью и практикой. Сведения о грыжах также встречаются в работах Гиппократа (V в. до н.э.), Цельса (I в. до н.э.) и других авторов. [1]
Существуют предрасполагающие и производящие факторы развития послеоперационных грыж. Предрасполагающие факторы: [3] [6] [21]
Производящие факторы: [3] [6] [21]
Симптомы послеоперационной вентральной грыжи
Вентральная грыжа чаще всего протекает бессимптомно. Одним из главных признаков данного заболевания является выявление выпячивания в одной или нескольких областях живота. Причем выпячивание появляется только при выполнении физнагрузки, натуживании, сильном кашле, чихании. Если после этого содержимое грыжевого мешка возможно погрузить, то можно говорить о том, что данная грыжа без ущемления. Если появляются жалобы на чувство жжения, болезненности, невозможности погружения содержимого грыжевого мешка и увеличение выпуклости в размерах, это уже признаки ущемления.
Патогенез послеоперационной вентральной грыжи
Все вентральные грыжи по образованию можно распределить на дистрофические и травматические.
К травматическим относятся все грыжи, которые возникают вследствие получения какой-либо травмы или выполнения оперативного вмешательства. Все остальные относятся к дистрофическим.
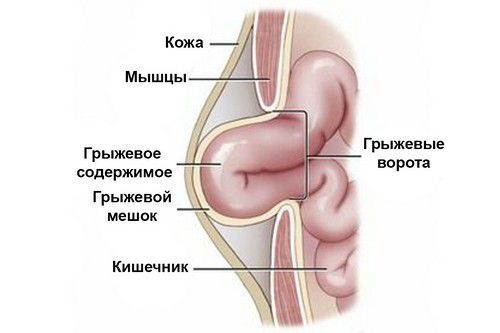
Любая вентральная грыжа имеет следующие составляющие:
Основное значение в этиопатогенезе грыж отводится дисбалансу между давлением в брюшной полости и возможностью мышечно-апоневротического каркаса выдерживать это давление. Две основные силы, которые действуют на послеоперационный рубец — это внутрибрюшное давление и напряжение мышц брюшной стенки. Если же рубец не выдерживает давления, появляется дефект, который нарушает мышечно-апоневротическую функцию брюшной стенки.
Появление грыжевого выпячивания наиболее ожидаемо у людей, у которых имеют место различного рода послеоперационные осложнения в первые полгода после вмешательства, т. к. в слоях передней брюшной стенки долгое время сохраняется воспаление. Известно также, что после перенесенного осложнения в передней брюшной стенке долгое время сохраняется воспаление. [7] [16] Есть данные и о непосредственной связи возникновения грыжи с заболеваниями периферической нервной системы. Основную роль в развитии послеоперационных вентральных грыж и их рецидивов играют нарушения в процессах формирования послеоперационного рубца, т. е. высокое количество тонких коллагеновых волокон с низкой плотностью. Вследствие дегенеративных изменений мышечно-апоневротический слой замещается рубцовой тканью, и это негативно сказывается на прочности стенки. Таким образом, нарушения в процессах метаболизма соединительной ткани являются, пожалуй, одним из главных факторов развития ПВГ. Это необходимо учитывать при выборе метода герниопластики и отдавать предпочтение методам малоинвазивным и безнатяжным, т. к. ткани, сшиваемые без значительного натяжения, не оказывают существенного влияния на функциональное и морфологическое состояние мышечно-апоневратического каркаса, и это не приводит к значительному повышению внутрибрюшного давления.
Классификация и стадии развития послеоперационной вентральной грыжи
В современной литературе нет единой общепринятой классификации вентральных грыж.
Грыжи делятся по следующим позициям:
1. Локализация (срединная (М); боковая (L); сочетанная (ML));
2. Размер грыжевых ворот (W1 (до 5 см); W2 (5-10 см); W3 (10-15 см); W4 (более 15 см);
3. Наличие или отсутствие рецидива (R1; R2; R3; R4).
2. Определять величину ПВГ можно по классификации К.Д. Тоскина и В.В. Жебровского (1980). [22] [25]
Кроме того, необходимо учитывать, вправимая грыжа или невправимая, ущемленная или нет.
Выделяют также три наиболее часто встречающихся варианта нарушения топографии брюшной стенки при ПВГ:
1 вариант — грыжевой дефект расположен по средней линии и образован срединными краями прямых мышц, без нарушения целостности самих мышц;
2 вариант — грыжевой дефект не только разрушил белую линию живота, но и имеет место нарушение анатомической целостности прямых или боковых мышц передней брюшной стенки, а также их апоневротических футляров;
3 вариант — когда имеются признаки 1 и 2 варианта, но отличие заключается в площади дефекта (15×15 см и более), а также наличие атрофии мышц и истончение апоневротических структур.
Диагностика послеоперационной вентральной грыжи
Основным методом диагностики грыжи являются физикальный осмотр, пальпация и сбор анамнеза.
Лечение послеоперационной вентральной грыжи
Для хирургического лечения ПВГ предложено огромное количество разнообразных способов, различающихся в основном техникой выполнения закрытия и укрепления грыжевых ворот (герниопластики). [24] Все способы герниопластики ПВГ можно разделить на две группы: пластика с использованием местных тканей и пластика с использованием дополнительных пластических материалов. Также возможна комбинация этих способов.
Герниопластика местными тканями
Существуют несколько способов герниопластики с использованием местных тканей:
Несмотря на большой риск развития рецидивов, пластика местными тканями имеет место в хирургической практике. Чаще всего данные способы применяются у детей и молодых женщин.
Пластика грыжевых ворот с использованием дополнительных пластических материалов
Пластика с использованием консервированной твердой мозговой оболочки
Среди гомопластических методик самой актуальной являлось лишь использование твердой мозговой оболочки, и немало хирургов, особенно в России, использовали для пластики консервированную твердую мозговую оболочку, особенно при больших и гигантских ПВГ. [2] Широкое применение пластика твердой мозговой оболочкой получила в клинике К. Д. Тоскина, где эта пластика применяется с 1972 г. Можно отметить хорошие результаты, так, на 252 операции имеет всего 1,8% рецидивов и 5,6% раневых осложнений. В современной герниологии данная методика не используется, так как к проблемам, связанным с заготовкой и хранением имплантатов, присоединилась проблема ВИЧ-инфекции и гепатита.
Пластика с использованием аутодермы
В связи с простотой выполнения и меньшей травматичностью (по сравнению с использованием аутофасции) среди аутопластических методик актуальной осталась лишь аутодермальная пластика. Эти способы и аллопластика с применением искусственных протезов и составляют базис современных пластик с использованием дополнительных пластических материалов. Первый опыт применения кожи для герниопластики принадлежит G. Simоn в 1881 г. Кожа при этом рассекалась вокруг грыжевого выпячивания, внутренние края сшивались между собой, и грыжевой мешок с ушитым кожным лоскутом погружался за счет сшивания наружных краев кожного разреза. Данная методика сопровождалась большим количеством рецидивов и специфических осложнений, например образованием дермоидных кист. При аутодермальной пластике важным моментом является фиксация кожного лоскута с некоторым натяжением, а также ранняя активизация больных. Такое перерождение кожного лоскута активно использовалось сторонниками аутодермальной пластики для широкой пропаганды этого метода. Одной из главных осталась проблема осложнений области раны и приживления трансплантата. Еще одним препятствием явилось то, что кожный лоскут перерождается не в плотную апоневротическую ткань, а в рубцовую рыхлую соединительную, стойкость к физическим нагрузкам у которой значительно меньше. Использование же аутодермальной пластики при лечении больших грыж с кишечными и/или лигатурными свищами вообще нецелесообразно. [12]
Использование синтетического материала
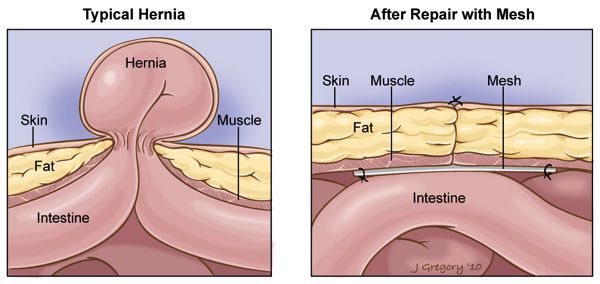
С 40-х годов XX века начался новый этап в герниологии, связанный с синтезом высокомолекулярных полимеров, пригодных для имплантации в ткани организма человека. Разработка, внедрение и использование современных полимерных материалов значительно расширили возможности протезирующей герниопластики ПВГ практически любых размеров. [10] В настоящее время протезирующая герниопластика является базовым методом лечения пациентов с ПВГ. Однако при протезирующей герниопластике встает вопрос об специфических осложнениях — серомах, из-за длительной экссудации реактивной жидкости в области протеза. [18] Частота осложнений может зависеть от многих факторов, начиная от используемого протеза и заканчивая способом его имплантации. На сегодняшний день, помимо техники хирурга, необходимо учитывать характеристики синтетических полимерных материалов для повышения эффективности протезирующих способов, поскольку осложнения, связанные с низким качеством протеза, могут перечеркнуть даже самую совершенную хирургическую технику. Применение таких материалов, как капрон, поролон, поливинилалкоголь, фторопласт и многих других увеличило частоту инфильтратов, сером и нагноений, длительно не заживающих свищей, секвестрации трансплантатов. [14] Некоторые авторы писали о канцерогенности пластмасс при их длительном пребывании в организме. [3] [17] [24] Учитывая все вышесказанное, синтетический материал для герниопластики должен быть химически инертным, прочным, эластичным, удобным для стерилизации и доступным по стоимости, протез не должен обладать канцерогенными и провоспалительными свойствами.
С развитием лапароскопической герниологии в последнее время появилось дополнительное требование — возможность образовывать барьер для развития спаек со стороны брюшной полости. J.P. Аmid (1997) выделяет четыре вида синтетических материалов:
Вид № 1 — тотально-микропористый эндопротез (атриум, марлекс, пролен, трелекс). Диаметр микропор у данного типа более 75 мкм. Через эти поры проникают свободно макрофаги, фибробласты, капилляры, коллагеновые волокна.
Вид №2 — тотально-микропористый протез (Gоre-Tex; хирургическая мембрана и двойная сеть) с размером микропор меньше 10 мкм.
Вид №3 — макропористый эндопротез с мультифиламентным компонентом (тефлон, мерсилен, дакрон, плетеная полипропиленовая сеть).
Вид № 4 — материалы с субмикроскопическими порами. Материалы 4-го типа практически не пригодны для пластики, однако в ряде случаев используются в сочетании с протезами 1-го типа для внутрибрюшной имплантации. В случаях инфицирования материала при порозности его волокон менее 10 мкм, протезы приходится полностью удалять, так как оставление его ведет к образованию хронического очага инфекции. Вышеописанные свойства встречаются в плетеных и крученых нитях, вследствие этого хороший протезный материал должен состоять из монофиламентных нитей. Основным материалом, отвечающим требованию, является полипропилен, при изучении которого не было выявлено признаков отторжения, канцерогенности и рассасывания с течением времени. На его основе были созданы ткани монофиламентная полипропиленовая сетка Mаrlex, бифиламентная полипропиленовая сетка Prоlene, полифиламентная полипропиленовая сетка Surgiprо, которые применяются и по сей день. Также диаметр пор материала определяет скорость и качество его вживления в ткань организма. Было доказано, что при размере пор более 75 мкм имплант в течение месяца на всю толщу прорастает коллагеновыми волокнами и фиброцитами, тогда как при порах меньшего размера превалирует гистиоцитарная инфильтрация и, как следствие, более слабая фиксация синтетического материала в тканях организма.
Использование протезов Mаrlex и Prоlene, размеры пор которых составляют 100 мкм, позволило снизить частоту раневых инфекционных осложнений по сравнению с лавсаном (мерсиленом) с 15% до 5%, а образование свищей — с 15% до 2%. Экспериментально было доказано, что оптимальный размер пор равен 2-3 мм. [22] Протезы из политетрафлюороэтилена (Gоre-Tex) достаточно инертны, сопоставимы с полипропиленом, однако адгезивные свойства их меньше, ввиду чего менее прочно вживляются в ткань организма. Помимо этого, их применение довольно часто осложняется хроническим инфицированием тканей. J.J. Bаuer с соавт. (2002) сообщает об использовании Gоre-Tex при операциях по поводу обширных грыж, результатом явилось нагноение раны у 7,1% и рецидив грыжи у 10,7% больных, у одного пациента протез пришлось удалить. Поэтому Gоre-Tex применяется исключительно при лапароскопических герниопластиках, при которых вероятность инфицирования протеза сведена к минимуму ввиду напряженного карбоксиперитонеума. [10]
Более нежный соединительнотканный рубец позволяет формировать применение так называемых «облегченных» сеток (Viprо, Viprо-2, Ultrаprо), то есть сеток с уменьшенным количеством полипропилена на единицу площади протеза, что уменьшает интенсивность воспалительной реакции. В настоящее время широкое применение получили полипропиленовые сетки PMS (6 11 см), PMM (15 15 см), PML (30 30 см), PMH, выпускаемые фирмой «Ethicоn»; полипропиленовые сетки SPMM-35 (7 13 см), SPMM-66 (15 15 см), SPMM-135 (22 33 см), выпускаемые корпорацией «TYCО», а также монофиламентная полипропиленовая сетка, выпускаемая санктпетербургской фирмой «Линтекс». [22] Использование других синтетических материалов нежелательно, поскольку увеличивает риск хронического инфицирование протеза, неизбежно требующее полного его удаления.
В мире ежегодно используется около 1 миллиона сетчатых имплантов для герниопластики. В некоторых странах до 90% всех грыж оперируется с использованием сетчатых полипропиленовых протезов. [22]
Среди методов протезирующей герниопластики можно выделить две большие группы: «ненатяжные» способы и комбинированные. Суть ненатяжной пластики заключается в использовании для закрытия грыжевого дефекта собственных тканей больного без полной адаптации (соприкосновения) краев грыжевого дефекта в комбинации с сетчатым протезом. При этом сетка может размещаться и фиксироваться различными способами, по принципу оnlаy, inlаy, оnlаy+inlаy, sublаy. При комбинированной протезирующей пластике грыжевой дефект устраняется полностью местными тканями, путем сопоставления и послойной полной адаптации его краев (натяжная пластика), благодаря чему происходит восстановление нормального топографо-анатомического строения брюшной стенки и ее функции, и дополнительно укрепляется протезом, который может располагаться по принципу оnlаy или sublаy. На основании вышеизложенного натяжную пластику многие хирурги-герниологи называют радикальной, а ненатяжную — паллиативной. Однако полное, послойное сопоставление топографо-анатомического строения брюшной стенки при обширных и гигантских грыжах, к сожалению, не всегда представляется возможным.
Ненатяжные способы протезирующей герниопластики
Суть заключается в пластике грыжевых ворот экзогенным материалом без какой-либо адаптации краев дефекта. Существует большое количество разнообразных способов ненатяжной герниопластики, отличающихся как способами размещения протеза, так и способами их фиксации. Основные способы ненатяжной герниопластики:
В девяностые годы были предложены для пластики гигантских грыж различные способы:
Комбинированные способы протезирующей герниопластики
В случаях применения «комбинированных способов» пластики закрытие грыжевого дефекта включает в себя один из вышеперечисленных способов апоневротической пластики только за счет местных тканей, а протез фиксируется над или под апоневрозом. Выбор того или иного метода пластики осуществляется хирургом индивидуально, в зависимости от вида и размера грыжи, состояния местных тканей, возраста пациента и наличия сопутствующей патологии.
На основании опыта хирургического лечения 188 пациентов с обширными и гигантскими грыжами В.Г. Лубянский с соавт. (2008) установили, что у больных до операции имеются нарушения функции брюшно-кавальной помпы, связанные с разрушением передней брюшной стенки и снижением подвижности купола диафрагмы. Часть кишечника при этом располагается за пределами брюшной полости. Всё это обуславливает низкое внутрибрюшное давление, что, в свою очередь, приводит к обструктивным и рестриктивным заболеваниям лёгких. При реконструкции передней брюшной стенки происходит восстановление работы брюшно-кавальной помпы, это обеспечивает увеличение скорости венозного кровотока в бедренной вене и является основой профилактики тромбоэмболических осложнений.
Вышесказанное обуславливает преимущество применения комбинированных методов протезирующей герниопластики вентральных грыж перед ненатяжными, заключающееся в устранении дооперационного патологического взаиморасположения анатомических структур передней брюшной стенки и восстановления физиологических свойств брюшного пресса. Чтобы предотвратить угнетение моторики кишечника, поднятие диафрагмы и смещение органов грудной клетки, которые могут привести к нарушению сердечной деятельности, дыхания и развитию абдоминального компартмент-синдрома, определяются четкие показания к тому или иному виду операции. Особое значение имеет предоперационная подготовка больных и своевременная профилактика сердечно-легочных осложнений в раннем послеоперационном периоде. По данным В.Н. Егиева и Д.В. Чижова (2004), применение комбинированной пластики дает до 20% рецидивов заболевания. [22] Большинcтво отечеcтвенных и зарубежных авторов отмечают от 15 до 35% рецидивов при пpотезирующей герниоплаcтике обширных и гигантских ПВГ.
Эндовидеохирургические методики протезирующей герниопластики
Новые горизонты в герниохирургии открывает малоинвазивная лапароскопическая техника, которая позволяет нивелировать многие недостатки традиционной герниопластики. Переворот в герниопластике в 1993 году совершил Karl LeBlanc, который предложил новую методику лапароскопической герниоплатики, при выполнении которой сетчатый эндопротез устанавливался внутрибрюшинно и его фиксация осуществлялась лапароскопически. Данная тактика в мировой литературе получила название IPOM (intraperitoneal onlay mesh). Техника IPOM предусматривает закрытие грыжевого дефекта с помощью специальных сетчатых эндопротезов, отличительной особенностью которых является двухслойное строение. Одна сторона сетки покрыта специальным раствором, который не вызывает адгезии при контакте с внутренними органами, вторая, наоборот, с адгезивными свойствами, чтобы как можно прочнее соединиться с брюшиной. Сетка подвешивается с помощью нерассасывающихся лигатур в брюшной полости и фиксируется с по периметру с помощью такеров. По оригинальной технике LeBlanc такеры были металлическими. Однако при классической IPOM-технике возрастает риск образования послеоперационных сером, гранулем грыжевого мешка, поэтому данная техника модифицируется.
Передовая методика в хирургии пупочных и вентральных грыж с эндопротезом Ventralex ST
Для выполнения операции по этой технологии пупочная или вентральная грыжа должна быть ранее не оперирована и с размером грыжевых ворот не более 6 кв. см. Оперативное вмешательство выполняется через небольшой герниотомический разрез и еще один дополнительный троакарный доступ в 5 мм. Под эндотрахеальным наркозом по левому флангу устанавливается 5 мм троакар. После выполняется герниотомический разрез до 1.5—2 см в области выпячивания и резецируется грыжевой мешок с его содержимым. Удаление содержимого грыжевого мешка безопасно, т. к. до этого было выполнение лапароскопии и выявлено, что нет риска повреждения внутренних органов. В брюшную полость вводится эндопротез Ventralex, напоминающий по форме гриб, имеющий, как было сказано ранее, две поверхности — фиксирующую и защитную. После установки эндопротеза Ventralex выполняется повторно лапароскопия для проверки качества установки протеза. После накладываются несколько кожных швов, и операция закончена.
Лечение пупочных и вентральных грыж этим способом имеет ряд преимуществ:
По данным многих авторов, частота осложнений после лапароскопической герниопластики колеблется от 2 до 26%, а частота рецидивов заболевания варьирует от 0 до 17%. Одним из основных настораживающих моментов при применении лапароскопии для лечения ПВГ является наличие длительного спаечного процесса в брюшной полости. При установке портов высока вероятность повреждения органов брюшной полости, вовлеченных в спаечный процесс.
Прогноз. Профилактика
По данным литературы, процент развития грыж после лапаротомий колеблется от 5 до 19% среди всех вмешательств. Грыжа является самым распространенным заболеванием в хирургии, и основное оперативное вмешательство в любом уголке мира — герниопластика. Несмотря на большое количество методов пластики, проблема рецидивов не решена и по сей день.
Необходимые условия для снижения риска развития рецидивов:
Грыжа передней брюшной стенки без непроходимости или гангрены (K43.9)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Примечание. В данную подрубрику включены:
— надчревная грыжа живота;
— инцизионная грыжа живота.
Согласно принятому Европейским обществом герниологов определению, инцизионной грыжей называют «любой дефект брюшной стенки с или без выпячивания в области послеоперационного рубца, выявляемый пальпаторно при клиническом осмотре или с помощью визуализации».
Некоторые авторы относят к грыжам белой линии живота также околопупочную грыжу, которая согласно МКБ-10 кодируется в другой подрубрике (см. «Пупочная грыжа без непроходимости или гангрены»- K42.9).
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Единая классификация как врожденных, так и приобретенных грыж передней брюшной стенки отсутствует.
Грыжи белой линии
По месту образования делятся на:
Примечание. Околопупочные грыжи рассматриваются МКБ-10 в подрубрике «Пупочная грыжа без непроходимости или гангрены» (K42.9).
Классификация инцизионных вентральных грыж (Шеврель и Рат, 2000):
2. Разделение ИВГ по размеру (обозначается буквой W) с шагом в 5 см от самых маленьких, где W1 15 см.
Были также предложены варианты классификации ИВГ (модификации) такими авторами, как Шумпелик (2000), Амматуро и Басси (2005), Дитц и соавт. (2007). Единая классификация, стандартизирующая оценку эффективности лечения и прочее, в рамках согласительной комиссии Европейского общества герниологов пока не разработана.