А все ли жидкости жидкие?
1. Введение
Жидкость окружает везде и всегда. Сами люди состоят из жидкости, вода дает нам жизнь, из воды мы вышли и к воде всегда возвращаемся. Но что же такое жидкость? С научной точки зрения, жидкость это – одно из агрегатных состояний вещества. Как вы себе представляете жидкость? Какими свойствами она должна обладать? В первую очередь, наверное, она должна литься, растекаться и так далее, а уж никак не выдерживать вес человека или занимать вертикальное положение, но не все в нашем мире так просто.
Однажды по телевизору я услышала такое понятие « неньютоновская жидкость». Да, мы на уроках изучаем состояния тел, но то, что представляет из себя неньютоновская жидкость, я не знала даже из курса физики. И мне стало интересно, что же это такое и какими основными свойствами обладает. Это и стало основной целью моей работы. Таким образом, цель работы – определение свойств неньютоновской жидкости и получение их экспериментальным путем.
Актуальность работы. Я считаю, что моя работа очень актуальна. В мире очень много жидкостей, которые нас окружают. И нам важно знать все виды этих жидкостей, в том числе и неньютоновская жидкость. Может, за ней будущее?
Задачи:
Методы исследования:
Объект исследования: различные жидкости в природе и их свойства, в том числе неньютоновская жидкость.
Предмет исследования: определение основных свойств жидкости экспериментальным путём.
Гипотеза: я предполагаю, что неньютоновская жидкость – это смесь, которая обладает свойствами жидкостей, а также некоторыми «особыми» свойствами.
2. Основная часть
2.1. Жидкость и её свойства
Жидкость – одно из состояний вещества, промежуточное между твердым и газообразным. Основным свойством жидкости является то, что она способна менять свою форму под действием механического воздействия. Идеальные – невязкие жидкости, обладающие абсолютной подвижностью, т.е. отсутствием сил трения и касательных напряжений и абсолютной неизменностью, а объёме под воздействием внешних сил.
Основным свойством жидкостей является текучесть. Если к участку жидкости, находящейся в равновесии, приложить внешнюю силу, то возникает поток частиц жидкости в том направлении, в котором эта сила приложена: жидкость течёт. Таким образом, под действием неуравновешенных внешних сил жидкость не сохраняет форму и относительное расположение частей и поэтому принимает форму сосуда, в котором находится. Жидкость не имеет предела текучести: достаточно приложить сколь угодно малую внешнюю силу, чтобы жидкость потекла.
Вязкостью обладают все жидкости (кроме сверхтекучей фракции жидкого гелия), и у всех она разная. Сжиженные газы очень текучи, жидкости при комнатной температуре тоже не слишком вязкие. Наибольшей же вязкостью обладают сложные жидкие системы: гели, эмульсии или суспензии, в том числе, жидкости с крайне высокой вязкостью – стёкла и аморфные твердые тела. 2
2.2. Ньютоновские и Неньютоновские жидкости.
Ньютоновской жидкостью называют жидкость, при течении которой ее вязкость зависит от градиента скорости. Обычно такие жидкости сильно неоднородны и состоят из крупных молекул, образующих сложные пространственные структуры. Исаак Ньютон – английский ученый, один из создателей новоевропейской науки. Он открыл закон вязкого трения, который устанавливает наличие линейной зависимости. Он также сформулировал основные законы классической механики (законы Ньютона), открыл закон всемирного тяготения. Что же такое неньютоновская жидкость?
Неньютоновскими, или аномальными, называют жидкости, течение которых не подчиняется закону Ньютона. Таких, аномальных с точки зрения гидравлики, жидкостей немало. Они широко распространены в нефтяной, химической, перерабатывающей и других отраслях промышленности. Если на них воздействовать резко, сильно, быстро – они проявляют свойства, близкие к свойствам твердых тел, а при медленном воздействии становится жидкостью. 3 К неньютоновским жидкостям можно отнести буровые растворы, сточные грязи, масляные краски, зубную пасту, кровь, жидкое мыло и др.
Зыбучий песок, так же как и разные виды так называемых неньютоновских жидкостей, обладает свойствами, характерными как для твердых объектов, так и для обыкновенных жидкостей. Неньютоновские жидкости состоят из мелких частиц, распределенных в жидкости, причем внешне могут напоминать твердые субстанции или гель. В Английском языке, впрочем, такие жидкости принято обозначать как “fluids”, тогда как обыкновенные жидкие вещества названы привычным словом “liquids”. 4
2.3. Исследование знаний учащихся по данной теме
Учащимся 7-9 классов была предложена анкета по исследуемой теме.
Знаете ли вы что такое жидкость?
____________________________________________________
2. может ли жидкость становится твердой? если да, то почему.
3.Слышали вы о таком понятии, как « Неньютоновская жидкость»?
4.Что может являться простейшим наглядным бытовым примером неньютоновской жидкости?
Мы получили следующие результаты.
7 класс
8 класс
9 класс
1.Знаете ли вы что такое жидкость?
2 может ли жидкость становится твердой?
Да – 6
Нет – 0
Не знаю – 8
Да – 3
Нет – 0
Не знаю – 5
Да – 3
Нет – 0
Не знаю – 6
3. Слышали вы о таком понятии, как « Неньютоновская жидкость»?
4. Что может являться простейшим наглядным бытовым примером неньютоновской жидкости?
Правильно – 1
Неправильно – 0
Не ответили – 13
Правильно – 1
Неправильно – 0
Не ответили – 7
Правильно – 1
Неправильно – 0
Не ответили – 8
На первый вопрос, знаете ли вы, что такое жидкости, мы получили следующие результаты:
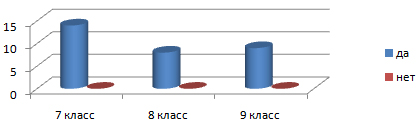
Таким образом, все тестируемые знают, что такое жидкость, и встречаются с жидкостями в жизни.
На второй вопрос, может ли жидкость становится твёрдой, мы получили следующее:
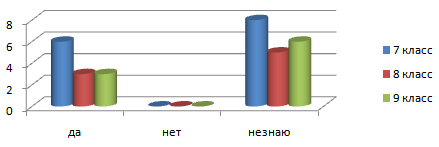
Таким образом, мы видим, что большая часть тестируемых не знают о неньютоновской жидкости и не слышали о таком свойстве жидкости, как твёрдость.
На 3 вопрос, слышали ли вы о таком понятии, как неньютоновская жидкость, были получены результаты:
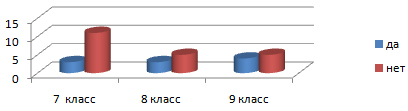
Больше половины учащихся не слышали о таком понятии, и не знают что это такое.
На 4 вопрос, что является простейшим бытовым примером неньютоновской жидкости, получили следующие результаты:
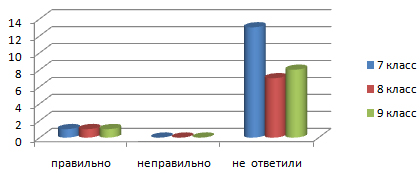
Таким образом, ровно 3 человека смогли привести примеры неньютоновской жидкости из жизни, остальные учащиеся, участвующие в опросе, не ответили ничего.
Можно сделать вывод, что учащиеся 7-9 классов знают, что такое жидкость, но ни разу не слышали о том, что жидкость может быть твёрдой. Поэтому мы решили экспериментальным путём определить основные свойства неньютоновской жидкости.
2.4. Практическая часть. Изготовление неньютоновской жидкости
Приготовление жидкости в домашних условиях:
1. Приготовьте крахмал и воду.
Берем 1 стакан воды и 2, 5 стакана крахмала.

2. Вливая воду в крахмал, медленно размешиваем массу (быстро мешать будет трудно).

3. По желанию можно добавит любой краситель. Это придаст жидкости красивый цвет.
4. Жидкость готова. Будем приступать к проведению экспериментов.
2.4. Исследование свойств ньютоновской и неньютоновской жидкости
Эксперимент №1. Определение плотности жидкости




Расчет по формуле которую известна из курса физики ρ = m/V
Неньютоновская жидкость
ρ, например, обычной воды известна из курса физики 7 класса и равна 1000 кг/м3
V измерила мерным стаканчиком = 25мл (25*10″-6″ м³)
m измерила при помощи механических весов. Масса жидкости в стакане 80 г, а масса стакана – 50. Масса смеси, без учёта массы стакана = 30 гр. (30*10″-3″ кг)
Подставила значение в формулу и получила, что ρ = 1200 кг/м³
Вывод. Таким образом, мы видим, что при расчётах и вычислениях плотности плотность неньютоновской жидкости больше, чем, например, плотность обычной воды. Это обуславливается тем, что плотность неньютоновской жидкости в нашем случае состоит из плотности крахмала и плотности воды.
Эксперимент №2. Определение скорости течения жидкости


Вычисления будем проводить по известной нам формуле
Ньютоновская жидкость
Неньютоновская жидкость.
От определённой точке на листе бумаги, мы налили немного воды. И за 18 секунд проверили, на какое расстояние наша вода растеклась.
Произвели вычисления и получили следующее:
За 15 секунд вода растеклась на расстоянии 16 см (0,16 м).
Мы произвели вычисления и получили, что скорость течения воды в данном случае равна 0,009 м/с
С неньютоновской жидкостью мы провели аналогичный эксперимент, как с водой. От определённой точки на листе бумаги мы налили неньютоновской жидкости и определили расстояние, на которое наша жидкость растеклась. Мы так же, как и в предыдущем случае, засекли 18 секунд и заметили, что неньютоновская жидкость растеклась на 10 см. (0,1 м).
При вычислении мы получили, что скорость течения неньютоновской жидкости равна 0,006 м/с
Вывод: После проведения данного эксперимента мы можем сделать вывод, что неньютоновская жидкость растекается медленнее, чем обычная вода, а всё из-за того, что проявляются свойства неньютоновской жидкости: при выливании жидкости она становится очень твёрдой и почти не растекается по листу бумаги.
Эксперимент №3. Определение давления жидкости



Вычисления проводятся по формуле определения давления жидкости.
Ньютоновская жидкость
Неньютоновская жидкость.
Эксперимент №4. Определение поведения жидкости при нагревании
В данном эксперименте у нас получилось 2 случая.
1 Случай. В данном эксперименте мы нагреем обычную, немного подкрашенную воду и неньютоновскую жидкость на газовой плите. Посмотрим в чём их схожесть и в чём их различие.


Ньютоновская жидкость
Неньютоновская жидкость
Мы используем обычную воду. Спустя некоторое время наша вода закипает и начинает испаряться.
При сильном нагревании на плите неньютоновская жидкость затвердевает, то есть из неё улетучивается вода, а на поверхности остаётся первоначальное состояние крахмала. Но если перевернуть получившуюся массу со дна на поверхность, мы заметим, что слой, который был на дне, превратился в клейстер, то есть стал очень липким и вязким. Это проявление одного из основных свойств неньютоновской жидкости.
2 Случай. В данном эксперименте мы нагреем обычную, немного подкрашенную воду и неньютоновскую жидкость на спиртовке. Посмотрим, в чём их схожесть и в чём их различие.


Ньютоновская жидкость
Неньютоновская жидкость
Мы используем обычную воду. Спустя некоторое время наша вода, как и предыдущем случае, закипает и начинает испарятся, а цвет воды в данном случае становится светлее.
В неньютоновской жидкости первоначально на дно осела краска, которую мы добавляли при изготовлении. Затем, спустя промежуток времени, из данной жидкости началась выделяться вода, а крахмал оказался на поверхности. Спустя еще некоторый промежуток времени, мы заметили, что данная жидкость начала желтеть и немного похрустывать. Когда мы убрали пробирку со спиртовки, мы заметили, что на осевшей желтоватой жидкости появились небольшие кристаллики, похожие на кристаллики льда. Таким образом, у нас образовался горячий лёд.
Таким образом, вода в обоих случаях закипает и со временем превращается в пар, а вот неньютоновская жидкость в первом случае проявляет свои клейкие и вязкие особенности, а во втором случае превращается в горячий лёд.
3. Заключение
Неньютоновская жидкость – это такая жидкость, которая в некоторых моментах ведет себя как жидкость, а в некоторых – как твердое тело. Если мы воздействуем на эту жидкость с силой, то оно становится твердым. Проще говоря, это такое вещество, которое может быть и твердым, и жидким, в зависимости от того, с какой скоростью мы с ним работаем. Если быстро толкаем, мнем, кидаем, стучим, то оно ведет себя как твердое тело, а если останавливаемся, то в наших руках оно растекается в лужицу.
При выполнении своей исследовательской работы цели и задачи, поставленные мною вначале, были достигнуты. Я узнала, что представляет собой неньютоновская жидкость, какими свойствами она обладает, смогла рассчитать некоторые из свойств жидкости: плотность и поверхностное натяжение. Таким образом, первичная гипотеза подтвердилась.
Более подробно с неньютоновскими жидкостями можно познакомиться на уроках физике, а также факультативных и кружковых занятиях.
2 Уилкинсон У.Л. Неньютоновские жидкости.- М.: Мир, 1964.
3 Энциклопедический словарь юного физика / Сост.В.А.Чуянов. – 2-е изд., испр. и доп.- М.: Педагогика, 1991.
4 Яворский Б.М., Детлаф А.А. Справочник по физике.- М.: Наука, 1979.
Синдром недостаточности пищеварения
Мальдигестия или прямая угроза для кишечника
Синдром недостаточности пищеварения или синдром мальдигестии не является редким явлением в современном мире. Одной из главных причин нарушения пищеварения принято считать недостаточную выработку пищевых ферментов, которые расщепляют компоненты пищи. Это состояние сопровождается выраженными клиническими проявлениями, которые заставляют человека обратиться за медицинской помощью.
Характеристики состояния
Синдром мальдигестии обусловлен функциональной недостаточностью поджелудочной железы, желудка или кишечника. Независимо от степени вовлеченности одного из органов пищеварительной системы, данное состояние приводит к нарушению процесса всасывания нутриентов, включая витамины и минералы. За короткий промежуток времени, расстройства пищеварения вызывают потерю массы тела, ухудшение состояния кожи и волос, негативно отражается на иммунитете человека, и провоцирует обострение любых хронических заболеваний.
Кроме того, остатки непереваренной пищи (химус) являются благоприятной средой для размножения болезнетворных организмов, с последующим развитием тяжелого кишечного дисбактериоза и аллергических реакций.
Несмотря на то, что существует отдельная (инволютная) форма мальдигестии, связанная с возрастными изменениями в организме пожилых людей, чаще всего с этим состоянием сталкиваются люди молодого и среднего возраста.
Причины развития
Одной из главных причин развития данного состояния является нарушение работы желудка или кишечника, а также поджелудочной железы с уменьшением продукции пищеварительных ферментов. К другим потенциальным факторам развития синдрома недостаточности пищеварения, можно отнести:
Нарушение процесса желчеобразования и желчевыделения.
Синдром недостаточности пищеварения условно делится на полостную, пристеночную и внутриклеточную мальдигестию. Полостная мальдигестия развивается при таких состояниях, как муковисцидоз, хроническое воспаление поджелудочной железы, а также после операций на данном органе. Снижение функциональности ферментов, ответственных за расщепление компонентов пищи, наблюдается при хроническом гастрите. Кроме того, развитию мальдигестии способствует язва желудка и синдром раздраженного кишечника, при котором наблюдается нарушение транзита химуса. Пристеночное пищеварение нарушается в том случае, если наблюдается повреждение клеток эпителия кишечника (энтероцитов). Повреждение эпителия кишечника наблюдается при целиакии, болезни Крона, а также при энтеритах различной этиологии.
Непереваренные остатки пищи, которые остаются длительное время в просвете кишечника провоцируют не только развитие дисбактериоза, но и приводят к образованию токсических компонентов (скатол, аммиак, индол), которые оказывают местнораздражающий эфеект и повреждают слизистую оболочку кишечника.
Клинические симптомы
Распознать расстройства кишечника при мальдигестии можно по таким характерным клиническим признакам:
Кроме того, для мальдигестии характерны такие симптомы, как общая слабость, частичная или полная утрата аппетита, а также снижение массы тела. У пациентов с мальдигестией наблюдается увеличение объема испражнений, при этом меняется их цвет и запах. В испражнениях наблюдается маслянистые включения (стеаторея). Синдром недостаточности пищеварения очень часто протекает в комбинации с непереносимостью лактозы (молочного сахара) или других пищевых компонентов.
При тяжелом течении, у пациентов с синдромом мальдигестией резко ухудшается общее состояние, нарушается процесс всасывания биологически-значимых компонентов и развивается мальабсорбция. На фоне данного состояния снижается масса тела, у женщин могут пропадать менструации, наблюдается ухудшение состояния кожи, волос и ногтей.
Лечение
Одним из главных условий правильного и результативного лечения мальдигестии является коррекция рациона. Из ежедневного меню исключают те продукты, которые плохо переносятся организмом. Питание усиливают продуктами, богатыми белком, углеводами и микроэлементами, при этом жиры урезают до минимума. Также, из меню исключают сырые фрукты и овощи. Стандартная терапия синдрома недостаточности пищеварения включает приём медикаментов, содержащих пищеварительные ферменты. Перестальтика кишечника восстанавливается с помощью приёма медикаментов из группы регуляторов моторики.
Для восстановления структурно-функционального состояния ЖКТ при мальдигестии и лечения дисбактериоза целесообразно использовать метапребиотики, которые бережно и эффективно нормализуют баланс кишечной и желудочной микрофлоры, подавляют рост и развитие болезнетворных микроорганизмов, а также восстанавливает поврежденный эпителий желудочно- кишечного тракта. Метапребиотик Стимбифид Плюс содержит фруктополисахариды и фруктоолигосахариды, которые являются ценным питательным субстратом для кишечной и желудочной микробиоты. Кроме того, Стимбифид Плюс дополнен лактатом кальция, стимулирующим рост и размножение полезных кишечных бактерий.
Комбинация из перечисленных компонентов позволяет добиться эффекта быстрого, безопасного и полного восстановления пищеварительной системы, пострадавшей от мальдигестии. Рациональное питание и приём метапребиотика Стимбифид плюс с профилактической целью, позволит избежать дисбиоза кишечника, расстройств пищеварительной деятельности и тяжелых осложнений, развивающихся на фоне синдрома недостаточности пищеварения. Метапребиотик может быть использован в любом возрасте.
Основные агрегатные состояния вещества
Статья находится на проверке у методистов Skysmart.
Если вы заметили ошибку, сообщите об этом в онлайн-чат (в правом нижнем углу экрана).
Агрегатные состояния вещества
Чтобы разобраться с тем, какими бывают агрегатные состояния, предлагаю по ходу чтения статьи заполнять таблицу.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
Лед, вода и водяной пар — это все три агрегатных состояния одного вещества. Лед — твердое состояние, вода — жидкая, пар — газообразное. Для каждого вещества существует три состояния.
Твердое состояние
Его очень легко представить — это любой предмет, который мы встречаем в жизни. В этом состоянии тело сохраняет форму и объем. Расстояние между молекулами, приблизительно равно размеру самих молекул, которые, в свою очередь, расположены очень структурированно.
Такая структура называется кристаллической решеткой — из-за четкой структуры молекулам сложно двигаться, и они просто колеблются около своих положений.
Заполняем нашу табличку
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
Жидкое состояние
В этом состоянии сохраняется объем, но не сохраняется форма. Например, если перелить молоко из кувшина в стакан, то молоко, имевшее форму кувшина, примет форму стакана. Кстати, в корове у молока тоже была другая форма.

Расстояние между молекулами в жидком состоянии чуть больше, чем в твердом, но все равно невелико. При этом частицы не собраны в кристаллическую решетку, а расположены хаотично. Молекулы почти не двигаются, но при нагревании жидкости делают это более охотно.
Вспомните, что происходит, если залить чайный пакетик холодной водой — он почти не заваривается. А вот если налить кипяточку — чай точно будет готов.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
Газообразное состояние
В жизни мы встречаем газообразное состояние вещества, когда чувствуем запахи. Запах очень легко распространяется, потому что газ не имеет ни формы, ни объема (он занимает весь предоставленный ему объем), состоит из хаотично движущихся молекул, расстояние между которыми больше, чем размеры молекул.
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около своего положения в кристаллической решетке
близко друг к другу
малоподвижны, при нагревании скорость движения молекул увеличивается
занимают предоставленный объем
больше размеров молекул
хаотичное и непрерывное
С агрегатными состояниями разобрались, ура! Но до сих пор неясно, каким образом у каждого вещества их целых три, и как одно переходит в другое. Для этого узнаем, что такое фазовые переходы.
Фазовые переходы: изменение агрегатных состояний вещества
При изменении внешних условий (например, если внутренняя энергия тела увеличивается или уменьшается в результате нагревания или охлаждения) могут происходить фазовые переходы — изменения агрегатных состояний вещества.
Фазовые переходы интересны тем, что все живое не Земле существует лишь благодаря тому, что вода умеет превращаться в лед или пар. С кристаллизацией, плавлением, парообразованием и конденсацией связаны многие процессы металлургии и микроэлектроники.
На схеме — названия всех фазовых переходов:

Переход из твердого состояния в жидкое — плавление;
Переход из жидкого состояния в твердое — кристаллизация;
Переход из газообразного состояния в жидкое — конденсация;
Переход из жидкого состояния в газообразное — парообразование;
Переход из твердого состояния в газообразное, минуя жидкое — сублимация;
Переход из газообразного состояния в твердое, минуя жидкое — десублимация.
График фазовых переходов
Если взять процесс превращения льда в воду, воды — в пар, и обратные действия, то мы получим очень информативный график.
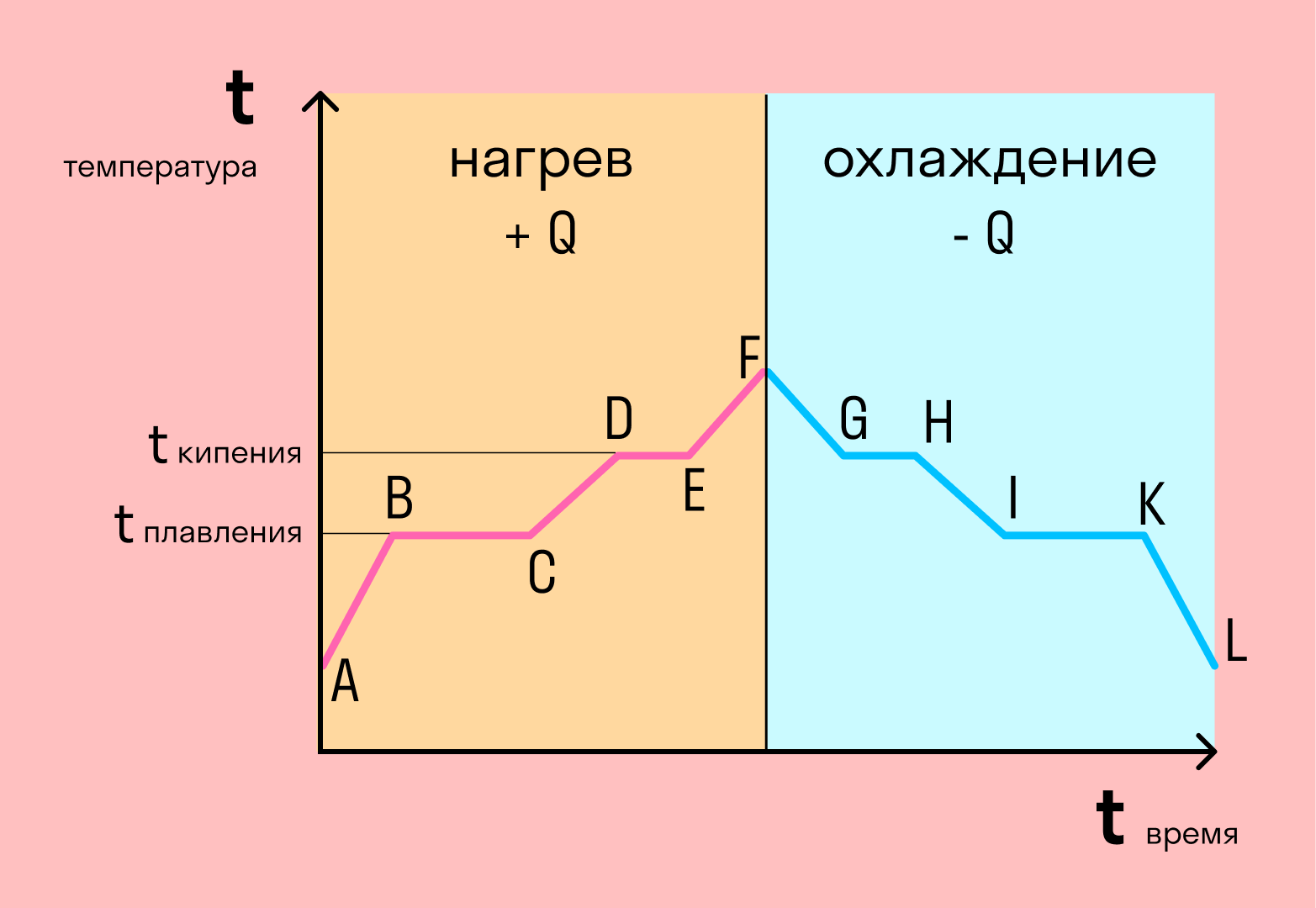
Разбираемся по шагам. Сначала взяли лед, конечно, при отрицательной температуре, потому что при нуле лед начинает плавиться. Нагрели лед до температуры плавления (до 0 градусов).
После того, как лед нагрелся до температуры плавления, он начинает плавиться. Плавление происходит при постоянной температуре тем дольше длится, чем больше масса плавящегося вещества. Еще этот процесс зависит от свойств самого вещества, но об этом немного позже.
Расправившись вещество уже в жидком состоянии снова начинает нагреваться, и температура увеличивается, пока не достигает температуры кипения. В данном случае нагревается вода — это значит, что ее температура кипения равна 100 градусам Цельсия.
При 100 градусах вода кипит, пока не выкипит целиком. В данном случае процесс аналогично плавлению происходит при постоянной температуре. Данный процесс нельзя путать с испарением, потому что парообразование происходит при конкретной температуре, а испарение — при любой.
Далее полученный пар нагревается, но путем нагревания невозможно дойти до другого фазового перехода — можно пойти только обратно.
Первый шаг в обратную сторону — охлаждение до температуры кипения.
Дойдя до температуры кипения (в данном случае 100 градусов), пар начинает переходить в жидкое состояние. Этот процесс также происходит при постоянной температуре.
Сконденсировавшись, вода охлаждается, пока не начнет замерзать.
Кристаллизуется (замерзает) вода при той же температуре, что и плавится лед — 0 градусов. Кристаллизация также происходит при постоянной температуре.
После кристаллизации лед охлаждается.
С нагреванием и охлаждением все совсем просто — мы либо передаем теплоту телу (веществу), и оно идет на увеличение температуры, либо тело отдает тепло и охлаждается.
В остальных процессах температура не меняется. Это связано с тем, что количество теплоты не всегда зависит от температуры. Формулы для всех процессов выглядят так:
Нагревание
Охлаждение
Q — количество теплоты [Дж]
c — удельная теплоемкость вещества [Дж/кг*˚C]
m — масса [кг]
tконечная — конечная температура [˚C]
tначальная — начальная температура [˚C]
Плавление
Кристаллизация
Q — количество теплоты [Дж]
λ — удельная теплота плавления вещества [Дж/кг]
m — масса [кг]
Парообразование
Конденсация
Q — количество теплоты [Дж]
L — удельная теплота парообразования вещества [Дж/кг]
m — масса [кг]
Онлайн-уроки физики в Skysmart не менее увлекательны, чем наши статьи!
Решение задач по фазовым переходам
С теорией разобрались — а теперь давайте практиковаться!
Задачка раз. Температура медного образца массой 100 г повысилась с 20 °С до 60 °С. Какое количество теплоты получил образец? Удельную теплоёмкость меди считать равной 380 Дж/(кг умножить на °С)
Q = 380 * 0,1*(60-20) = 1520 Дж
Ответ: образец получил 1520 Дж
Задачка два. Какое количество теплоты необходимо для плавления 2,5 т стали, взятой при температуре плавления? Удельная теплота плавления стали λ=80кДж/кг. Теплопотерями пренебречь.
80 кДж/кг = 80000 Дж/кг
Q = 80000*2500 = 200 000 000 Дж = 200 МДж
Ответ: для плавления 2,5 т стали необходимо 200 МДж теплоты.
Сублимация и десублимация
Мы уже рассказали про такие процессы, как сублимация и десублимация.
Примерчики из жизни🤓
Про принтеры. Цветные принтеры (только не лазерные) печатают путем сублимации. Вот как это работает: частицы краски быстро переходят из твердого состояния в газообразное и оседают на бумаге — так получается цветная картинка.
Рисуночки на окнах. Если вы решите проехаться на автобусе в холодную погоду — увидете на стеклах чудесные узоры. Из-за огромной разницы температур между улицей и автобусом, мы можем наблюдать процесс десублимации в виде красивых рисунков на стеклах. Иней образуется похожим способом — резкое похолодание приводит к десублимации воздуха.
Влажность воздуха: испарение и конденсация
Такие процессы, как испарение и конденсация, становятся более логичными и простыми, если их рассмотреть на примере влажности воздуха.
Влажность воздуха говорит нам о том, сколько в воздухе содержится водяного пара. Любое количество пара в воздух не запихнешь, поэтому, во-первых, его там очень мало, а во-вторых, при избыточном количестве водяного пара происходит конденсация — это когда образуется роса.
Как влажность влияет на человека
Для человека влажность очень важна, потому что мы состоим из воды на 90%. Если окружающей среде нечего испарять, она будет испарять нас. Поэтому при низкой влажности мы чувствуем сухость во рту, а при высокой — волосы впитывают влагу, разбухают и начинают виться. На этом принципе построены некоторые гигрометры — приборы для измерения влажности. Они так и называются — волосяные гигрометры. Только внутри не человеческий волос, а конский, но принцип от этого не меняется.
При высокой влажности холод и тепло воспринимаются более чувствительно. Это связано с потливостью человека при высокой температуре. Такой механизм помогает нам бороться с жарой, но при высокой влажности пот не может испариться. При испарении пота мы теряем избыточное тепло, а в данном случае этого не происходит.
При низкой влажности происходит нечто похожее. Как ни странно, в мороз мы тоже потеем (намного меньше, но все-таки это происходит). Если влажность на улице низкая, то пот испарится из-под куртки и нам будет комфортно, а при высокой влажности — он там задержится и будет проводить тепло наружу, забирая у нас драгоценные Джоули тепла. Поэтому зимой в Петербурге холоднее, чем в Москве.

Влажностью можно управлять. Существуют мешочки с шариками адсорбентами, которые кладут в коробки с обувью, чтобы впитать лишнюю влагу. Чтобы окна не запотевали, можно насыпать в рамы соль, которая также впитает влагу. А если вам наоборот нужно больше влаги — берем увлажнитель воздуха (классная вещь!): он добавляет в воздух водяной пар.